K0016K deltenta 4 LP3 11-12
advertisement

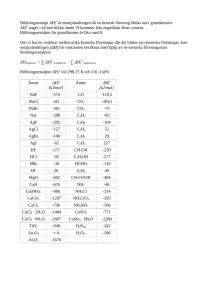
tentaplugg.nu av studenter för studenter Kurskod K0016K Kursnamn Kemiska principer Datum 2012-04-23 Material Deltentamen 4 Kursexaminator Lars Gunneriusson Betygsgränser 3 = 50-74,5%; 4 = 70-89,5%; 5 = 90-100% Tentamenspoäng 70,8% Övrig kommentar Avdelningen för kemiteknik Luleå tekniska universitet Kemiska principer, K0016K Deltentamen 4: Termodynamik Tentamensdatum: 2012-05-24 Skrivtid: 1 pass Tentamensutlämning: Nästkommande vecka Poäng och betygsberäkning: Ett medelvärde för de procentuella resultaten från deltentamen 1 till 4 beräknas. Följande betygsgränser gäller: För betyg 3 på kursen krävs medelvärdet 50 % För betyg 4 på kursen krävs medelvärdet 70 % För betyg 5 på kursen krävs medelvärdet 90 % Därutöver krävs att minst 25 % av poängsumman uppnåtts för varje enskild deltentamen. Studenter som inte uppnår godkänt betyg får vid detta kurstillfälles ordinarie tentamen själv välja vilken/vilka delar som ska skrivas om för att uppnå godkänt betyg. Det sist skrivna resultatet för den valda delen eller delarna räknas då in i slutresultatet. Observera att denna möjlighet enbart ges vid detta kurstillfälles ordinarie tentamen. Om ytterligare tentamen blir aktuellt skrivs fortsättningsvis fullständig tentamen över hela kursens innehåll. LYCKA TILL!!! Tillåtna hjälpmedel: Kemiska Data, räknare Lös endast en uppgift per inlämnat blad och märk dem med namn och personnummer. Blad utan dessa personuppgifter kommer inte att rättas. Utförliga och fullständiga lösningar/motiveringar krävs för full poäng. Anta standardtillstånd och 25 C (exakt) om inte annat anges. 1 10p Krockkuddar i bilar blåses upp, genom en reaktion där natriumazid, NaN3(s), reagerar och producerar en stor volym kvävgas. Den viktigaste reaktionen är: NaN3(s) H = -21.7 kJ mol-1 Na(s) + 1.5N2(g) a) En krockkudde blåses upp av 67.0 g kvävgas (omkring 60 dm3) Beräkna entalpiändringen vid reaktionen, samt massan natriumazid som behövdes för att bilda denna volym kvävgas. (4p) b) Anta att all reaktionsvärme åtgår till att värma den bildade kvävgasen, vilken blir då temperaturen hos gasen omedelbart efter att den bildats? Anta temperaturen 25.00 C före reaktionen. (4p) c) Vilket värde har H f för NaN3(s)? (2p) Lösning a) M(N2) = 28.01 g/mol n( NaN 3 ) n( N 2 ) 1 1.5 n(N2) = (67.0/28.01) mol 2.3920 mol n(NaN3) = (2/3) n(N2) = (2/3) (67.0/28.01) mol M(NaN3) = 65.01 g/mol 1.59466 mol m(NaN3) = 104 g H = n(NaN3) (-21.7 kJ/mol) = -34.604 kJ ( H = n(N2) (2/3) (-21.7 kJ/mol) = -34.604 kJ ) H = -34.6 kJ b) Cp(N2,g) = 29.12 JK-1mol-1 H(uppt.) - H (avg.) H = n Cp T 496.8 K 34.604 kJ T = H/(n Cp) = 34.604·103 J/(2.3920 mol·29.12 JK-1mol-1) Temperaturen blir då 25.00 C + 496.8 C 522 C (795 K) Temperaturen sjunker dock snabbt, gasens värmekapacitet är ju också låg vilket gör att risken för brännskador blir låg. Bildat Na omvandlas till ofarliga produkter genom reaktioner med andra hjälpämnen. c) Hf : ”Entalpiändringen vid bildningen av ett ämne ur grundämnena i deras stabilaste tillstånd”. Definitionsmässigt är dessa ämnens Hf -värden satta till = 0. => Na(s) + 1.5N2(g) NaN3(s) Hf = 21.7 kJ mol-1 2 14p Bränd kalk har många användningsområden, men ett av de största är till rökgasrening i kolkraftverk. Den brända kalken framställs enligt: CaCOB3(kalcit) CaO(s) + CO2(g) B B a) Beräkna H och S för reaktionen. b) Beräkna p(CO2) när processen befinner sig i jämvikt vid 100.0 C c) Vid vilken temperatur blir koldioxidtrycket 1 atm? d) Vad är den största källan till osäkerhet i beräkningen? B B (4p) (4p) (4p) (2p) Lösning a) Ämne CaO(s) CO2(g) CaCO3(s) H (kJ/mol) S (J mol-1K-1) (1) (2) (3) (1)+(2)-(3) (1)+(2)-(3) S (J mol-1K-1) 39.75 213.74 92.9 Hf (kJ/mol) -635.09 -393.51 -1206.9 178.3 160.59 S = 160. J mol-1K-1 H = 178.3 kJ/mol Obs! Att ange enheten som J/mol·K innebär (J/mol)·K, inte J/(mol·K)! Bättre då att skriva Jmol-1K-1 b) CaCO3(s) Generellt: CaO(s) + CO2(g) 1 pCO2 CaO CO2 CaCO3 1 1 T H R ln K G° = H° - T S° = -RTlnK 178.3 10 3 1 8.314510 373.15 ln K K pCO2 S R 160.59 = -38.1543 8.314510 K = p(CO2) = 2.69 10-17 bar c) p(CO2) = 1.013 bar bar H 1 S ln K R T R R ln K T H 1 T S K = 1.013 ln K S H R R ln K H S R 1 T 1 T T S H R ln K 178.3 10 3 K =1111 K 8.314510 ln 1.01325 160.59 t = 838 C (1.11 103 K) d) Antagandet att H (och S ) är temperaturoberoende. Vid en noggrannare beräkning, så behövs data på dessa storheters temperaturberoende.