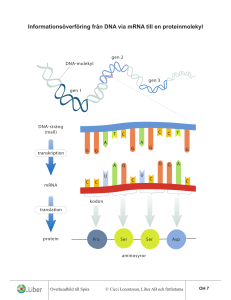
Mutations- analys av KRAS inför riktad terapi vid
advertisement

n klinik och vetenskap originalstudie Mutationsanalys av KRAS inför riktad terapi vid kolorektalcancer Kvalitetskontroll av molekylärpatologiska metoder i Sverige FREDRIK ENLUND, docent, Klinisk molekylär patologi, verksamheten för patologi och cytologi, Sahlgrenska universitetssjukhuset, Göteborg [email protected] GISELA HELENIUS, PhD, laboratoriemedicinska kliniken, enhet patologi, Universitetssjukhuset i Örebro RICHARD PALMQVIST, lektor, överläkare, Klinisk patologi, Norrlands universitetssjukhus; Medicinsk biovetenskap, patologi, Umeå universitet ANDERS EDSJÖ, med dr, ST-läkare, Labmedicin Skåne, Klinisk patologi, Malmö MAGNUS SUNDSTRÖM, PhD, avdelningen för molekylärpatologi, sektionen för klinisk patologi och cytologi, Akademiska sjukhuset, Uppsala Kostnaden för riktade terapier inom cancervården har ökat kraftigt de senaste åren. Terapierna består av antingen antikroppar riktade mot receptorer på cellytan eller intracellulära tyrosinkinasinhibitorer med syfte att hindra tumörcellens okontrollerade cellsignalering. Riktad terapi i kombination med traditionell cytostatikabehandling har använts med goda resultat på ett flertal tumörtyper under de senaste åren, med paradexempel som imatinib (Glivec) vid kronisk myeloisk leukemi och trastuzumab (Herceptin) vid vissa typer av bröstcancer. Specifikt för de riktade terapierna är att de bör föregås av en genetisk karakterisering av patientens tumör för att förutsäga individens respons. Adekvata, kvalitetssäkrade och behandlingsstyrande test är därför viktiga och kommer att få allt större betydelse då nya riktade terapier är på väg in i klinisk rutinbehandling. Nätverk för klinisk validering Många av de behandlingsstyrande testen för främst solida maligniteter utförs av laboratorier inom den nya gren av patologin som kallas molekylärpatologi. Under de senaste åren har antalet genetiska analyser på formalinfixerad paraffininbäddad vävnad ökat med exempel som FISH-analys av HER2 och mutationsundersökningar av cKIT, PDGFRA och nu senast även KRAS. Samspelet mellan traditionell histopatologisk granskning och molekylärpatologisk analys är viktigt och innebär en interaktion mellan patologen, som gör ett urval av vilken vävnad som ska analyseras, och molekylärgenetikern, som utför analysen på DNA extraherat från utvald läkartidningen nr 5 2010 volym 107 tumörvävnad. Resultaten tolkas därefter ofta gemensamt av de specialiserade yrkeskategorierna, vilket ställer krav på organisatorisk samlokalisation (varje patologenhet bör ha tillgång till molekylärgenetisk apparatur och kompetens). I den här artikeln beskrivs arbetet inom ett nybildat nationellt nätverk för klinisk molekylärpatologi med att validera mutationsstatusanalys av KRAS-genen. Analysen utförs inför eventuell riktad terapi med monoklonala antikroppar vid metastaserande kolorektalcancer. Liknande kvalitetsgrupper för HER2-analyser vid bröstcancer (HER2-analysgruppen) har under det senaste decenniet med stor framgång arbetat med kvalitetskontroll av analyser och formulering av nationella riktlinjer för FISH-analyserna [1]. Kolorektalcancer och anti-eGFR-terapi Kolorektalcancer är efter prostata- och bröstcancer den vanligaste formen av cancer i Sverige. År 2007 registrerades runt 6 000 nya fall, vilket utgör drygt 11 procent av all rapporterad tumörsjukdom [2]. I dag finns det två godkända riktade terapier mot kolorektalcancer på marknaden. De två preparaten, cetuximab (Erbitux) och panitumumab (Vectibix), är båda monoklonala antikroppar och verkar genom att binda till och blockera receptorn epithelial growth factor receptor (EGFR). EGFR är en tillväxtfaktorreceptor vars aktivitet leder till intracellulär signalering, som resulterar i tumörcellsproliferation, minskad apoptos, ökad metastasbildning och aktivering av tumörrelaterad angiogenes [3]. De båda anti-EGFRpreparaten reducerar risken för tumörprogression och förbättrar den progressionsfria överlevnaden samt livskvaliteten hos patienter med behandlingsrefraktär kolorektalcancer [4-6]. Det är dock bara hos en mindre grupp av patienter, 8–23 procent, som man kan se behandlingsrespons av cetuximab [4, 5] eller panitumumab [6]. KRas-mutationer i kolorektalcancer Mutationer i EGFR förekommer sällan i kolorektalcancer, till skillnad från i lungcancer [7], och har därför lågt värde som behandlingsstyrande markör. Nedströms EGFR i den intracellulära signaleringskedjan finns proteinet KRAS. Specifika mutationer i KRAS leder till att proteinet aktiveras oberoende av stimulering av receptorn. Enligt litteraturen är KRAS muterad i kodon 12 eller 13 i 30–40 procent av alla kolorektalcancrar, och mer än 3 000 fall av KRAS-mutationer har hittills rapporterats till Sangerinstitutets databas [7]. De flesta mutationerna som har beskri- n sammanfattat Behandling av cancerpatienter med nya riktade terapier medför krav på implementering och kvalitetssäkring av behandlingsstyrande molekylärpatologiska analyser. 30–40 procent av alla patienter med kolorektalcancer har en mutation i genen KRAS. Mutationen resulterar i ett ständigt aktivt protein, som gör tumören resistent mot anti-EGFR-behandling med t ex cetuximab (Erbitux) och panitumumab (Vectibix). Därför måste KRAS-mutationsstatus fastställas innan eventuell behandling med dessa läkemedel inleds. Ett svenskt projekt för kvalitetskontroll beskrivs, där histologisk bedömning av kolorektaltumörvävnad samt metoder för DNA-extraktion och KRAS-mutationsanalys har utvärderats. Känsligheten i KRAS-analyserna har också utvärderats genom att jämföra erhållen mutationsfrekvens för respektive mutationsanalys i det totala antalet analyserade kolorektalcancerfall i Sverige. 255 n klinik och vetenskap vits är lokaliserade i exon 2, kodon 12 (ca 82 procent) och 13 (ca 17 procent), men mutationer har också påvisats i kodon 59, 61 och 146. Flera studier har visat att mutationer i kodon 12 och 13 starkt korrelerar med resistens mot cetuximab eller panitumumab [8, 9]. Därför har den europeiska läkemedelsmyndigheten, European Medicines Agency, EMEA ‹http://www. emea.europa.eu/›, godkänt dessa två preparat för behandling av patienter med EGFR-uttryckande, metastaserande kolorektalcancer med icke-muterat (vildtyp) KRAS. Vidare rekommenderar EMEA att utvärdering av mutationsstatus för KRAS ska utföras av ett erfaret laboratorium med validerad testmetod [10]. Noterbart är att den kliniska betydelsen av KRAS-mutationer i kodon 61 eller 146 ännu inte är fullständigt klarlagd men att indikationer finns att även dessa mutationer ger resistens mot anti-EGFR-behandling [11]. Metod Ett första steg för att nationellt kvalitetskontrollera KRASanalyserna togs hösten 2008 genom ett samarbetsprojekt inom det svenska nätverket för klinisk molekylärpatologi. Projektet samordnades från Sahlgrenska universitetssjukhuset i Göteborg, och de molekylärpatologiska laboratorierna i Umeå, Uppsala, Örebro, Göteborg och Malmö bidrog med kolorektaltumörvävnad för DNA-extraktion och KRAS-analys. Syftet med studien var att histologiskt granska kolorektaltumörvävnader och jämföra hur olika patologer bedömer relevant tumörområde för den molekylärpatologiska analysen. Dessutom har olika extraktionstekniker av DNA från den formalinfixerade paraffininbäddade tumörvävnaden utvärderats. Slutligen har även en jämförelse gjorts av resultaten från tre oberoende analysmetoder för detektion av KRAS-mutationer. Studien kallades följaktligen HEMRAS (Histologi, Extraktion, Mutation RAS) och kan ses som en mindre pilotstudie avseende kvalitetskontroll. Nio molekylärpatologiska laboratorier deltog i studien (Umeå, Uppsala, Stockholm, Linköping, Örebro, Göteborg, Helsingborg, Malmö och Lund). I studien analyserades material från tio olika kolorektaltumörer från formalinfixerat paraffininbäddat material (FFPE). Inledningsvis utvärderade en gastrointestinalt inriktad patolog materialet enligt WHO:s klassifikation för differentieringsgrad [12] samt angav hur stor andel viabla tumörceller som fanns i preparatet och markerade lämpligt tumörområde för eventuell makrodissektion (Histologi). Därefter utfördes en DNA-extraktion från FFPEmaterial, där samtliga laboratorier använde den rutinmetod som finns uppsatt på respektive enhet (Extraktion). Slutligen analyserades proven för mutationer i KRAS-genen med gängse detektionsmetod för respektive laboratorium (Mutation). Följande DNA-extraktionsmetoder utvärderades: QIAamp DNA FFPE Tissue Kit, QIAamp DNA minikit och Qiagen EZ1 (robot). Metoder för mutationsanalys var Sangersekvensering (ABI), pyrosekvensering (QIAGEN) och TheraScreen K-RASmutationsanalys (DxS), en metod baserad på realtids-PCR (för teknisk beskrivning av respektive metod, se Fakta 1). Resultat Vad gäller histologisk bedömning och DNA-extraktion bedömdes samtliga tio kolorektalcancervävnader likvärdigt av patologerna. Alla laboratorier extraherade DNA av bra kvalitet (optisk densitet, OD, 1,8–2) oberoende av vald teknik. Ingen påvisbar skillnad kunde hittas mellan QIAamp DNA FFPE och QIAamp DNA mini-metoderna, dock uppvisades ett lägre DNA-utbyte med det automatiserade Qiagen EZ1-systemet (3–10 gånger lägre utbyte). Alla deltagande laboratorier påvi256 n fakta 1 Sangersekvensering är numera en rutinmetod på de flesta molekylärgenetiska laboratorier och används för bestämning av DNA-sekvens. • I det första steget amplifieras målsekvensen med PCR och renas därefter från överblivna primrar och nukleotider. • Den renade PCR-produkten amplifieras sedan ytterligare en gång med en specifik sekvenseringsprimer och fluorescerande terminerande nukleotider som, då de inkorporeras, hind­ rar reaktionen att fortsätta. • Därmed stoppas förlängningen av DNA-kedjan, vilket ger upphov till olika långa fragment med olika termineringsnukleotider. • Fragmenten separeras i en tunn kapillär och detekteras med hjälp av laser, där de olika termineringsmolekylerna ger ifrån sig en signal vid olika våglängder, vilket görs om till toppar i olika färger i ett s k ferogram (Figur 1 A). • Fördelen med tekniken är att den är relativt billig, robust och har lång läsram (500–700 bp). • Nackdelen är att tekniken är beroende av rena material och att andelen tumörceller i det analyserade provet måste vara minst 30–40 procent för att med säkerhet kunna påvisa en mutation. Pyrosekvensering är en svenskutvecklad sekvenseringsmetod som har visat sig användbar främst för identifiering av mutationer och för analys av enbaspolymorfier (SNP) och DNAmetyleringsstatus. • En mutationsanalys av KRAS med pyrosekvensering baseras på DNA-syntes, där varje inbunden nuk­leotid ger upphov till en ljussignal. • Ljussignalens styrka är direkt proportionell till antalet bundna nukleotider, vilket innebär att resultatet från mutationsanalysen ger svar inte bara på muta- tionsstatus utan även en kvantifiering av den andel av det analyserade DNA som uppvisar en eventuell mutation (Figur 1 C). • Förutom detektion av de sju vanligaste KRAS-mutationerna ges med pyrosekvensering en möjlighet att studera övriga beskrivna KRAS-mutationer i kodon 12, 13 och 61. I likhet med mutationer i kodon 12 och 13 ger mutationer i kodon 61 ett konstitutivt aktiverat KRAS-protein, vars kliniska betydelse nu börjat undersökas [11]. • Nyligen har en diagnostisk pyrosekvenseringsanalys, PyroMark KRAS kit (QIAGEN), lanserats. Denna CEcertifierades i maj 2009 genom ett samarbete med enheten för molekylärpatologi vid Akademiska sjukhuset i Uppsala. TheraScreen (allelspecifik PCR) Den analys som används av de flesta laboratorier i Sverige är TheraScreen K-RAS mutation kit (DxS, Ltd/Qiagen). • Analysen är CE-märkt, baserad på realtids-PCR och detekterar de sju olika KRAS-mutationer som är lokaliserade till kodon 12 och 13 som i dag rekommenderas som grund för behandlingsbeslut (12Ala, 12Asp, 12Arg, 12Cys, 12Ser, 12Val och 13Asp). • Analysens styrka är dess sensitivitet (enligt specifikationerna krävs endast 1 procent muterade celler) och robusthet men med reagenskostnad som nackdel. • Rent tekniskt grundas sensitiviteten på två egenskaper hos analysen, den förs­ ta att enbart muterat DNA amplifieras, mångfaldigas, den andra att samma selektivitet även återfinns i detektionssteget. Denna selektivitet är å andra sidan en begränsning om frågetecken skulle uppkomma kring fall av någon annan ovanligare mutation än de sju som analyseras. läkartidningen nr 5 2010 volym 107 n klinik A T G och vetenskap G/A T G G C G T A G G B A: 15 % C: 0 % G: 85 % T: 0 % C 125 A: 1 % G: 99 % 100 75 50 25 0 E S T A C G A C T C A G A T G C G T A G Figur 1. Exempel på provresultat från Sangersekvensering (A), TheraScreen KRAS-mutationsanalys (B) och pyrosekvensering (C). Provets tumörceller (som här är i minoritet jämfört med normala celler) uppvisar en kodon 12 GGT>GAT-mutation som identifieras genom en extra nukleotid A-signal (A och C). Med TheraScreenmetoden identifieras mutationen genom närvaro av en extra PCR-produkt som härstammar från de muterade tumörcellerna (B). sade samma förändringar i KRAS-kodon 12 eller 13 i samtliga tio prov oberoende av använd analysmetod (Sangersekvensering, pyrosekvensering eller TheraScreen). Se Figur 1 för exempel på resultat med de olika teknikerna. Känsligheten i KRAS-analyserna har utvärderats genom att jämföra uppnådd mutationsfrekvens för respektive teknik med det totala antalet analyserade kolorektalcancerfall (416) i Sverige. Sammanställning av data från de nio deltagande laboratorierna redovisas i Tabell I. dIsKussIoN Huvudfrågan för HEMRAS-studien, om den analys av KRASmutationsstatus som utförs av de svenska molekylärpatologiska laboratorierna är pålitlig, kan angripas på flera sätt. Ett sätt är att undersöka samstämmigheten mellan svaren i det aktuella utskicket, ett annat att analysera om de ingående laboratoriernas mutationspanorama stämmer överens med varandra och med den mutationsfrekvens som rapporterats i tidigare studier. samstämmighet och pålitliga resultat Vad gäller de tio analyserade proven i denna studie kan konstateras att samma mutationsstatusresultat uppnåddes oavsett laboratoriebedömning av tumörområde eller vald metod för snittning, DNA-preparation och mutationsanalys. Det är läkartidningen nr 5 2010 volym 107 taBell I. Fördelning av antal kolorektalcancerfall som analyserats med respektive mutationsdetektionsteknik vid samtliga KRASanalyserande laboratorier i Sverige (till och med 30 november 2008). Sangersekvensering Pyrosekvensering DxS Totalt Antal fall 108 194 114 416 KRAS-mutationer i kodon 12 eller 13, procent 36 38 37 37 givetvis klokt med en viss försiktighet vad gäller slutsatser utifrån ett så begränsat antal prov, men resultaten stämmer väl överens med den slående samstämmighet vad gäller mutationsfrekvens som fanns såväl mellan olika laboratorier som mellan olika analysmetoder. Att mutationsfrekvensen i de 416 undersökta fallen som rapporteras i denna studie stämmer så pass väl med uppgifter från de 3 158 undersökta tumörerna i Sangerinstitutets databas CGP, 37 procent för bägge materialen, stärker ytterligare bilden av en pålitlig analys [7]. Enligt vår bedömning ger samtliga utvärderade metoder för mutationsanalys ett pålitligt resultat. Vid val av analysmetod finns alltså utrymme för att väga in de egenskaper som ändå 257 n klinik och vetenskap skiljer metoderna åt: sensitivitet och pris. Den allelspecifika PCR-metoden från DxS anges detektera 1 muterad cell mot en bakgrund av 100 analyserade celler, vilket förstås ökar möjligheten att få ett pålitligt svar även från ett suboptimalt material. Realtids-PCR kräver för de flesta molekylärbiologiska laboratorier heller inga nyinvesteringar i apparatur. Å andra sidan är reagenskostnaden betydligt större än för pyro- och Sangersekvensering. Pyrosekvensering är också relativt känslig, i storleksordningen 1 muterad cell mot en bakgrund av 10–20 celler kan detekteras [13], och dessutom kvantitativ och snabb. Kostnaderna för reagens är lägre, men metoden är etablerad hos färre laboratorier och kan därmed innebära investeringskostnader vad gäller apparatur. Sangersekvensering slutligen är den mest flexibla och reagensmässigt billigaste metoden och ger dessutom mest information. Metoden är dock mer tidskrävande och ställer, på grund av lägre detektionskänslighet, högre krav på det histologiska grundarbetet, vilket också kan leda till totalt högre arbetskostnader. Kunskapen räcker tyvärr inte Räcker då kunskap om KRAS-mutationsstatus för att förutsäga möjligheterna att framgångsrikt behandla med antiEGFR-terapi? Svaret är tyvärr nej. Även om en aktiverande mutation i KRAS mycket starkt talar mot behandlingssvar [8, 14] bär bara 30–40 procent av de patienter som inte svarar på anti-EGFR-terapi på en sådan mutation. Det finns i dag en hel del som talar för att bakgrunden till den resistens som ses hos patienter utan aktiverande mutationer i KRAS är andra genetiska förändringar i de gener som kodar för proteiner i signalvägarna nedströms EGFR. Stöd från retrospektiva studier finns t ex för en betydelse av mutationer i BRAF, precis nedströms KRAS, och i PIK3CAgenen, som kodar för ett protein av central betydelse i den andra huvudsignalvägen aktiverad av tyrosinkinasreceptorer, PI3K/AKT-signalvägen [15, 16] (Figur 2). Därutöver finns resultat från mindre studier som talar för betydelsen av förlust av PTEN, ett protein som normalt ska hämma aktiviteten av just PI3K [17, 18]. Det finns alltså ett flertal retrospektiva studier, men ännu saknas en motsvarighet till de större, prospektiva studier som kraftigt bidragit till KRAS nuvarande position som ledande behandlingsprediktiva faktor vid antiEGFR-terapi mot kolorektalcancer [8, 9, 14, 19]. Nästa steg i kvalitetsarbetet Hur ser nästa steg i kvalitetsarbetet ut? Nationella eller regionala kvalitetskontrollutskick finns i dag i ett flertal europeiska länder. För enheter som så önskar finns också ett tyskt program med tio tumörprov per omgång, öppet även för utländska laboratorier (QuIP, Deutsche Gesellschaft für Pathologie e.V.). Den europeiska patologföreningen, European Society for Pathology, har också sammanfattat beskrivningar och rådgivande slutsatser från ett konsensusmöte i samband med föreningens internationella kongress i Barcelona 2008. Dessa slutsatser sammanfattades i en beskrivande och rådgivande artikel hösten 2008 [10]. Som ett tredje steg startas nu en europeisk supportsida, och ett europeiskt kvalitetssäkringsprogram har sjösatts. KoNKlusIoN I takt med att fler riktade terapier introduceras så kommer kvalitetsarbete liknande detta att framgent vara en naturlig del av svensk rutinsjukvård. Den molekylära patologin är väletablerad inom sjukvården i Europa och på frammarsch inom svensk sjukvård, och vi som är aktiva inom fältet vill slutligen 258 P KRAS P Pl3K PLCγ PTEN BRAF MEK PKC Akt ERK mTOR Apoptos Migration Proliferation Överlevnad Figur 2. Schematisk presentation av EGFR-signalering. Stimulering och dimerisering av EGFR leder till receptorfosforylering (P) och aktivering av ett flertal intracellulära signaleringsvägar nedströms EGFR. Signaleringen leder till förändrad aktivitet hos gener involverade i diverse cellulära svar, såsom överlevnad, proliferation (celldelning) och migration. Figuren är modifierad efter ett original av dr Patrick Micke, Akademiska sjukhuset, Uppsala. poängtera vikten av samverkan mellan sjukvårdens olika specialiteter och kompetenser, som i detta fall patologi, onkologi och genetik, för att tillsammans kunna erbjuda bästa möjliga individanpassade behandling för den enskilda patienten. n Potentiella bindningar eller jävsförhållanden: Inga uppgivna. n Deltagande laboratorier i kvalitetsutskicket: Karolinska univer- sitetssjukhuset, enheten för patologi/cytologi, Mehran Ghaderi och Johan Lindholm; Universitetssjukhuset i Linköping, Klinisk patologi, Martin Hallbeck; Helsingborgs lasarett, Klinisk patologi, Patrick Joost; Universitetssjukhuset i Lund, forskningsenheten onkologen, Mats Jönsson. Medarbetare vid Sahlgrenska universitetssjukhuset i Göteborg, Klinisk patologi och cytologi, Pushpa Saksena, Carina Karlsson, Lisbeth Gustafsson och Carola Andersson; Akademiska sjukhuset i Uppsala, sektionen för klinisk patologi och cytologi, Johan Botling, Patrick Micke, Monica Lindell och Karolina Edlund; Universitetssjukhuset i Örebro, enheten för patologi, Sune Eriksson, Gabriella Lillsunde-Larsson och Anna-Lena Ohlsson; Norrlands universitetssjukhus i Umeå, Klinisk genetik, Irina Golovleva; Universitetssjukhuset i Malmö, Klinisk patologi, Malin Goldman, Malgorzata Tomaszewska, Christer Halldén och Britta Halvarsson. Kommentera denna artikel på Lakartidningen.se REFERENSER 1. Fernö M, Haglund M, Bendahl PO, Olsson H, Rydén L. Analys av HER2 i bröstcancer kvalitetssäkrad. Viktig behandlingsprediktiv och prognostisk faktor. Läkartidningen. 2008;105(32-33):2181-4. 2. Socialstyrelsen. Cancerstatistik för 2007. http://www. socialstyrelsen.se/uppfoljning/ statistik/statistikdatabas 3. Ciardiello F, Tortora G. EGFR antagonists in cancer treatment. N Engl J Med. 2008;358(11):1160-74. 4. Jonker DJ, O’Callaghan CJ, Karapetis CS, Zalcberg JR, Tu D, Au HJ, et al. Cetuximab for the treatment of colorectal cancer. N Engl J Med. 2007;357(20):2040-8. 5. Cunningham D, Humblet Y, Siena S, Khayat D, Bleiberg H, Santoro A, et al. Cetuximab monotherapy läkartidningen nr 5 2010 volym 107 n klinik och vetenskap and cetuximab plus irinotecan in irinotecan-refractory metastatic colorectal cancer. N Engl J Med. 2004;351(4):337-45. 6. Peeters M, Siena S, Van Cutsem E, Sobrero A, Hendlisz A, Cascinu S, et al. Association of progressionfree survival with patient-report­ ed outcomes and survival: results from a randomised phase 3 trial of panitumumab. Br J Cancer. 2007; 97(11):1469-74. 7. Catalogue of somatic mutations i cancer. www.sanger.ac.uk/ genetics/CGP/cosmic 8. Allegra CJ, Jessup JM, Somerfield MR, Hamilton SR, Hammond EH, Hayes DF, et al. American Society of Clinical Oncology provisional clinical opinion: testing for KRAS gene mutations in patients with metastatic colorectal carcinoma to predict response to anti-epidermal growth factor receptor monoclonal antibody therapy. J Clin Oncol. 2009;27(12):2091-6. 9. Lièvre A, Bachet JB, Boige V, Cayre A, Le Corre D, Buc E, et al. KRAS mutations as an independ­ ent prognostic factor in patients with advanced colorectal cancer treated with cetuximab. J Clin Oncol. 2008;26(3):374-9. 10. van Krieken JH, Jung A, Kirchner T, Carneiro F, Seruca R, Bosman FT, et al. KRAS mutation testing for predicting response to antiEGFR therapy for colorectal carcinoma: proposal for an European quality assurance program. Virchows Arch. 2008;453(5):41731. 11. Loupakis F, Ruzzo A, Cremolini C, Vincenzi B, Salvatore L, Santini D, et al. KRAS codon 61, 146 and BRAF mutations predict resist­ ance to cetuximab plus irinotecan in KRAS codon 12 and 13 wildtype metastatic colorectal cancer. Br J Cancer. 2009;101(4):715-21. 12. Hamilton SR, Aaltonen LA, editors. WHO Classification of tu- 13. 14. 15. 16. mours. Pathology and genetics. Tumours of the digestive system. Lyon: IARC Press; 2000. Ogino S, Kawasaki T, Brahmandam M, Yan L, Cantor M, Namgyal C, et al. Sensitive sequencing meth­od for KRAS mutation detection by Pyrosequencing. J Mol Diagn. 2005;7(3):413-21. Van Cutsem E, Köhne CH, Hitre E, Zaluski J, Chang Chien CR, et al. Cetuximab and chemotherapy as initial treatment for metastatic colorectal cancer. N Engl J Med. 2009;360(14):1408-17. Di Nicolantonio F, Martini M, Molinari F, Sartore-Bianchi A, Arena S, Saletti P, et al. Wild-type BRAF is required for response to panitumumab or cetuximab in metastat­ ic colorectal cancer. J Clin Oncol. 2008;26(35):5705-12. Sartore-Bianchi A, Martini M, Molinari F, Veronese S, Nichelatti M, Artale S, et al. PIK3CA mutations in colorectal cancer are asso- ciated with clinical resistance to EGFR-targeted monoclonal antibodies.Cancer Res. 2009;69 (5):1851-7. 17. Frattini M, Saletti P, Romagnani E, Martin V, Molinari F, Ghisletta M, et al. PTEN loss of expression predicts cetuximab efficacy in metastatic colorectal cancer patients. Br J Cancer. 2007;97(8): 1139-45. 18. Perrone F, Lampis A, Orsenigo M, Di Bartolomeo M, Gevorgyan A, Losa M, et al. PI3KCA/PTEN deregulation contributes to im­­­paired responses to cetuximab in metastatic colorectal cancer patients. Ann Oncol. 2009;20(1): 84-90. 19. Karapetis CS, Khambata-Ford S, Jonker DJ, O’Callaghan CJ, Tu D, Tebbutt NC, et al. K-ras mutations and benefit from cetuximab in advanced colorectal cancer. N Engl J Med. 2008;359:1757-65. Vi bevakar dina jobbintressen Beställ vår bevakningstjänst så mailar vi jobben som passar just dig! Gå in på Lakartidningen.se Utmanande saklig läkartidningen nr 5 2010 volym 107 259