Introduktion till kromatografi
advertisement

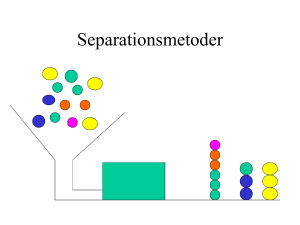
Introduktion till kromatografi Med hjälp av kromatografi separerar man komponenter i en blandning. Kromatografiska tillämpningar bygger på användningen av en stationär fas och en rörlig fas. Till olika kromatografer kan varierande detektorer adderas, antingen kvantitativa eller kvalitativa. I en kromatograf befinner sig komponenterna som skall separeras i den rörliga fasen. Som känt är har olika ämnen olika kemiska och fysiologiska egenskaper. Tack vare de olika egenskaperna bromsas olika ämnen olika mycket upp av den stationära fasen. Tiden för hur länge ett ämne befinner sig inne i kromatografen kallas retensionstid. Alltså: olika ämnen får olika långa retensionstider i och med deras olika egenskaper, Schema 1 & Schema 2. Det finns ett flertal kromatografiska tekniker. Här nämns endast några av dem TLC Thin layer chromatography Tunnskikts kromatografi GC Gas chromatography Gaskromatografi LC/Flash Flash column chromatography LC, vätskekromatografi IEC Ion exchange chromatography Jonbyteskromatografi SEC Size exclusion chromatography Uteslutningskromatografi/storlekskroamtografi Schema 1 klargör den kromatografiska principen. Ett ämne fördelas mellan en rörlig fas och en fast fas och fördröjs därför. Olika ämnen fördröjs olika mycket vilket gör att de separerar från varandra. Schema 2 illustrerar hur kromatografi används för att separera och kvantifiera ett provs beståndsdelar. Substanser som analyseras är upplösta i den mobila fasen som pumpas genom en kolonn vilken är fylld med en stationär fas. Olika ämnen, beroende på sina kemiska egenskaper, vandrar olika snabbt genom kolonnen. De separerade molekylerna kan sedan detekteras t.ex. med hjälp av en UV-absorbansdetektor vars utslag är proportionell mot koncentrationen av en viss substans i provet. Demonstrationer 1. TLC / Thin layer chromatography / Tunn skikts kromatografi Utförs i Auditoriet. Schema 3 illustrerar hur man med TLC kan separera komponenterna i en blandning genom att de i olika grad följer med vätskan som sugs upp på en tunnskiktsplatta. Schema 4 beskriver hur man i praktiken kan använda TLC för att kontrollera att en reaktion är färdig. Till vänster jämför vi reaktionsblandningen (R) vid start med referensprover av ren X, Y och Z. När reaktionen har gått halvvägs (mitten) har produkten Z bildats i reaktionsblandningen samtidigt som X och Y inte är förbrukade. Till höger ser vi hur det ser ut när reaktionen gått färdigt, startmaterialen är förbrukade och reaktionsblandningen innehåller enbart produkten Z. 2. LC/Flash / Flash column chromatography / LC, vätskekromatografi I demonstration 2 går vi och tittar på vätskekromatografiska system som är beskrivna i schema 5 och schema 6. Plats: forskningslaborationerna. Schema 5 Traditionell vätskekromatografi (flash kromatografi). Schema 6 HPLC med en fraktions samlare. 3. GC / Gas chromatography / Gaskromatografi Demonstration av en GC och GC/MS utförs nära kurslabbet. Schema 7 beskriver funktionsprincipen för en GC. Källor: Organisk Kemi, Ulf Ellervik och Olov Sterner, Studentlitteratur, 1’a upplagan, 2004 Wikipedia.org Självstudier Organisk Kemi, Ulf Ellervik och Olov Sterner, Studentlitteratur, 1’a upplagan, 2004 http://www.wikipedia.org/ chromatography http://chromatographyonline.findpharma.com