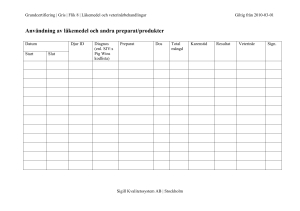
1 (3) Det har uppstått störningar i tillgången till
advertisement

1 (3) 19.5.2015 Uppdaterat 26.5.2015 Uppdaterat 13.8.2015 Uppdaterat 17.9.2015 Uppdaterat 6.10.2015 Uppdaterat 11.11.2015 Uppdaterat 21.1.2016 Uppdaterat 4.2.2016 Det har uppstått störningar i tillgången till penicillinpreparat avsedda för produktionsdjur . Detta beror på bristen på den aktiva substansen i Europa och gäller flera veterinärmedicinska preparat som innehåller bensylpenicillin Frågor och svar om tillgången till veterinärmedicinska preparat som innehåller bensylpenicillin 1. Vad är en störning i tillgången? Läkemedelspreparatet kan inte importeras på normalt sätt. Det kan finnas olika orsaker till detta. Den nuvarande situationen beror på att det råder brist på den aktiva substansen i veterinärmedicinska preparat som innehåller bensylpenicillin (bensylipenisillinprokain) i världen. 2. Gäller problemet endast Finland? Störningarna i tillgången till bensylpenicillinpreparat avsedda för produktionsdjur gäller hela EU-området och ärendet har behandlats i samarbete med Europeiska läkemedelsmyndigheten och myndigheterna i de övriga EES-länderna. 3. Finns det närmare uppgifter om tidpunkten för störningarna i tillgången? Det är möjligt att det blir ett avbrott i tillgången till bensylpenicillinpreparat för djur i början av hösten, om tilläggspartier inte fås in. I fråga om vissa förpackningsstorlekar kan det uppstå störningar i tillgången till injektionspreparat redan under slutet av sommaren, men med en normalförbrukning bedöms totallagret (alla preparat och förpackningar) räcka fram till början avseptember. Försäljningslagret för det intramammära preparatet i frågan räcker uppskattningsvis fram till början av augusti, om ytterligare leveranser inte fås. Uppdaterad 26.5.2015 Ytterligare leveranser för det intramammära preparatet i frågan har bekräftats. Enligt den nya beräkningen, med en normalförbrukning, bedöms totallagret för det intramammära preparatet i frågan räcka fram till slutet av oktober. Uppdaterat 13.8.2015 Användningen av de obligatoriskt lagrade injektionspreparaten som innehåller bensylpenicillin har påbörjats och preparaten får användas endast enligt Eviras bindande användningsrekommendationer. Genom att begränsa användningen strävar man till att säkra tillgången av preparaten till de viktigaste användningsområdena under hela störningsperioden. Med en genomsnittlig förbrukning bedöms lagret (alla preparat och förpackningar, inkluderande de obligatoriska lagren) räcka fram till mitten av november om inga kompletterande leveranser fås. Uppdaterad 17.9.2015 Ytterligare leveranser för både det intramammarä preparatet och de injektionspreparaten i frågan har bekräftats. Enligt den nya beräkningen, med en normalförbrukning, bedöms totallagret (alla preparat och förpackningar, inkluderande de obligatoriska lagren) för de injektionspreparaten räcka fram till slutet av december 2015 och för det intramammära preparatet fram till början av mars 2016. Lääkealan turvallisuus- ja kehittämiskeskus | Säkerhets- och utvecklingscentret för läkemedelsområdet | Finnish Medicines Agency PL 55, 00034 FIMEA | Puh. 029 522 3341 | [email protected] | www.fimea.fi | Y-tunnus 0921536-6 2 (3) Uppdaterat 6.10.2015 Ytterligare leveranser för de injektionspreparaten i frågan har bekräftats. Enligt den nya beräkningen, med en normalförbrukning, bedöms totallagret (alla preparat och förpackningar, inkluderande de obligatoriska lagren) för de injektionspreparaten räcka fram till mitten av februari 2016. Uppdaterad 11.11.2015 Ytterligare leveranser för det intramammära preparatet i frågan har bekräftats. Enligt den nya beräkningen, med en normalförbrukning, bedöms totallagret för det intramammära preparatet i frågan räcka fram till maj 2016. Uppdaterad 21.1.2016 Med en normalförbrukning, bedöms totallagret för både injektionspreparaten och det intramammära preparatet i frågan räcka fram till maj 2016. Uppdaterad 4.2.2016 Med en normalförbrukning, bedöms totallagret för injektionspreparaten räcka fram till juni 2016 och för det intramammära preparatet i frågan fram till juli 2016. 4. Var har man gjort i Finland för att utreda ärendet? I Finland har ärendet utretts i samarbete mellan Fimea, Evira, representanter för försäljningstillståndsinnehavarna och partiaffärerna för att konsekvenserna av ett eventuellt avbrott skavara så små som möjligt i Finland. Lagermängderna och nya beställningar har följts upp varje vecka och preparatets tillräcklighet har bedömts. Social- och hälsovårdsministeriet har fattat beslut om att underskrida de obligatoriska lagren för läkemedelspreparat som innehåller bensylpenicillin. Om försljningslagren tar slut, övergår man till att använda det obligatoriska lagret, varefter preparat endast får användas för indikationer enligt Eviras rekommendationer under den tid störningen varar. Syftet är att säkerställa att det finns tillräckligt med preparat för de viktigaste användningsändamålen. 5. Vad avses med ett obligatoriskt lager? Syftet med lagstiftningen om obligatorisk lagring är att trygga tillgången på läkemedel och möjligheten att använda läkemedel i situationer där den normala tillgången på läkemedel i vårt land försvårats eller är förhindrad på grund av leveransstörningar, en allvarlig kris eller någon annan motsvarande orsak. Importörer av läkemedelspreparat ska lagra de mängder läkemedelspreparat som lagstiftningen förutsätter. Om obligatorisk lagring och obligatoriskt lager regleras i lagen om obligatorisk lagring av läkemedel (979/2008) och statsrådets förordning om obligatorisk lagring av läkemedel som getts med stöd av den (1114/2008). Som obligatoriskt lager för bensylpenicillin regleras en mängd som motsvarar tre månaders genomsnittliga förbrukning. se http://www.fimea.fi/övervakning/obligatorisk lagring 6. Varför fås inte ytterligare partier av veterinärmedicinska läkemedel som innehåller bensylpenicillin från utlandet? Importörer och försäljningstillståndsinnehavare är ansvariga för importen av läkemedel. De har utrett de partier som är tillgängliga och arbetar för att få in nya partier i landet. Problemet omfattar emellertid överlag tillståndspliktiga veterinärmedicinska läkemedel som innehåller bensylpenicillin i Europa. 7. Vem kan importera läkemedel till Finland? Enligt läkemedelslagen kan läkemedel importeras till landet av bl.a. läkemedelsfabriker, läkemedelspartiaffärer och i vissa specialfall även av apotekare för apotekets egen verksamhet. En veterinär får inte importera läkemedel eller veterinärmedicinska läkemedel annat än i vissa undantagsfall: om en legitimerad veterinär som varaktigt är bosatt i Finland har fört ut läkemedel ur landet för tryggande av läkemedelsbehandlingen av i Finland varaktigt bosatta personer eller djur under deras tillfälliga vistelse utomlands, får han eller hon återinföra 3 (3) de överblivna läkemedelspreparaten.