Kemtentaredigerad - Magnus Lagerberg Homepage
advertisement

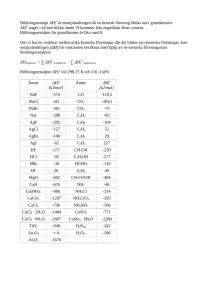
Instuderingshjälp till Allmänkemi 10 p av Magnus Lagerberg Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 1 Termokemi Entalpi =energiinnehållet i ett mol av ett ämne. Entalpi ändring H REAKTION = H PRODUKTER -H REAKTANTER H = cTm =värmekapaciviteten temperaturändringen massan =J/Kg K (ellerC)gram= joule H<0 Exoterm reaktion energi avges till omgivningen H>0 Endoterm reaktion energi upptas från omgivningen Hess lag Entalpiändringen är oberoende av reaktionsvägen H för en reaktion med okänd entalpi kan beräknas med hjälp av kända reaktioner. Multiplicera reaktionerna med ett tal(even negativa, ej nödvändigtvis heltal) så att summaformeln blir den du söker. När en reaktion reverseras, multpliceras med -1 ändrar H tecken. H3 = H2+H1 Ex tenta 25/1-97 fråga 5: H0=-638 kJ för den termiska sönderdelningen av fyra mol ammoniumperklorat enligt: 4NH4CLO4 (s) 2N2(g) + 4HCl(g)+5O2 (1) Men aluminiumpulver reagerar ammoniumperklorat häftigt och större värmemängder frigörs framför allt på grund av reaktionen 4Al(s) +3O2(g) 2Al2O3(s) (2) som har ett H0 = -3352 kJ (per fyra mol Al(s) En sådan reaktionsblandning utnyttjas i första stegets fastbränsleraketer (”boosters”) på USA:s rymdfärjor, och stora gasvolymer produceras på ett nästan explosionsartat sätt enligt följande reaktionsformel: 10Al(s) +6NH4ClO4(s) 5Al2O3(s) +3N2(g) +6HCl(g) +9H20(g) (3) Beräkna H0 för reaktion (3) med hjälp av H0 för reaktion (1) och (2) H H H1=-638kJ H2=-3352kJ H3= ? 4NH4CLO4 (s) 2N2(g) + 4HCl(g)+5O2 4Al(s) +3O2(g) 2Al2O3(s) 10Al(s) +6NH4ClO4(s) 5Al2O3(s) +3N2(g) +6HCl(g) +9H20(g) H11,5=1,5(-638kJ) H22,5=2,5(-3352kJ) H3=H1+H2=-9337kJ Hf0 Bildningsentalpi gäller för föreningar som bildats från rena grundämnen i sina standardtillstånd P=1atm, t=25C,C=1,000M (gaser: t=0C) 0 grundämnen har enligt def Hf =0 HREAKTION=Hf0PRODUKTER - Hf0REAKTANTER Ex uppgift 5b tenta 25/1-97 Beräkna H med hjälp av tabellvärden 10Al(s) +6NH4ClO4(s) 5Al2O3(s) +3N2(g) +6HCl(g) +9H20(g) Hf0PRODUKTER= 5(-1675,7) +30 +6(-92,3) Hf0REAKTANTER= 100 +6(-295,3) HREAKTION= -11108,5-(-1771,8)= -9336,7 +9(-241,8) Tips: kolla laboration nr 9. Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 2 Bindningar Bryta bindningar kräver tillsats av energi Bilda bindningar frigör energi ex exoterma processer förbränning kondensering och stelning galvanisk cell endoterm process H = + exoterm process H = - endoterma processer fotosyntes avdunstning, smältning, kokning Elektrolys entropi är ett mått på oordningen Drivkraften för en reaktion beror av de tre storheterna H S och temperaturen. En reaktion sägs vara spontan om H -TS<0 ex fråga 5 c tenta 25/1-97 Beräkna S0 med hjälp av tabell värden (BD) Observera att S0 för grundämnen enligt tab 5.2 i BD anges per mol atomer. S0=S0PROD-S0REAKT=(550,9+6186,8+9188,7)-6(186,2)=1326,4 fråga 5d: Är tecknet på S0 som du beräknat i ”c)” det man skulle gissat för reaktionen (3), och i så fall varför eller varför inte? Det är troligt att utsprutningen av gas för drivningen av en rymdfärja är en spontan process tecknet på S måste därför vara positivt för om S var negativt skulle processen ej vara spontan dvs H -T(-S)>0 G=H -TS G= negativ medför att processen sker spontant G= positiv medför en icke spontan process. S0 Begränsande reaktant ex 6PCl3 + 6Cl2 +P4O1010POCL3 m 1kg 1kg 1kg ? M 137,5 70,9 283,9 153,32 n 7,28 14,1 3,52 ? Jämför förhållandena teoretiskt och verkligt. (börja med möjliga) 6PCl3/1P4O10=6/1(teoretiskt) 7,28/3,52=2,068 (verkligt) PCL3 i underskott 6PCL3/6Cl2=1 teoretiskt 7,28/14,1=0,52 (verkligt) PCl3 i underskott PCl3är i underskott och bestämmer utbytet. 6PCl3 =10POCl3 PCl3 =10/6 POCl3 xPCl3 = x10/6 POCl3 x=7,28 mol 7,28mol PCl3 ger 7,2810/6 mol POCl3 nM=m 72,8/6 153,32=1,9 kg POCl3 Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 3 Varför är vatten molekylen vinklad? Syret har 6 valenelektroner och vätet var sin = 4 par två av dessa par är bundna till vätet men två par är obundna sk lonepairs och tar plats. - 105 + Joner som hydratiseras omges av vattenmolekyler. Positiva joner =katjoner omges av vattenmolekyler med sin negativa sida vänd mot jonen. Anjon (negativ) omges av vattenmolekyler med sin positiva sida vänd mot jonen Hur många bestäms av laddning och jonens storlek oftast fler än 4. Elektrolyter Joner i vattenlösning bidrar till elektrisk ledningsförmåga. Starka elektrolyter är t.ex lättlösliga salter eller starka syror. Svaga elektrolyter är tex syror som ej protolyseras fullständigt eller svårlösliga salter. Icke elektrolyter är ämnen som då de löses i vatten ej bildar joner, tex sockerlösning. Olika typer av reaktioner i princip kan alla hänföras till dessa tre huvudtyper: fällning syra/bas redox Jonföreningar är olika mycket lösliga i vatten Lättlösliga : ofta nitrater NO-3 alkalimetallsalter Li+, Na+, K+ ammoniumsalter NH4+ brom, klor och jodjoner är lättlösliga sulfatsalter tex H2SO4 svårlösliga sulfider av tungmetaller PbS metaller med höga atomnummer period 6 Tabell 5:3 i BD msat /mol/100g Syntes Framställ ett mer svårlösligt salt av mer lättlösliga, studera löslighetstabell, använd ovanstående lättlösliga salter, (Finns det någon skillnad på fällning och syntes)? ex: Pb(NO3)2 +2KI PbI2 +2K+ +2(NO3-) (framställning av blyjodid) CoCO3 +H2SO4 Co2 +CoSO4(H2O) Syror protongivare baser protontagare Starka syror protolyseras fullständigt, flerprotoniga protolyseras ett steg. Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 4 Titreringar omslagspunkten: antalet mol av titratorn är lika med antalet mol av titranden kraftig stigning på grafen Oxmedel (reduceras själva) oxiderande syror HNO3 H2SO4 jonföreningar där höga oxtal förekommer N kan avge 5 elektroner som mest N+5 nitrater är oxmedel NO3ädla metaller i jonform Ag+ Reduktionsmedel(oxideras själva) alla oädla metaller: Zn, Mg, Na, Al ammoniumjonen NH4+ vill gärna oxideras Öva balansering av redox. PV=NRT Vol för en mol gas vid STP =22,42 dm3 V=1R273,15/101325 ideal gas Densitet för en gas ersätt n med m/M, lös ut m/V=gram/m3 PTOT=P1+P2+P3… Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 5 Bohr modellen gäller egentligen endast för väte och övergavs på 1920talet. Kvantmekaniken utvecklades under 20-talet av Heisenberg, de Broglie och Schrödinger.Elektroner rör sig med ljusets hastighet på en liten yta man kan egentligen säga att den existerar överallt samtidigt. Man kan inte beräkna elektronens läge och hastighet samtidigt. Osäkerhetsrelationen. Vågfunktionen beskriver en eller flera sannolikheter att hitta en elektron i en viss punkt. Orbitaler egentligen banor eller kurvor. Men orbitaler bör istället ses som en våg. 4 kvanttal används för att beskriva orbitaler. 1 huvudkvantalet, n beskriver energi och storlek på orbitalen egentligen avståndet från kärnan. n=1,2,3… (”K”, ”L”, ”M”;..) 2.Bikvanttalet, L(lilla) bskriver orbitalens form L n-1 L=0,1,2,3,… s,p,d,f,g,h… 3.Magnetiska kvanttalet, m beskriver orbitalens riktning -Lm+L ex L=0 m=0 L=1 m=-1, 0, +1 L=2 m=-2,-1, 0, +1, +2 4.Spinnkvanttalet, s beskriverhur elektroner spinner kring en axel, två möjliga håll. S=+½ eller s=-½ Pauliprincipen alla fyra kvanttalen får ej vara lika Perioden i periodiska systemet=huvudkvanttalet n den upphöjda siffran anger hur många elektroner i deta skal eller i denna stående våg. Upp eller ned pil anger olika spinntal Elektronkonfigurationer beskrivs ofta med [ädelgasskal av ett ämne] + orbital t.ex Li 3 elektroner[He] 2s1 (heliumskal med en elektron i 2s orbitalen) K 19 elektroner[Ar]4s1 1s2 2s2 2p6 3s2 3p6 4s1 F 9 elektroner[He]2s2, 2p5 (argonskal med en elektron i 4s orbitalen) (heliumskal med 2 i sorbitalen och 5 i p orbitalen joner kan betraktas på liknande sätt ex Li+ [He] skal Elektronegativitet Förmåga att attrahera gemensamma elektroner i en bindning och dra dem närmare sig. sid 49 BD FONCLBRISCH Ju större skillnad i elektronegativitet typiska jonbindningar lägre skillnad i elektronegativitet = kovalenta bindningar , typiska molekylföreningar (elektronparbildning) Bästa metoden: skriv ut i grundämnesform, kolla sid 49 BD tex CaO syre har3,5 och kalcium 1,0 skillnad = 2,5 enligt BD har 79 % är föreningar med denna skillnad i elektronegativitet jonbindningar Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 6 Joniseringsenergi= den energi som krävs för att avlägsna en elektron från ett ämne Ökar med jonstyrkan Kärnan är positivt laddad och håller hårdare i andra elektronen än den första AlAl+ +eI1=580kJ/mol BD sid 44 Al+Al2++eI2=1815kJ/mol Positiva joner är mindre än den atom de bildats ifrån ju högre positiv laddning desto mindre jon. Negativa joner blir större än den atom de bildats ifrån. Negativ energi dvs energi frigörs då en negativ jon bildas. Storleken på atomer i per sys. Minskar åt höger i en period men ökar nedåt i grupp. En tunn stråle böjs av ett laddat föremål. Kovalenta föreningar ett eller flera elektronpar gemensamt. Dipoler två eller flera atomer med olika elektronegativitet olika laddningar i VL och HL. Tex vatten eller HF. Kolkedjor blir mindre polära ju längre kolkedjor Lewisstruktur Strukturer av molekyler med alla valenselektroner utsatta. 1. räkna ihop alla valens elektroner NO3- =5+36+1=24 st 2. 2.Två elektroner bildar en kovalent bindning eller ett fritt elektronpar. =12 par .. :O: förslag | N :O: :O: ¨ ¨ 3.Kan någon atom få ädelgasskal stämmer för ett syre förslag :O: || N :O: :O: 4. Resonans ofta fördelaktig elektronerna fördelas över flera atomer. Dubbelbindningen finns på alla tre syreatomerna samtidigt. Är likvärdiga Obs innebär ej att elektronpar skuttar runt. Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 7 Obs oktettregeln gäller endast t.om. 2:a perioden tex ej för svavel som får utökad oktett F F \ / F --- S -- F / \ F F S (ej dipol negativ åt alla håll) oktaeder 0,5-2Å (1Å=10-10m) Hur långa blir bindningarna? Där energin blir lägst bestämmer längden på bindningarna. Allting strävar efter lägsta energiinnehåll. Idealt läge Om de kommer närmare uppstår repulsion. Jonstorlek ungefär som atomer, positiva joner blir mindre Negativa joner blir större. Elektronegativitet förmåga att dra till sig elektroner. Vänstra delen av per syst. Otroligt låga mått på elektronegativitet bildar lätt positiva joner. När uppstår en jonförening eller kovalent bindning? Stor skillnad i elektronegativitet jonförening Bra metod förutom tabeller: man smälter föreningen och kontrollerar elektrisk ledningsförmåga. Den förening som leder ström i smälta är en jonförening. Ibland är det en kovalent bindning och leder ej ström. Atomstorlek Lattice= gitterenergi när ett ämne går från gasform till fast form frigörs väldigt mycket elektroner. Joner med höga laddningar ger större gitter energi (BD sid 115) Gitterenergi är den energi då joneri gasfas bildar ett salt. Större negativt värde fås om jonerna har hög laddning. Dipoler uppstår då elektronegativitet förskjuter laddningarna i en viss riktning. H Lewis struktur för Ammoniak NH3 | Valenser 5+31=8 4 par N Förslag i allmänhet mest elektronegativt i mitten. / \ H H oktett för N , ett lone pair repulsion ” N / | \ H H H XeF4 lonepair tetraederstruktur om man räknar lonepair egentligen trigonal prisma dipol 8+47=36 18par F \ / ¨ Xe ¨ plan kvadrat ej dipol / \ F F F Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 8 O3 36=18 9 par två kan få oktett .. O .. O resonans // \ : O : : O: .. ej dipol 120graders vinkel(360/3=120) / \\ :O: :O: .. Jämvikt Kemisk jämvikt är dynamisk vid jämvikt är hastigheterna mellan VL och HL lika stora v1 Br2 (l) Br2(g) v1=v2 v2 Efter ett tag uppstår en jämvikt så att antalet Br2(l) är konstantsamt Br2(g) är konstant. Tiden att uppnå jämvikt varierar starkt, vissa systems tid att uppnå jämvikt är ej kända. [A]2 [B] K=---------[A2B] uttrycket bestämmer enhet men oftast enhetslös. A2B 2A +B Upplösning av ett salt i vatten (gäller ideala fall) AgCl(s) Ag+ +Cl[Ag+] [Cl-] Ksp=---------------------(BD sid 120) [AgCl]=1 (rent ämne) Svag syra HF(aq) H+ +F[H+] [F-] KA --------------[HF] (BD sid 122) svag bas på samma sätt. Starka syror fullständig protolys [H+] [SO42-] KA---------------- = 0 (PSO3)2 KP =gasjämvikt----------------(PSO2)2 (PO2) BD sid 124 Komplexjämvikter K1 och K2 Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 9 Allmänt om jämvikter Om man lägger till något på vänster sida förskjuts jämvikten åt andra hållet mot höger. Naturen strävar efter att motverka små förändringar så att jämvikt skall råda. Chateliers princip. Reversibel går att vända fram och tillbaka Irreversibel går ej att vända tillbaka. Ex A +B C + D Om D tas bort från systemet förskjuts jämvikt åt höger. Extra B förskjuter jämvikten åt höger. A tas bort förskjuts åt vänster. Uttrycket strävar mot konstanten. Ändringar motverkas. Tex om temp ökar i en exoterm reaktion förskjuts jämvikten åt vänster. Trycket ändras påverkar ej om lika många gasmolekyler i VL som i HL. Om olika antal gasmolekyler så påverkar trycket. Om K är stor favoriseras HL 13.61 Bra övning Slutsatser efter genom gången tenta(13/6 -97) Vid balansering kolla om uttrycket går att förkorta. Åskådarjoner behöver man inte ta med i balanseringar. Synteser: målet är att få fram en ren produkt eventuella rester måste avgå, enklast om det är en gas. Molmassa för föreningar står i BD M/g mol-1. Tidsbesparande! Molmassan för hela produkten tas med även om tertahydrat (4H2O) Löslighetsprodukt Ksp anger hur många joner som bildas. Löslighet anger hur mycket av ett ämne som kan lösas. Ex: CaCO3(s) Ca2+ (aq) + CO32-(aq) KSP= [Ca2+][CO32-]=5,010-9 Lösligheten av Calcit CaCO3: Vid lösning av calcit bildas xx joner=510-9 x2=510-9 Hur mycket calcit har då lösts ? x=510-9 =710-5 dvs ur 710-5 mol calcit bildas (710-5 710-5) mol joner dvs (710-5)2=510-9 jmf lösligheten med tabellvärdet för resp ämne och kolla potensen i BD står 1,3010-5 att jämföras med 710-5 Om vattnet surgörs kommer 2H+ att tillsammans med CO32- bilda kolsyra H2CO32-. Kolsyran avgår som gas och för att bibehålla jämviktsuttrycket förskjuts jämvikten åt höger. Konstanter ändras ej! (men endast vid STP!) Ksp är en konstant. PH-pC diagram pka värden där titreringskurvan är flackast. I diagrammet där syra och bas skär varandra. Lämpligast ekvivalens punkt är det tydligaste språnget på titrerkurvan. Oftast den andra för en tvåprotonig syra. Syrans molmassa ur titetringskurvan ex H2A +2OH- A2- +2H2O Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 10 molförhållande syra bas =1:2 (hälften så många mol i syran som i basen) basens volym och koncentration är kända syrans massa är känd CV=n Syrans n =nBas/2 Om 0,002 mol bas är ekvivalent med nBAS/2 syrans mol = 0,001 n=m/M M=m/n M =1,2345/0,001=1234,5 M För att kunna skissa ett pH-pC diagram krävs pka värden samt pC TOT pCtot= -lgkoncentrationen C=n/v=0,001/0,1=0,1 -lg0,1=2 1 2 3 4 5 6 7 8 9 10 11 12 13 14 1 2 3 4 5 6 7 8 9 10 11 12 13 14 pka Obs enprotonig pka3,5 pHe=7,8 pCTOT=2 start 2,5 pHe pH - 7,5 pHe 3,5 pka + OH H Vol(OH-) tvåprotonig pka1=4 och pka2=7 pka1 pCtot =2 pka2 pHe1 pHe2 pCtot =2 start kurvan ändrar lutning varje gång den stöter på pka-värden. Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 11 Galvanisk cell den mest oädla oxideras och bildar minuspol medan den ädlare eller med högst E0 reduceras vid pluspolen. E0CELL =E0+-E0- (alltid positivt) ECELL=E0 - (RT/nF)lnQ Q=[Prod]/[Reakt] Vid jämvikt är Ecell=0 och då har alla joner vid +polen förbrukats Dvs [ox]=[ox]+ [red] Bindningar Att bryta bindningar kostar mer energi än att bilda. Om reaktionen är endoterm har det kostat mer att bryta än att binda energimässigt. Om reaktionen är exoterm har bindningarna(prod) avgivit mer energi än vad det kostade att bryta(reakt) Går att räkna på. Hupplösning=H produkter - H reaktanter H egentligen Hf0 här. H för joner sid 112 BD H för föreningar tabell 5:3 BD Hupplösning= negativ =exoterm Hupplösning=positiv=endoterm G=H-TS G=negativ=spontan Om en reaktion är spontan vilket tecken måste då S ha om reaktionen är exoterm resp endoterm? Exoterm H=negativ S=positiv oordningen ökar för ett visst värde på T (entropistyrd) Endoterm H=positiv S=positiv men mer styrd av entalpin. Kinetik v=k [FTF]n[OH-]m initialhastighetsmetoden: man mäter hastigheter i början av reaktionen visuellt eller med hjälp av spektrofotometri. 1. Variera koncentrationen av [FTF] medan [OH-] hålls konstant v=k1[FTF]n om 1 M FTF ger hastigheten v och 2M ger hastigheten 4v blir exponenten n =2 2. Variera koncentrationen av OH- på samma sätt. V=k2’[OH-] ger exponenten m hastighetskonstanten k bestämmer totalreaktionens hastighet. Beror bla av T k=Ae-EA/RT Arrheniusekvationen. Jämvikt med gaser Om lika många gasmolekyler i VL som Hl påverkar inte trycket ex H2O(g)+ C(s) H2(g) + CO(g) [H2] [CO] k=----------------[H2O(g)] C(s) [H2] [CO] =----------------[H2O]1 Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg H2O i gasfas ej rent ämne!!! 12 Anta att trycket fördubblas PH2 PCO KP1=---------------PH2O 2PH2 2PCO KP2=----------------= 2Q jämvikten driv åt vänster. 2PH2O G= positiv =spontan Krävs mycket energi för att bryta C(s) bindningar fler bindningar bryts i Vl än som bildas i HL. Reaktionen måste vara endoterm H = positiv = endoterm Gaser bildas i HL större oordning S måste vara positiv. Om T ökar så minskar G (blir mer negativt) Vid en viss Temp blir H och S lika stora, över den temp då G<0 är alltså reaktionen spontan. Drivkrafter för reaktionen är entalpi, entropi och Temp. Forts. föreläsningsanteckningar. Lewis struktur för I3Antal valenselektroner= 37+1=22 11 par _ _ 1:a förslaget | _I - I - I_| 3 lonepair de stör så lite som möjligt om de ligger i ett annat plan än atomerna. 120 grader (oktett regeln gäller endast till 2:a perioden) ett känt jämviktsuttryck kan användas för att räkna ut ett okänt ex: 2SO2 +O2 2SO3 K=278 SO2 +½O2 SO3 K=? K1=[SO3]2 / ( [SO2]2 [O2] ) K2=[SO3]1 / ( [SO2]1 [O2]½ ) K2=K1 =27816,67 2SO32SO2 +O2 K3=? K3= invertering av K1=1/2783610-4 Q gäller vid icke jämvikt och räknas ut på samma sätt som K. Om Q < K råder ej jämvikt reaktionen fortsätter åt höger. Om Q > K råder ej jämvikt reaktionen går till vänster. Om Q = K råder jämvikt. Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 13 Syra - bas begrepp Syra är protongivare och bas är protontagare. PH definieras som -(10)lg [H+] pH=-lg[H+] ex pH i 0,20 M HCL pH=-lg[0,20]=0,70 Vattnets autoprotolys vatten kan fungera både som syra och bas amfolyt, amfotär. H2O (l)+ H2O (l) H3O+ +OH[H3O+] [OH-] [H3O+] [OH-] jämvikt i vatten = -------------------=-------------------------= 1,010-14 [H2O] [H2O] 1 Vad är pH i vatten vid jämvikt? Behöver H+ koncentrationen. [H3O+] [OH-]= xx=10-14 x= 10-14 [H+]=10-7 pH=-lg [10-7] pH =7 pH i basisk lösning 2,0 M NaOH (stark bas och syror protolyseras fullständigt) Om 2,0 M NaOH 2 M OH(NaOH (s) +H2O Na+ (aq)+OH-(aq) +H2O) KW=10-14=[OH-][H3O+] Om [OH-]=2 [H3O+]= 110-14/2=0,510-14 pH=-lg[0,510-14]=14,30 pOH +pH=14 Om pH = 4 vad är [H+] 4=-lg[x] 10-4=10-(-lgx) x=10-4 Syra konstanten Ka syra HSO4H3PO4 H2PO4HPO42KaKb= 1,010-14 Ka 1,010-2 7,910-3 6,210-8 4,410-13 pKa 2,00 2,1 7,2 12,4 bas SO42H2PO4HPO42PO43- Kb 1,010-12 1,2710-12 1,610-7 22,710-3 pKb 12,00 11,89 14-7,2=6,8 14-12,4=1,6 Kb=(10-14)/Ka pKa+pKb=14 ex pka= 7,2 vad är Kb? pkb=14-7,2=6,8 kb =10-6,81,610-7 Kan utläsas ur pH-pC diagram Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 14 syrans koncentration (initialt) =pCtot ex pCtot=1,46 10-1,46=0,035 Lösningens sammansättning vid ett visst pH Dra en linje för ett visst pH [x] 10-DET Y-VÄRDE SOM STÅR TILL VÄNSTER pka värden pHe värden Hur man ritar ett pH-pC diagram. Pka värden samt [syra] krävs. Rutat papper 1-14 y och x axeln. -lg [syra]=pCTOT En vågrät linje dras vid detta värde. PKa värden markeras på pH axeln. Två diagonala linjer för OH- och H3O+ drages. Hac och Ac- linjer dras utgår från pka och är parallella med de diagonala linjerna. Startpunkten för titrering vid jämvikt mellan H3O+ Acjämviktspunkten pHe där Hac OH- Titreringskurvor Avläs ekvivalenspunkten där den är som tydligast(oftast andra vid tvåprotoniga syror). Pka kallas också halvtitrerpunkten. =Ve/2 där titreringskurvan är som flackast. Buffertverkan är som störst vid pka och minst vid ekvivalenspunkten. Dissociationsgrad anger hur stor procent av syran som protolyseras. Ex dissociationsgraden för en syra är 3 %. Koncentrationen för syran är 0,15 M. Vad blir Ka? HA H+ +A[HA]3%=A- =H+ [O,15]0,03=4,510-3 Ka= ([H+][A-]) / [HA]= (4,510-3 4,510-3) / (0,15-4,510-3) = 1,410-4 Dissociationsgraden kan även räknas ut från startvärdet i pH-pC diagrammet. Ex 0,50M svag syra har start värdet pH 2,5 och pC 2,5 [A-]=10-2,5 [A-] / [HA]= dissociationsgraden=10-2,5/0,50=0,006 =0,6% Bas i pH-pC diagram NH3+H2O NH4+ +OH0,150M NH3 KB = 1,810-5 pKb=4,8 pC tot =-lg 0,150= 0,82 Ka Kb =Kw Ka= Kw / Kb =10-14/1,810-5 =5,5610-10 pKa=-lg 5,5610-10 =9,26 eller pKa+pKb=pKw pKa=14-4,8=9,2 Vad är [OH-] vid titreringens början Rita pH-pC diagram och markera pC-tot samt pka. Korresponderande syra till vänster. Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 15 pKa pCTOT pHSTART =11,25 pHe pH+pOH=14 pOH=14-11,25= 2,75 [OH-]=10-2,75=1,7810-3 vid ekvivalenspunkten? pHe=5 pOH=9 [OH-]ekv=10-9 Där Ha och A skär varandra är de lika stora. [Ha]=[A-] =½ CTOT just i krökningen av kurvorna. Ex 0,035M syra pCtot=1,46 -lg½CTOT=0,30+pCtot =1,76 10-1,76 =0,0175 =0,035/2 Buffertlösning Buffertlösning innehåller en svag syra och dess korresponderande bas. (eller vice verca) Denna lösning ändrar ej pH så lätt. En bra buffert uppstår då pH = pKa samt jämvikt mellan syra och korresponderande bas. PH=pKa + lg[bas]/[syra] Om bas/syra =1 lg 1=0 ex 0,10M Hac och 0,25 M NaAc pH = 4,8 + lg 0,25/0,10 Ättiksyra / natriumacetat pH=5,14 Ex 3:e 25/1(tenta) Hur mångs cm3 av titratorlösningen behöver man tillsätta för att få en buffert med pH 8,5? Närmaste pKa = 9,3 syrans koncentration =0,1 M Syra bas par är NH4+ (syra) och NH3 (bas) Titratorlösning är NaOH 1M pH=pka+lg[bas]/[syra] 8,5=9,3 +lg x 8,5-9,3=lg x 10-0,8=x x=0,158 Förhållandet mellan syra och bas skall vara 0,158 [NH4+] +[NH3]=0,1 0,1-y +y=0,1 y/(0,1-y)=0,158 y=(0,1-y)0,158 y=0,0158-0,158y 1,158y=0,015 y=0,0136 När är koncentrationen av NH3 0,0136? (NaOH 1M) CV= n 0,01360,2=0,00272 mol Vol OH- = 1:a ekvpunkten +0,00272 mol 1:a ekv punkten =20cm3 CNAOHV=0,00272 V=0,00272/1 0,003 VOH= 20cm3 +3cm3=23cm3 Salter som löses i vatten. Lösningen blir sur :NH4NO3 Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 16 neutral NaCL, KNO3 basisk NaAc Natriumacetat, Na neutralt Ac är en bas Katjoner(positiva joner) i grupp 1 och 2 blir neutrala(pH) grupp 3 sura tex aluminium Många katjoner är starkt sura (metalljoner) pH i kalkvatten Ca(OH)2? Ca(OH)2 (s) Ca2+ +2OH1-x KSP x 2x = x (2x)2 = 1,310-6 4x3=1,310-6 x=((1,310-6)/4)1/3 2x=[OH]=26,8710-3 [H+] =10-14 / (26,8710-3) =0,7310-12 pH = -lg(0,7310-12)=12,1 x=6,8710-3 Oxider kan också vara basiska neutrala eller sura. Ex MgO +H2O Mg2+ +2OHJu högre laddning på katjonen desto surare. Neutral är de som förekommer naturligt som mineraler tex tennoxid, Feoxid etc. Kap 16 Termodynamik H värmeförändring H= negativ exoterm H=positiv endoterm Energin kan inte förstöras men omvandlas Hess Lag: energiförändringen är oberoende av vägen. Höga energinivåer är instabila. Det krävs ofta aktiveringsenergi (Ea) för att sätta igång kemiska reaktioner. I termodynamiken studeras energier för olika tillstånd, men vi vet inte så mycket om intermediära faser( kinetik) eller hur fort reaktionen sker. Spontan reaktion, sker av sig själv utan yttre påverkan efter igångsättning , Ea. Alla spontana reaktioner är inte exoterma. Vissa endoterma processer sker spontant t.ex lös salmiak i vatten. Det blir kallt alltså har saltet tagit upp värme(endoterm reaktion) Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 17 Entropi S Termodynamisk funktion som beskriver antal möjliga arrangemang ett system kan anta. Om möjligheterna är många så blir sannolikheten att detta skall inträffa hög. Entropin är ett mått på oordningen. Hög oordning = hög entropi. S fast ämne< S vätska<< S gas. Totalt sett i universum ökar entropin. Andra huvudsatsen: Totala entropin ökar i universum. I alla spontana processer ökar STOT. SUNIVERSUM=Ssystem +SOMGIVNINGEN S har enheten J/molK. Tecknet för S bestäms av riktningen. Om SOMGIVNINGEN> 0 då har en exoterm reaktion skett., värme har avgetts. Riktningen på S talar om ifall exoterm eller endoterm reaktion har skett. Storleken på S beror av Temperaturen SOMGIVNINGEN= -HSYSTEMET/T (reaktionens temp vid jämvikt) Gibbs fria energi G= H - TSsystem S + (mer oordning) H - (exoterm) + + (endoterm) -(mindre oordning) - (exoterm) - + (endoterm) Spontanitet spontan vid alla temperaturer explosivt Spontan vid hög temp tex salt i vatten (endoterm) oordningen ökar spontan vid låga temperaturer t.ex vatten fryser till is. ej spontan vid någon temperatur t.ex elektrolys En reaktion är spontan om energiinnehållet är lägre för produkten. Om oordningen blir stor så ökar sannolikheten för en reaktion. S= SPRODUKTER - SREAKTANTER SUNIVERSUM= SSYSTEM + SOMGIVNING (Somgivning anger värmeflödet exo eller endo term) SUNIVERSUM= SSYSTEM - HSYSTEM/T multiplicera bägge led med T TSUNIV = TSSYST -HSYST muliplicera med -1 -TSUNIV= H-TSSYST T = Kelvin , alltid positiv -TSUNIV=G G=H-TSSYST Om -TSUNIV är< 0 G< 0 för spontana processer. T.ex när nitroglycerin exploderar, massor av gaspartiklar bildas. Hög Temp , exoterm ökad oordning H(-) -T(stort tal) S(+)= - -(+)= -- =G= -=spontan process. 1:a huvudsatsen 2:a 3:e Totala energin i universum är konstant För alla spontana processer så ökar den totala entropin i universum SUNIV >0 En perfekt kristall har entropin = 0 vid 0Kelvin G kan ej mätas direkt men kan beräknas från H och S värden. Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 18 Ex H =25 kJ, S=5,0 J/Kmol, T = 300 K G= 25103 -300(5,0)=25000-1500=23500 positiv = ej spontan reaktion. Enl Hess Lag kan reaktioner vändas: S + 3/2O2SO3 2SO2 +O22SO3 G =-371 G = -142 S +O2 G = ? Vänd på (2) och dividera med 2 Använd G0f ( ex G=-371 -½(-142) = 300 kJ/mol spontan. NTP formation = bildning) CH4 -75 186 -51 H0f S0f G0f (1) (2) 2O2 20 2205 20 H0f =prod-reakt =-393 + 2(-242) - (-75 )+(-0) S0f =prod- reakt =214 + 2189 -(186+2205) G0f = prod-reakt= 2(-229)+(-394) -(-51-0) CO2 -393,5 214 -394 2H2O 2 -242 2189 2-229 =-803kJ (exoterm) =-4J/mol (oordnigen minskar = -801 kJ/mol Beräkning av G från jämviktskonstanten K G= G0 +RTlnK G0 är inte samma sak som G0f G < 0 G = 0 G > 0 spontan jämvikt icke spontan reaktionen sker åt andra hållet. Ex H2O H+ +OHanta att jämvikt råder KW = 1,00 10-14 0=G0 +RTlnK G=0 G0=-RTlnK = -8,3145 298,15 ln 1,0010-14 =79,0 kJ/mol icke spontan process reaktionen sker åt andra hållet. Kap 9 VSEPR-metoden Valence Elektron Repulsion Shell Pair Lewis strukturer: bindningen skall vara så långt från varandra som möjligt 4 bindningar-tetraeder orbitaler: gäller främst obundna atomer Molekylstrukturer: hybrider Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 19 Orbitalerna förändras: Enskilda atomer har ej sama form som de som är bundna till andra De nya orbitalerna kallas hybridorbitaler. Processen kalls hybridisering. Antalet effektiva elektronpar 2 3 4 5 geometrisk form hybridisering linjär sp trigonal sp2 tetraeder sp3 trigonal bipyramid dsp3 6 oktaeder d2sp3 Detta kapitel borde man nog läsa lite noggrannare. Men s-orbitaler är tydligen mer eller mindre sfäriska medan p-orbitaler ser ut som 8:or i ett tredimensionellt koordinatsystem p och s orbitaler kan kombineras och bildar då sp hybridider I3- bildas då jod löses i vatten linjär molekylform 37+1=22 elektroner = 11 par ej period 2 oktettregeln gäller ej. _ \/ _ |I - I - I| | Kvävgas |N= N| Betrakta atomen i mitten den har 5 elektronpar = dsp3 De yttre atomerna har 4 elektronpar =sp3 Varje atom har 4 par = sp3 Molekylorbitalmodellen Molekylorbital 1 = MO1 addition av två s-orbitaler MO1=1sA +1sB ex vätgas --------- x H1SA --------- H1sB Energinivå Bindande, molikylorbitaler ligger alltid lägre i energinivå än de antibindande samt ligger lägre än de antibindande som fanns från början. MO1 ligger mitt emellan A och B som har lägre energi sk bindande molekyl A=B MO2 ligger på utsidan av atomerna A och B och har högre energitillstånd, kallas antibindande molekyl ex H2- har 3 elektroner. H ---------x (antibindande) H --------- Bindningstal = Bond order (antal bindande - antal antibindande)/2 H2=(2-0)/2=1 H2- =(2-1)/2=½ Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 20 Ju lägre bindningstal desto svagare bindning ex syre O2 2 s och 4 p på varje atom --- --- 2p (4) 2p(4) --- --- 2s(2) 2s(2st) O2 är paranegativt oparade antibindande elektroner finns, dessa kommer att förstärka ett magnetfält. Vad finns det för bindningar mellan molekyler? Sk intermolekylära molekyler. De svagaste är Vander Vaal och beror på tillfälliga dipolmoment. Tex mellan 12 och I2 V.d.V bindningar ökar med ökande molekylstorlek. Tex halogenerna. Svaga bindningar mellan molekyler beror på tillfälliga dipoler som uppstår då elektroner rör sig. Inom halogenmolekylerna är det kovalenta bindningar (elektronparbindningar) Mellan molekyler i bensin V. d. V. Opolärt. Blir starkar ju större molekyl. Lika löser lika: lika starka Van der Vaal bindningar, samt lika polaritet. V.d.V: alla gaser eller vätskor med låg smält och kokpunkt. H Något starkare än V. D. V är dipol-dipol bindning. / H--------O Vätebindningar FONClBRISCH / O \ H \ Gäller endast F, O, N, bindningar till väte. H Väte bindningar har högre kokpunkt än vanliga dipol-dipoler. Ex H2O kokar vid 100 grader medan H2S kokar vid - 60 grader. Jonbindningar tex NaCL laddningarna är den sammanhållande kraften. Starkast elektrostatiska krafter. Jonföreningar ligger långt ifrån varandra i per. Sys. Och leder ström i smält form. Metallernas valenselektroner är jämt fördelade över alla atomer sk delokaliserade. Värmeledningsförmåga påverkas av hur pass lättrörliga de delokaliserade elektronerna är. Kristallstruktur CCP cubic close packing HCPHexagonal close packing Diamant delokaliserade elektroner samt starka bindningar åt alla håll grafit ”” sexhörniga ringar starka bindningar inom skikten men svagare mellan skikten. Ångtryck Runt om ”ovanför” varje fast eller flytande ämne finns en viss mängd gas, som har ett visst tryck sk ångtryck. Ju mer lättflyktigt desto högre ångtryck. 0 för NaCl men mkt högt för bensin. I2 och CO2 har icke försumbara ångtryck och sublimerar lätt( övergår från fast fas till gas form utan mellan liggande flytande fas). Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 21 Ångbildningsentalpi HVAP= Den värme som krävs för att bryta bindningar i en vätska (eller fast ämne) och bilda ånga(gas). T ex vatten som avdunstar och ytan(tex kinden) blir kall. HVAP för vatten=41kJ/mol T gas vatten och gas vätebindningar bryts 100 vatten is och vatten i flytande form (is struktur bryts) 0 is tid Lösningsprocessen 1. Bryta bindningar i ämnet som skall lösas, kräver energi 2. Bryta bindningar i lösningsmedel, kräver enrgi 3. Nybilda bindningar mellan det lösta ämnet och lösningsmedlet frigör energi Kan endast ske då H3 < (H1+H2) H1 =+ (endoterm) H2 =+ (endoterm) H3 =- (exoterm) Molaritet = n/V=C Molalitet= n/ kgLÖSNINGSMEDEL=mol/kg Mass% = massan av löst ämne/ massan av lösningen Molbråk= mol ämne/tot antal mol=ksi= ex 50,0 g CsCL löses i 50,0g H2O totVol blev 63,3 ml Mass% =50,0/(50+50)= 0,50 50% Molaritet=(50/(132,34+34,35))/0,063 4,70 mol/dm3 Molalitet=(50/(132,34+34,35))/0,050 5,94 mol/kg Molbråk= nvatten/ ntot (50/18) / (50/(132,9+32,45)+50/18) 0,0966 Ångtryck Ett visst mängd av ett fast ämne befinner sig i gasfas. Ett löst ämne med lågt ångtryck (NaCL) i vatten Raoults lag: Plösning= lösningsmedelP0Lösningsmedel T =KB m kokpunktsändring= kokpunktlösningsmedel molalitet NaCl + is sänker ångtrycket vilket leder till att fryspunkten sänks och kokpunkten höjs Ex socker 4,9 g och 175 g vatten. Påverkas kokpunkten? Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 22 4,9 g socker = 0,01431 mol socker Molalitet = mol/kglösningsmedel=0,01431/0,175 =0,08180 Kb= Molal boilingpoint elevation constants (finns inte i BD!!) för vatten enl Zumdahl = 0,51 T=0,510,08180=0,0417 Den nya kokpunkten blir 100,042 grader C Van´t Hof faktorn i= antal mol i en lösning/ antal mol salt som skall lösas. NaCL Na+ +Cli=(1+1)/1 =2 teoretiskt värde ofta lägre i verkligheten. Eftersom tillfälliga jonparningar bildas. Osmos små partiklar kan vandra men inte större tec vatten molekyler kan vandra men inte proteiner. Det osmotiska trycke beror av koncentrationsskillnader och strävan att utjämna koncentrationsskillnader. Kinetik Läran om reaktionshastigheter och reaktionsmekanismer Reaktionshastighet = koncentrationsändring /tidsenhet=C/t=mol / Litersek. Initialmetoden Det ena ämnets koncentration varieras medan det andra hålls konstant. Och tiden för koncändringen studeras. Det andra ämnet studeras på samma sätt. Man kan därefter bestämma hur betydelse fullt ett ämne är för reaktionshastigheten. V=k [A]0,1,2… index betecknar 0:e, 1:a, 2:a ordningen etc behöver ej vara heltal. K är en konstant med enheten 1/s=s-1 Hastigheten för hela reaktionen v= k[A]x [B]y Reaktionsmekanismer beskriver de steg som inträffar då en reaktion sker. Framgår ej av formeln. Aktiveringsenergi trösker´lenergi som krävs för att reaktionen skall komma igång. Arrheniusekvationen k=Ae-Ea/RT k=hastighetskonstanten, A= frekvensfaktor, Ea= aktiveringsenergi R=8,3145 T=Kelvin ex temp ändras från 275 till 300 kelvin och k ändras 7x Vad blir aktiveringsenergin? 1k=Ae-Ea/R275 7k=Ae-Ea/R300 A är konstant logga med ln och lös ut A. A=lnk/ (-Ea/R275)=ln(7k)/ (Ea/R300) ?? Vad påverkar en reaktions hastighet? 1. Antal kollisioner(temp, tryck). 2. Ofördelaktiga kollisioner? Kanske bara kan ske i en viss vinkel. 3. Steriska effekter (passar bara på ett sätt) 4. Katalysatorer/inhibitatorer Katalysatorer påskyndar reaktioner utan att själv förbrukas, aktiveringsenergin sänks. Homogen katalys katalysatorn i samma fas som det katalyserade ämnet. Heterogen katalys katalysatorn i annan fas än det katalyserade ämnet. Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 23 Kap 17 Elektrokemi Elektrolys: oxidation sker vid anoden(pluspolen) KARO Katod Anod Red Ox Galvaniskt element oxidation sker vid (minuspol) metall oxideras och löses upp vid - polen detta är negativt metallreduceras och faller ut i ren form vid + polen detta är positivt Oxidation ökning av oxtal avger elektroner Reduktion minskning av oxtal tarupp elektroner Galvanisk cell E0=E0+-E0- Den ädlaste matallen kommer att reduceras och den oädlare oxideras. Normalpotential, den med högst E0 värde kommer att reagera åt rätt håll och reduceras vid + pol medan den med lägre E0 värde kommer att reagera åt andra hållet jämfört de reduktioner som står i Normalpotentialtabeller, dvs oxideras vid -polen. Skall alltid bli ett positivt värde annars blir det fel. Normalpotentialer ändras ej vid muliplikation eller vändning Stor skillnad i normalpotential ger en kraftig reaktion. Line of notation -| Mn2+ MnO4-|| IO4- IO3-| + elektrodmaterial, saltbrygga, anod reaktion, katod reaktion E0 gäller vid 1 molar STP ström esaltbro elektrolyt Zn Zn2+ Cu Cu2+ minus pol + pluspol oxidation reduktion Skriv cellschema ex ex Zn , Ag -Zn|Zn2+ || Ag+|Ag+ Halv reaktioner red (Ag++e- Ag)2 + E0= 0,80 2+ ox Zn Zn +2e - E0=-0,76 + 2+ cellreaktion 2Ag +Zn 2Ag +Zn E0=0,80-(-0,76)=1,56 Ecell=E0 -(RT/nF)ln Q Q=[Ag]2[Zn2+]/[Ag+]2[Zn]=(120,1)/(0,121)=10 Ecell=1,56-(8,314294,15)/(296485)ln10= 1,531V Samband mellan G och E0 G=-nFE0 n=antal mol e-, F= 96485 gäller vid ej STP Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 24 Om E0 är positivt blir G<0 spontan process Hur ändras E om vi ej har standard tillstånd E=E0 -(RT/nF)lnQ Nernst´s ekvation Bd variant av nernst´s formel gäller endast för halvcell E=E0 +RT/nF ln[ox]/[red] Elektrolys Genom elektrisk energi kan en icke spontan reaktion ske. Uppladdning av batteri, rening av metaller. Hur mycket bildas: It=nF I=ström (ampere), t=sek, n= mol elektroner, F = Faraday Korrosion Inte bara rost utan all slags oönskad förstörelse av material. Korrosion går fortare och är beroende av O2, ytan, spänningar, korngränser, salt dvs elektrolyter, fukt luftföroreningar. Olika O2 koncentrationer ger uphov till potentialskillnad metall i kontakt med annan metall den oädlare oxiderar. Offeranod(Mg eller Zn) eller galvanisering hindrar korrosion Korrosionsskydd: målning, förzinkning, passivisering(tunt aluminiumskikt som tillåts oxidera, offeranod, legeringar tex rostfritt stål. Hur vet man hur stora atomer och joner är och vilka avstånd det är i strukturer? Diffraktionsexperiment. Bombarderar ett prov med strålning Röntgen neutronstrålning elektroner(elektronmikroskop) Om provet är kristallint (välordnat, tydlig struktur) (amorf= stelnad vätska tex glas.) så bryts difrakteras strålningen i vissa punkter som kalls reflexer Braggs lag: n=2dsin d=avståndet mellan atomplan, =infallande vinkel Kristallin form är teoretiskt i verkligheten oftast en blandning mellan kristallint och amorf. BOD Biochemical oxygen demand är ett mått på hur mycket lättnedbrytbart kol som finns i vatten BOD5(dagar)< 1mg/l rent Bod5 < 5 mg/l förorenat Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 25 Avloppsrening: a grovfiltrering av större föremål b. Sedimentering c. Tillsatser kan öka sedimenteringen FeSO414H2O hydroxidbildning 2. Minska BOD a. Sandbädd mättad med mikroorganismer b. syrefri miljö 3. Görs ej på alla reningsverk Fällning av fosfatjoner med släckt kalk Ca(OH)2 Ca3(PO4)2 oljefilm på vattnet. Sprids ut på mark mättad med välgödda mikroorganismer. Kväverening NO2- och NO3- N2 speciella mikroorganismer oxidation kan underlättas av H2O2 väteperoxid eller ozon O3. 4. Tungmetaller H2S +M2+(tungmet) MS +2H+ tungmetallsulfider är svårlösliga. 1 Labbar Instuderingshjälp till Kemitentan 16/1-98 Magnus Lagerberg 26