Gen expressionsanalys
advertisement

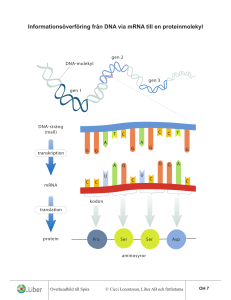
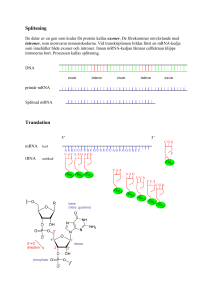
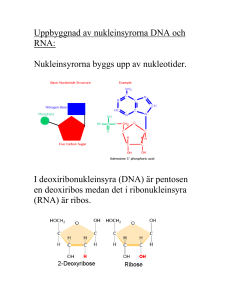
Genexpressions analys - RNA-uttryck Alla gener som är aktiva transkriberas: det bildas ett RNA (transkript). Proteinkodande gener transkriberas till mRNA, ribosomalRNA gener till rRNA osv. Man pratar ofta om sk. genexpression eller genuttryck. om man menar mRNA, benämns det ofta som mRNA expression/uttryck alt. protein expression/uttryck. mRNA expressionen bidrar givetvis till att ge en gen dess specifika funktion i en celleller vävnadstyp. Genom att studera mRNA expressionen kan man få viktig information om en gens funktion och hur den regleras. mRNA expressionen studeras vanligtvis utifrån några olika aspekter: 1. I vilken cell- eller vävnadstyp uttrcks mRNAt (vävnadsspecificitet)? 2. Vilken storlek har mRNAt och finns det flera mRNA (komplexa transkriptionsenheter)? 3. Hur mycket mRNA finns det (mRNA nivå) i en specifik cell- eller vävnadstyp? 4. Hur regleringen av mRNA expressionen sker? Det finns flera olika metoder att studera ovan frågeställningar. De flesta metoder kräver att man preparerar RNAt som skall analyseras. Preparation av RNA Preparerar man RNA från en vävnad får man sk. totalRNA vilket innehåller alla typer av RNA: rRNA, mRNA och tRNA. (mRNA utgör c:a 7-10% av totalRNAt) RNA kan prepareras från vävnad genom extraktion med sur fenol (DNA samt proteiner avlägsnas med fenolen) följt av etanol fällning av RNAt. En metod som utnyttjar denna extraktion kalls Trizol™ extraktionsmetoden. Isolering/anrikning av mRNA från totalRNA Man utnyttjar att de allra flesta mRNA har en polyA-svans när man isolerar mRNA. En polyT(20-50) esDNAsträng binds upp till små kulor (ofta av Fe) och blandas med totalRNAt. polyTnukleotiden och polyA-svansarna kommer att hybridisera och det är sedan möjligt att magnetiskt rena kulorna vilka drar med sig mRNAt. Resterande delar av RNAt kan sedan tvättas bort. Man får loss mRNAt genom att värma eller tillsätta salt. mRNAt kan sedan fällas med etanol och lösas upp i en en buffert. Denna procedur kallas PolyA+ selektion och det RNA som man får kallas Poly A+RNA. (det finns ett fåtal mRNA som saknar polyA-svans och dessa missar man!) Egenskaper hos RNA RNA är mer känsligt än vad DNA är och skall hanteras på is. Det förvaras bäst fruset -80°C. Känsligheten ligger i att RNA mycket lätt tuggas ner av RNA specifika nukleaser sk. RNaser. RNaser är mycket stabila proteiner som finns lite här och var. Bakterier samt alla andra organismer producerar dem och vi har dem på vår hud. Rika källor på RNaser är bukspottkörtel, tunntarm och mjälte. När man arbetar med RNA finns risk för RNase kontamination med RNA degradation till följd. Genom att arbeta sterilt och på is miskar man risken att RNAt degraderas (bryts ner). 1 mRNA analysmetoder: qRT-PCR ”northern blot” analys Array expressionsanalys RNA (cDNA) sekvensering * In situ hybridiserings analys PCR-baserad analys som har hög känslighet och är snabb. Analys som ger information om relativ mängd, mRNA storleken samt om det finns flera RNA. Metod att analysera expression av många gener. Låg känslighet men kraftfull eftersom många (alla) gener kan analyseras samtidigt. Sekvensering av hela cDNA bibliotek. Dyrt men kraftfull metod eftersom man får en fullständig information om vilka gener som uttrycks Metod att analysera mRNA direkt i vävnader ”på stället” (vävnadssnitt). RT-PCR (reverse transcriptase PCR) RT-PCR är en kvantitativ PCR-baserad analys som bygger på att mRNA först översätts till cDNA vilket utgör templat vid PCR analysen. En PCR reaktion körs och mängden produkt (PCR fragment) kommer att vara proportionell mot mängden cDNA. Specifikt primer-par för mRNA (cDNA) sekvesnsen Översätt mRNAt till cDNA med reverse transkriptas Använd cDNAt som templat vid PCR reaktionen Analysera mängden PCR produkt som producerats i de olika proverna efter ett specifikt antal cykler. cDNA syntes! Enligt ppt presentation: oligo dT primer – RT pol , Taila 5’ med cG – ”:a strängen med dC oligo etc. EcoRi adaptorer Relativa mängen PCR produkt i de olika proverna motsvarar skillnader i cDNA och följaktligen mRNA nivåer i urspungs RNA proverna. q RT-PCR (quantitative reverse transcriptase PCR, ibland ”real-time”) Mängden produkt bestäms efter varje cykel. Detta sker under själva PCR reaktionen (därför namnet real-time) genom att mäta specifik fluorescense som avges från PCR produkten. Det finns olika sätt att mäta produkten. Mängden produkt plottas mot antalet cykler (se bild för analys av prover A – G…). Antalet cykler som används för att nå upp till en specifk nivå (jämförelsenivån) används för att bestämma nivåerna av specifikt mTNA i varje prov. Resultatet ger ofta de relativa mRNA nivåerna mellan olika prov. Ex. (bild) prov A (skär jämförelsenivån vid c:a 8 cykler) och innehåller i detta fall drygt 8x (23)mer mRNA än prov B (som skär nivån vid c:a 11 cykler). Fördel: Snabb, billig, enkel och mycket känslig metod. Nackdel: Den extrema känsligheten gör att man lätt kan få falska positiva resultat. Trots att den är enkel är det svårt att bemästra reproducerbarheten och variationen i metoden. Även eventuella skevheter, fel eller variationer amplifieras ju exponentiellt och kan bli stora. 2 ”northern blot” analys Ger information om 1) mRNA nivåer samt 2) mRNA storlek(ar). Ett mRNA har en specifik längd som beror av genens struktur och hur "splicingen" sker. Genomsnitts mRNAt är 2-3kb men det finns mRNA som är 10kb eller större. northern blot analysen börjar med storleksseparation av RNA (totalRNA eller polyA+ RNA) med hjälp av agarosgelelektrofores. Olika RNA prover som skall jämföras körs i olika brunnar. Gelen måste köras under denaturerande betingelser därför att RNA har stor tendens att bilda sekundärstrukturer som påverkar vandringen i gelen och vandrar då ej efter längd. Formaldehyd tillsätts i gelen för detta ändamål. RNAt förs sedan över ("blottas") till ett nylon/nitrocellulosafilter som sedan behandlas för att fästa RNAt till filtret. För att kunna analysera ett specifikt mRNA måste man ha en specifik probe som kan hybridisera till mRNA som man vill studera. Proben måste var komplementär till mRNAt dvs - anti-sense och märks vanligtvis in med radioaktivitet genom random priming (för ett ds DNA fragmnet) eller in vitro transkribering (för ett fragment i en vektor). Principen för northern-blot analys är lik Southern-blot analys. Skillnaden ligger i att RNA sitter på filtret och inte DNA. 1. Gelelektrofores 2. Blot 3. Filterhybridisering med radioaktiv probe 4. Tvätt för att avlägsna icke hybridiserad probe 5. Exponering på röntgenfilm eller PhosphoImager för att se mängd och vilken storlek mRNAt som proben hybridiserar till har. Mängden radioaktivitet är proportionell till mängden mRNA. Genom att använda storleksmarkörer kan storleken på mRNAt bestämmas. Resultatet ger: Ett eller flera mRNA Längden på mRNA Relativa mRNA nivån i de olika proven (jämföra mellan prover på samma gel) 3 (Nivåerna visas av intensiteten av banden) Filtret kan användas på nytt med annan probe efter det att den gamla proben avlägsnats från filtret genom behandling vid 94°C 10 min. varvid hybridiseringen mellan mRNA och probe bryts. Nackdel: omfattande och tekniskt svår. Array expressionsanalys Array expressionsanalys används då man vill jämföra två prover m. a. p. vilka geners mRNA uttryck som skiljer mellan de två proverna. Tex. kan en tumörcell jämföras med sin normala motsvarighet. Metodens styrka ligger i att man kan jämföra tusentals gener på en och samma gång. Principen är att enkelsträngat DNA med känd sekvens som motsvarar en specifik gen fästs i ett rutmönster på ett filter eller en liten glas platta i små prickar. Man vet således vad varje prick/DNA kodar för och i vilken position i rutmönstret det sitter. RNA prepareras och används för att göra motsvarande cDNA från de två olika proverna ( ex. tumör och normal). Vid cDNA syntesen tillsätts fluorescerande märkning; (nukleotider med en fluorofor kopplad). Röd fluorofor till tumör-cDNAt Grön till normala cDNAt. Man blandar sedan de två inmärkta cDNA proverna och hybridiserar dem till DNAt på filtret eller glasplattan. Om en gen bara uttrycks i tumörprovet kommer det att fluorescera rött, om den uttrycks lika mycket i båda kommer det att fluorescera gult (rött + grönt) och är genen aktiv bara i normalcellerna kommer punkten att fluorescera grönt. Genom att studera vilka punkter som skiljer sig så kan man få reda på vilka gener som är olika reglerade (differentiellt uttryck) i de två proverna! Oligonukleotid arrays (Affymetrix arrays) Både oligonukleotider och cDNAs kan användas för att konstruera arrays. Principen påminner om varandra för båda arrayanalyserna. Företaget Affymetrix har utvecklat en metod att syntetisera oligonukleotider direkt på de små plattorna. 4 Fördelar: man analyserar alla gener Nackdelar: Bara högt uttryckta gener kommer att ge signaler så man kan missa många viktiga men lågt uttryckta gener. RNA (cDNA) sekvensering Allt RNA i forma av cDNA sekvenseras från en eller flera vävnader. Detta ger hela ”transkriptomet” och man kan bioinformatiskt få reda på vilka gener som uttrycks samt hur mycket mRNA från en eller många specifika gener det gjorts. Sekvenser från cDNA kloner från ett bibliotek som sekvenserats från ena änden kallas Ests. Est = expressed sequence tags. Dessa sekvenser (bara änden på ett cDNA) representerar ett cDNA (tag) som är uttryckt (expressed). All sekvensdata läggs i en databas som motsvarar det prov som analyserats. Man analyserar/”räknar” hur många sekvenser av ett specifikt mRNA det finns i databasen och därmed får man information om hur uttrycket av en gen eller flera (alla gener) är uttryckta i den vävnad från vilken RNAt var framrenat och sekvenserat. In situ hybridiseringsanalys Analys av mRNA in situ (på stället/plats) i celler och vävnader. Vävnaden förbehandlas och snittas i tunna snitt c:a 10-15µm tjocka. Snitten samlas upp på objektsglas för mikroskopi och hybridiseras som om det vore ett filter. Man använder en probe för att detektera mRNAt. Proben kan vara antingen radioaktivt inmärkt eller enzymatiskt. Det är vanligt att Ribo-prober används vid in situ hybridisering. Riboprobe måste vara anti-sense mot mRNAt som skall studeras Vid radioaktivt inmärkning skall α-[35S] ATP användas, lågintensiv β-strålare, kort räckvidd. Stegen vid in situ hybrdiserings analys: • Snittning av vävnad och uppsamling på objektglas • Hybridisering - 35S (snitt med probe) • Tvätt • Autoradiografi resp. exponering på fotografiskemulsion. Emulsion är flytande film som låtes torka i ett mycket tunnt skickt över vävnadssnittet • Framkallning av film/emulsion • Analys (emulsion måste analyseras i i mikroskop) Celler som har mRNA/probe hybrid blir radioaktiva och producerar silverkorn i emulsionen (den fotokemiska reaktionen) som syns som prickar över "positiva" celler. Icke-radioaktiv inmärkning DIG - ATP (DIG= digoxigenin) Digoxigenin-märkta nukleotider inkorporeras i anti-sense riboproben. Digoxigenin är en molekyl som finns hos vissa växter men ej djur. Det finns mycket bra antikroppar som binder DIG mycket specifik. Man anänder sig av antikroppar till vilka man kopplat (konjugerat) enzymet alkaliskt fosfatas. 1. Snittning av vävnad 2. Hybridisering med DIG - probe 3. Tvätt för att avlägsna icke hybridiserad probe 5 4. 5. 6. 7. Inkubering med fosfataskopplad anti-DIG antikropp Tvätt för att avlägsna icke bunden antikropp Färgningsreaktion Analys i mikroskop Färgreaktion: Färglöst substrat övergår i en olösligfärgad produkt i närvaro av alkaliskt fosfatas. Substratet NBT-BCIP ger blåfärgad produkt. Det finns olika enzymer och substrat. 6 Electrophoresis of DNA or RNA DNA or RNA RNA gel - denaturing conditions RNA 28S 18S 1 2 cDNA synthesis using Oligo-dT and dG Cloning using Eco R1 adaptors/linkers 3 4