Alternativ splicing: Mutationer i BRCA1 och BRCA2 orsakar
advertisement

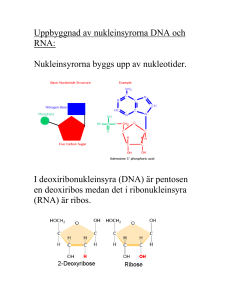
Institutionen för fysik, kemi och biologi Examenarbete Alternativ splicing: Mutationer i BRCA1 och BRCA2 orsakar bröstcancer Sahar Azadi Examensarbetet utfört vid IFM Biologi 2012-05-31 LITH-IFM-G-EX--13/2721—SE Linköpings universitet Institutionen för fysik, kemi och biologi 581 83 Linköping Avdelning, Institution Division, Department Datum Date Avdelningen för biologi Institutionen för fysik och mätteknik Språk Language x Svenska/Swedish Engelska/English Rapporttyp Report category Licentiatavhandling x Examensarbete C-uppsats D-uppsats Övrig rapport ________________ _______________ URL för elektronisk version ISBN ____________________________________________ ISRN ____________________________________________ Serietitel och serienummer Title of series, numbering ISSN LITH-IFM-G-Ex—13/2721--SE Handledare Supervisor: Johan Edqvist Ort Location: Linköping Titel Title Alternativ splicing: Mutationer i BRCA1 och BRCA2 orsakar bröstcancer Alternatice splicing: Mutations in BRCA1 and BRCA2 cause breastcancer Författare Author Sahar Azadi Sammanfattning Abstract During the past decade it has been shown that alternative splicing is a important mechanism for the proteome diversity. AS is a mechanism that generates a large amount of protein isoforms from a low number of human genes. Alternative splicing is regulated by four groups of cis-regulatory elements and different splicing factors. Even though AS is important for the diversity and complexity of different organisms it is also a source for different genetic diseases like cancer. This review article will focus on breast cancer and its connection to the mechanism of alternative splicing. Breast cancer is a common disease in women. In recent years many studies have shown an important relationship between mutations in the alternative splicing mechanism and the two most important genes involved in breast cancer BRCA1 and BRCA2. This article will also present different efforts against this disease. Nyckelord Keyword Alternativ splicing, BRCA1, BRCA2, Breast Cancer, Splicing, DNMT, PARP 1 Innehållsförteckning Abstrakt ...................................................................................................................................... 3 Introduktion ................................................................................................................................ 4 Alternativ splicing ...................................................................................................................... 5 Regleringsproteinerna SR och hnRNP .................................................................................. 7 Olika typer av alternativ splicing .......................................................................................... 8 Alternativ splicing har en stor betydelse vid cancer ............................................................. 9 Epigenetiska modifieringar och DNMT genen ........................................................................ 10 Viktiga gener för forskningen inom bröstcancer...................................................................... 11 Vilka domäner har BRCA1? ............................................................................................... 11 BRCA1 och homolog rekombination .................................................................................. 12 BRCA1 och non-homologous end-joining .......................................................................... 12 Mutationer i BRCA1 ........................................................................................................... 13 BRCA1 splice varianter ...................................................................................................... 14 BRCA2 ..................................................................................................................................... 15 Vilka domäner har BRCA2? ............................................................................................... 16 BRCA2 splicevarianter……………………………………………………………………17 Kopplingen mellan BRCA1 ochBRCA2.................................................................................. 17 Forskningen kring förebyggandet av bröstcancer .................................................................... 18 Splicingvarianter och läkemedel……………………………………………..……………….18 Samanfattning………………………………………………………………...……..…..……19 Referenser........................................................................................................................... …..21 2 Abstrakt Under det senaste decenniet har det visat sig att alternativ splicing är en viktig mekanism för proteomets mångfald. Alternativ splicing är en mekanism som genererar en stor mängd proteinisoformer från ett lågt antal mänskliga gener. Alternativ splicing regleras av fyra grupper av cis-regulatoriska element och olika splicing faktorer. Även om alternativ splicing är viktig för mångfalden och komplexiteten i olika organismer är det också en källa för olika genetiska sjukdomar som cancer. Denna review artikel kommer att fokusera på bröstcancer och dess koppling till mekanismen alternativ splicing. Bröstcancer är en vanlig sjukdom hos kvinnor. På senare år har många studier visat ett viktigt samband mellan mutationer i alternativ splicing mekanismen och de två viktigaste generna involverade i bröstcancer BRCA1 och BRCA2. Denna artikel kommer också att presentera olika insatser mot denna sjukdom. Nyckelord: Alternativ splitsning, BRCA1, BRCA2, bröstcancer, splicing, DNMT, PARP 3 Alternativ splicing: Mutationer i BRCA1 och BRCA2 orsakar bröstcancer Introduktion År 1977 upptäckte nobelpristagarna Philip Sharp och Richard Roberts att eukaryota gener oftast är uppdelade i kodande exoner och icke kodande introner [1]. Detta innebär att eukaryota gener är avbrutna, d.v.s. icke kodande sekvenserna ligger inom kodande regioner och bryter av den kodande genen. För de flesta eukaryota celler måste RNA genomgå olika processer innan den slutgiltige mRNA:t ska genomgå translation och syntetisera ett visst protein. En utav de viktigaste processerna kallas för splicing. Splicing innebär att intronerna plockas bort från prekursor-mRNA (pre-mRNA). Därutav består mRNA endast utav kodande sekvenser d.v.s. exoner som sätts ihop under splicing processen [2, 3]. Splicing sker via två esterfieringsteg. De två esterfieringstegen katalyseras av splicosomen. Splicosomen är en makromolekylkomplex som består bland annat av fem små ribonukleoprotein partiklar (snRNPs); U1, U2, U4, U5 och U6. Dessa snRNPs omsluter intronen vid splicing. Varje intron har en 3’ splice site region och en 5’splice site region. Intronens 5’ site innehåller en GU dinukleotid och 3’ siten har tre konserverade segment; förgreningspunkten, polypyrimidindelen och ett terminalt AG segment. Som det visas i figur 1, så börjar första esterfieringsteget med att en hydroxyl grupp i föreningspunkten attackerar fosfaten i 5’ siten. Detta leder till att exonen klyvs från intronen. Nu sitter 5’ intronen ihop med hydroxyl gruppen i förgreningspunkten på 3’ siten. Två produkter uppstår från denna klyvning. Andra esterfieringsteget är en attack från hydroxylgruppen på den fria exonens 3’ site mot fosfaten på 3’siten av intronen. Detta steg ligerar två exoner och frigör intronen [4,5,6]. Figur 1. De två esterfieringstegen för pre-mRNA splicing. Proteingrupper som är inblandade i första steget är blå markerade. Grupper från andra steget är rosa markerade. Bilden är tagen från källa 4 i referenslistan. 4 Dessa två esterfieringsteg sker med hjälp av spliceosomen. Spliceosom bildningen börjar med att snRNP U1 binder till 5’splice sitet på pre-mRNA:t. Heterodimeren U2AF (U2 auxuliary faktor), som är ett hjälparprotein, binder till 3’splice sitet och SF1 (splicingfaktor 1) binder till förgreningspunkten. Dessa tre steg utgör E-komplexet (early complex), som är ATP oberoende (Se fig.2). Nästa steg är bildandet av ett ATP-beroende A-komplex. Med hjälp av U2AF ersätts SF1 på förgreningspunkten utav snRNP U2. A-komplexet står för ATPdependent pre-spliceosome complex. I nästa steg binder tre snRNPs U5, U4 och U6 till Akomplexet och B-komplexet bildas. B-komplexet innehåller samtliga faktorer som krävs för att splicing ska ske. Innan B-komplexet blir aktivt sker en del konformationsförändringar. U1 och U4 lossnar och C-komplexet bildas, därefter sker splicingen [7,8,9]. Figur 2. Mekanismen för splicing. Innan själva splicingen sker måste splicosomen bildas på rätt plats. Detta sker i olika steg där intermediära komplex bildas. Bilden är tagen från källa 8 i referenslistan. Alternativ splicing Alternativ splicing är en process som medför att olika proteiner kan produceras från en enda gen. Studier har visat att 40-60% av människans gener genomgår alternativ splicing [10]. År 1977 upptäcktes exoner och introner hos andenovirusets hexon gen. Strax därpå upptäcktes processen splicing. Som tidigare nämnt sker splicing efter transkriptionen då introner tas bort från pre-mRNA och exonerna fogas ihop. Exonerna kan fogas ihop via flera olika kombinationer, vilket medför att det bildas olika mRNA isoformer från en gen. Detta kallas alternativ splicing [11]. 5 Figur 3. Bilden ger en generell förklaring till mekanismen alternativ splicing. En gen kan innehålla flera exoner och introner. Exonerna kan under splicing sättas ihop på olika sätt. Detta kallas alternativ splicing (AS). AS ger upphov till olika proteiner från samma gen. Bilden är från källa 12 i referenslistan. Det finns två modeller för mekanismen alternativ splicing; intron definition och exon definition. Antingen kan intronen plockas bort som i beskrivningen ovan, eller så kan exonen exkluderas [4]. Intron definition innebär att splicosomen och inblandade splicing proteiner känner igen intronen och placeras runt den. Intron definition anses vara det evolutionära ursprunget för alternativ splicing. Exon definition sker när de inblandade proteinerna för AS placeras runt exonen. En indikation för exon definition är hög koncentration av G-C bindningar. Exon definition är en mekanism som har utvecklats med tiden och är vanligare hos högre eukaryoter [13]. Det finns flera cis-element som avgör vilka exoner som ska uteslutas och vilka exoner som ska vara med. Dessa delas in i fyra grupper; exonic splicing enhancers (ESE), exonic splicing silencers (ESSs), intronic splicing enhancers (ISEs), intronic splicing silencers (ISSs) [10]. ESE och ESS förekommer i exoner som genomgår alternative splicing. ESE aktiverar närliggande splice siter och detta leder till att inkluderingsfrekvensen för exonen ökar vid alternativ splicing. För ESS gäller det motsatta, d.v.s. exkluderingsfrekvensen för exonen ökar [14]. ISE och ISS fungerar på motsvarande sätt men för introner [11]. 6 Figur 4. Bilden visar de olika splicingregulatorerna ESS, ESE, ISE och ISS. Splice site igenkänning styrs av att proteiner som SR, hnRNP, TIA1 m.m. interagerar med de olika regulatoriska sekvenserna. Bilden är tagen från källa 4 i referenslistan. Regleringsproteinerna SR och hnRNP Cis-elementen interagerar med regleringsfaktorerna, SR-proteiner (serin- och argininrik region) som initierar exoninkludering och hnRNPs (heterogeneous nuclear ribonucleoproteins) som inhiberar exoninkludering. SR-proteiner har en viktig roll vid splice site igenkänning. Dessa proteiner kan binda in till ESE och initierar exoninkludering i mRNAt. Det är fortfarande okänt om ESE aktiviteten är beroende av SR proteiner eller inte men deras närvaro verkar vara viktig för identifiering av exoner [15]. Alla SR proteiner innehåller två viktiga sekvenser. Ena sekvensen är RS domänen, som binder till andra RS domäner. SR proteiner kan även innehålla en eller två RRMs, RNA recognition motifs, som binder till RNA:t. RRMs sitter vid N-terminalen och RS domänen sitter vid C-terminalen. RS domänen fosforyleras via olika kinaser. Denna fosforylering är mycket viktig för att RS domänerna ska kunna interagera med varandra samt kunna vara inblandade i splicing mekanismen [16,17]. Ett utav de viktigaste SR proteinerna som spelar en stor roll vid splicing är ASF/SF2 (Alternative splicing factor/splicing factor 2). Genom att interagera med pre-mRNA och snRNPs ökar ASF/SF2 sin affinitet för splice siten [18,19]. Fosforylering av serin sker vid ASF/SF2 proteinets RS domän. Fosforyleringen sker med hjälp av SR specific protein kinase, SRPK1. Detta leder till att proteinet förs till kärnan och påverkar en del protein-protein interaktioner som sker i samband med splicing [20]. Ändring av mängden splicing faktorer i cancerceller har visat sig vara en betydelsefull faktor för cancer, t.ex. bröstcancerceller har en högre mängd av splicing faktorn SF2/ASF som är viktig för AS mekanismen.[21] En annan regleringsfaktor är hnRNPs (Heterogeneous nuclear ribonucleoproteins). HnRNPs är en multifuktionell proteinfamilj. Dessa proteiner är inblandade i splicing, mRNA export, lokalisering av mRNA, translation och stabilitet [22]. Proteinet hnRNP består av flera funktionella domäner. Den viktigaste domänen är RRM, som styr proteinets interaktioner med pre-mRNA. De flesta hnRNP proteiner innehåller även RGG boxar som är upprepningar av Arg-Gly-Gly tripeptider [23]. 7 HnRNPs inhiberar splicing. Detta kan ske på olika sätt. Proteinet kan binda till splice siten direkt, vanligtvis till ESS på pre-mRNA, och inhibera splicing. HnRNP kan även inhibera splicing genom att interagera med proteiner som binder till enhancern [24]. För att förstå hur hnRNP reglerar AS krävs lite bakgrundsfakta. En viktig skillnad mellan cancerceller och friska celler är deras metaboliska regulation. Mogna celler utnyttjar citronsyracykeln och oxidativ fosforylering, vid närvaro av syre, för maximal energi produktion. Celler som växer snabbt, t.ex. embryoniska celler och cancer celler, utnyttjar en annan metabolisk väg dvs. icke oxidativ nedbrytning av glukos. Dessa celler omvandlar glukos till laktat anaerobt. Detta fenomen kallas Warburg effekten. Ett enzym som är inblandad i den glykolytiska metabolismen är pyruvat kinas (PK). Proteinet hnRNP kontrollerar den metaboliska switchen mellan de två olika stadierna dvs oxidativ fosforylering och aerobisk glykolys. Detta görs genom att hnRNP påverkar alternativ splicing för enzymet PK och dess isoformer. Dessa studier påvisar återigen att alternativ splicing spelar en stor roll vid tumörbildningar och cancer.[25]. Mutationer som påverkar regleringsproteiner och komponenter som är inblandade i alternativ splicing medför högre risk för flera gener att modifieras felaktigt [26]. Alternativ splicing regleras via extracellulära signaler främst via aktivering av komplexa signal transduktions nätverk. I dagsläget finns det alltför lite information om hur dessa extracellulära signaler påverkar splicing faktor aktiviteten[27]. Olika typer av alternativ splicing Det finns flera typer av alternativ splicing mekanismer som kan delas in i fem grupper. Första och vanligaste gruppen är exon skipping. Exon skipping står för cirka 40% av alternativ splicing hos högre eukaryoter. Exon skipping innebär att ett exon tillsammans med dess sammanhängande introner splicas bort från transkriberingen. Förekomsten av exon skipping ökar ju högre upp i den eukaryotiska trädet man kommer, vilket innebär att den typen av alternativ splicing har en evolutionär betydelse för utvecklingen av högre eukaryoter [28,29,30]. Den andra och tredje gruppen är alternativ 3’ splice site (SS) selection och 5’SS selection. Dessa typer av mekanismer inträffar när två eller fler splice siter känns igen i ena änden av en exon. Den fjärde gruppen är mutually exclusive exons, det innebär att bara en exon väljs utav en grupp av uppradade exoner [30]. Den minst vanliga typen av alternativ splicing hos människan är den femte gruppen som kallas intron retention. Där får intronet vara kvar i mRNA. Denna mekanism är dock vanlig hos växter.[4] 8 Figur 5. Olika mekanismerna för alternativ splicing. Bilden är tagen från källa 30 i referenslistan. Alternativ splicing är viktig för reglering av genexpression hos eukaryoter. Många sjukdomar har även visats vara kopplade till en mutation eller en förändring i processen alternativ splicing. Sambandet mellan alternativ splicing och bildandet av onkogener och tumörsuppressorer har väckt stora intressen inom forskningen för olika sjukdomar bl.a. cancer. [31] Bröst cancer är en vanlig sjukdom hos kvinnor och under senare år har man kommit fram till viktiga samband mellan mutationer i alternativ splicing mekanismen för viktiga gener som kan ge upphov till bröstcancer.[32] Texten kommer att ta upp de kopplingar som har hittats mellan alternativ splicing och bröstcancer hittills. Eventuella hypoteser om huruvida man kan förhindra och behandla felaktig splicing kommer att diskuteras. Alternativ splicing har en stor betydelse vid cancer Alternativ splicing har visats spela en stor roll vid tumörutvecklingen i cancer. Detta kan göras antingen via inaktivering av tumörsuppressorer eller via aktivering av funktioner hos proteiner som bidrar till tumörbildning [32]. Studier har visat att förekommandet av alternativ splicing minskar hos cancerceller jämfört med normala celler. Detta kan bero på inaktivering av proteiner som reglerar splicingen. Även typen av alternativ splicing skiljer sig mellan cancerceller och vanliga celler. Cancerceller har en högre nivå av intron retention än vanliga celler som istället har exon skipping. Även typerna 3′ splice site och 5′ splice site förekommer mer hos cancerceller. Detta visas tydligt i figur 6 Exon skipping är den vanligaste typen av alternativ splicing hos de flesta eukaryoter [33]. 9 Figur 6. Fördelningen av alternativ splicing typer hos cancerceller (lila) jämfört med friska celler(blå). Bilden är tagen från källa 33 i referenslistan. Ett exempel på hur splicing varianter kan vara viktiga inom cancer är den humana DNMT genen (DNA metyltransferas). Genen kodar för de enzym som katalyserar metyleringen av DNA. Denna modifikation har oftast regleringseffekter [34]. Metyleringen av DNA har visat sig påverka cellbildningen, strukturen på kromosomen samt reglerar vissa genetiska uttryck. Studier har även visat att metylering av DNA har en direkt påverkan på transkriptionen. Idag finns det forskning som påvisar en direkt koppling mellan metylering, DNMT och cancer [35,36] . Epigenetiska modifieringar och DNMT genen Epigenetiska modifieringar är ärftliga samt reversibla förändringar i genuttrycket. Dessa modifieringar är oberoende av ändringar i själva DNA sekvensen. Exempel på epigenetiska modifieringar är DNA-metylering och histonmodifiering [37,38]. DNA-metylering har visats spela en stor roll vid utvecklingen av cancer. Det finns speciella enzymer s.k. DNAmetyltransferas (DNMT) enzymer som ger upphov till metyleringen av DNA:t. Många onormalt splicade typer av DNMT transkript har visat sig förekomma i tumör och cancerceller. Dessa mRNA transkript bidrar till att cellen förökar sig dubbelt så snabbt än vanliga celler, vilket leder till tumörbildning [34]. DNMT består av en grupp enzymer som katalyserar metyleringen av CpG dinukleotider på DNA:t. DNMT transfererar en metylgrupp från SAM (S-adenosyl-metionin) till C5 positionen på pyrimidinringen för cytosin i CpG dinukleotider [39]. SAM produceras i levern och är ett vanligt cosubstrat vid metyltransfereringar. CpG nukleotider är vanligtvis placerade på specifika delar av genen bland annat förekommer ometylerade CpG öar som är en sekvens med mycket hög C och G frekvens. CpG öar förekommer oftast vid promotorer. Metylering av CpG är mycket viktig för olika processer bl.a. genomisk imprinting, X-kromosom inaktivering, avlägsnandet av repetitiva element samt reglering av vissa genetiska uttryck [40,41]. 10 För metyleringen av CpG öarna i cancerceller krävs onormalt högt hypermetylering. Detta leder till transcriptional silencing, d.v.s. transkriptionen stoppas. När dessa CpG öar förekommer vid promotorer hos tumörsuppressorer leder det till att transkribering av dessa stoppas och suppressorerna bildas inte. Viktiga tumörsuppressorer för bröstcancer som drabbas är ER (estrogen receptor) och BRCA1 [42]. Vi återkommer till dessa suppressorer senare i texten. Det finns fem DNMT isoformer; DNMT1, DNMT2, DNMT3a, DNMT3b och DNMT3L. Det är bara tre av dessa isoformer som metylerar DNA:t. De typer som främst förekommer i cancerceller är DNMT1 och DNMT3b. Studier har visat att dessa två gener fungerar cooperativt dvs. båda generna måste slås ut för en märkbart minskad metylering samt minskad cancer spridning [43]. Alternativa splice varianter av isoformen DNMT3b förekommer mycket i cancerceller [44]. Även om dessa splice varianter inte kodar för katalytiskt aktiva proteiner kan de ge upphov till DNA metylering i cancerceller. Hur mekanismen för detta fungerar är fortfarande oklart [45]. Viktiga gener för forskningen inom bröstcancer Under den senaste tiden har många gener identifierats som är direkt inblandade i bröstcancer. Generna BRCA1 och BRCA2 är två exempel på dessa gener. BRCA1 breast cancer type 1 susceptibility protein, är en tumörsuppressor gen som identifierades år 1994. Studier har visat att BRCA1 genen har väldigt många olika splice varianter som även uttrycker sig på olika sätt. Än så länge har mer än ett trettiotals olika mRNA splice varianter identifierats [32]. Det har visats att mutationer i dessa proteiner leder till uppkomst av tumörer främst i bröst och äggstockar. Denna gen har många olika splice varianter gör den till en bra utgångspunkt för studier av alternative splicing och kopplingen till bröstcancer. Främsta orsaken till bröstcancer är ärftlighet. Både BRCA1 och BRCA2, som också är en tumör suppressor gen, är ärftliga bröstcancer gener. Bärare på mutationer i generna BRCA1 och BRCA2 uppskattas ha 85% högre risk för bröstcancer [48]. I normala celler fungerar BRCA1 och BRCA2 som proteiner där de stabiliserar DNA:t och förhindrar okontrollerad celltillväxt. BRCA1 är även inblandad i reglering av cell cykeln, centrosom duplikationen samt aktivering av transkriptionen [49]. Studier har visat att mutationer i dessa gener förekommer främst hos Ashkenazi judar [48]. Vilka domäner har BRCA1? BRCA1 genen kodar för ett protein med 1863 aminosyror hos människan, och har 24 exoner. N-terminalen består av en zinc-finger domän som är en Cys-His domän. Denna domän brukar förekomma hos proteiner som kan interagera med DNA. Exon 11 är det största exonet hos BRCA1. Denna exon kodar för mer än 60% av proteinet. Den domän av proteinet som kodas av exon 11 kan interagera direkt eller indirekt med proteiner som RAD50, RAD 51, RB och c-Myc [49]. C-terminalen för BRCA1 genen är viktig för dess tumörsuppressor aktivitet. Det är mutationer i denna region som leder till ökad risk för bröstcancer. Denna region innehåller två repeterande sekvenser som kallas BRCT repeats. BRCT repeats fungerar som protein-protein interaktions moduler [50]. Studier visar att BRCT repeats sitter ihop på ett sätt som är mycket viktig för BRCA1:s roll som tumörsuppressor. C-terminalen hos BRCA1 interagerar med 11 många proteiner bl.a. BRCA2, ATM, BARD1 och p53. På grund av dessa interaktioner kan saknad av funktionellt BRCA1 ge upphov till genetisk instabilitet, ökad apoptos och störningar för cellens tillväxt [51]. Mutationer i dessa proteiner är också väsentliga i olika grad för uppkomsten av bröst cancer[49]. En av BRCA1 viktigaste uppgifter är att åtgärda skador på DNA:t. Dessa skador kan vara interna eller externa som t.ex. UV eller oxidativ stress. BRCA1 lokaliseras oftast till dubbelsträngs brott på DNA:t [52]. Olika skador på DNA:t medför olika reparationsprocesser. Dubbelsträngsbrott repareras vanligtvis via homolog rekombination (HR) eller nonhomologous end-joining (NHEJ). Proteinet BRCA1 medverkar i båda dessa reparationsprocesser [53]. BRCA1 och homolog rekombination Proteinet som kodas från BRCA1 genen är inblandad i processen homolog rekombination. Denna process används för att reparera dubbelsträngs brott i cellernas DNA. När processen HR är muterat, antingen via mutationer i BRCA1 eller skador i andra inblandade proteiner, måste cellen utnyttja andra typer av reparationsprocesser. Dessa reparationssystem är mer felbenägna än HR. Detta kan leda till ostabila kromosombildningar och ökad risk för tumörbildning [54]. Reparering av HR utnyttjar ena systerkromatiden som mall för att få till rätt baspar i DNA:t. Dubbelsträngsbrott(DSB) aktiverar ATM kinaset (ataxia telangiectasia-mutated), som i sin tur aktiverar hela DNA damage responsen. Repareringsprocessen börjar med att 3’änden av varje sida av DSB frigörs med hjälp av MRN (RAD50-MRE11-NSB1) komplexet och detta styrs av BRCA1. MRN komplexet binder till det skadade DNA:t och genomgår en del konformations förändringar som i sin tur håller ATM kinaset aktivt på DSB siterna [55]. Den enkelsträngade DNA:t omges av RPA, en grupp av proteiner som binder till RAD51 som i sin tur katalyserar invasionen av ssDNA:t till systerkromatider. Då systerkromatiden används som mall i denna reparations process elongeras ssDNA och holiday junctions bildas mellan de två systerkromatiderna. Slutligen löses holiday junction och DNA:t ligeras felfritt [53]. BRCA1 och non-homologous end-joining Till skillnad mot HR, som använder systerkromatiden som mall för reparering av DNA:t , så innebär NHEJ en direkt ligering av DNA-änden via ett ligeringskomplex. Det kan uppstå fel i repareringen mer ofta än vid HR men ändå så spelar NHEJ en stor roll för DNA reparering och den genetiska stabiliteten. Det har gjorts många studier som visar att NHEJ regleras av BRCA1. Skador på gener inblandade i NHEJ har visats leda till ökad risk för utveckling av bröstcancer [53]. Man har försökt få fram kopplingen mellan NHEJ och BRCA1 och hur mutationer och defekter i BRCA1 kan leda till cancer [56]. Det har nyligen påvisats att skadade BRCA1 hos mouse embryonic fibroblasts (MEFs) leder till en tydlig minskad aktivitet av NHEJ [57,58]. Forskning har gjorts för att hitta liknande samband hos människan. Fortfarande kan inget fastställas då olika studier och försök har lett till olika resultat. En förklaring kan vara att det finns fler än en NHEJ mekanism och där BRCA1 inte behövs vid alla dessa mekanismer. Hos människan har BRCA1 polymorfier en stor betydelse vid NHEJ och bröstcancer [56]. 12 Mutationer i BRCA1 Studier har visat att BRCA1 är inblandad i regleringen av alla faser av cell-cykeln. Mutationer i BRCA1 kan därför medföra skador i DNA samt apoptos. Figur 7 visar att mutationer i BRCA1 leder till genetisk instabilitet. Detta på grund av mutationens påverkan på cellcykelfaserna, centromduplikationen och DNA reparerings mekanismen. Den genetiska instabiliteten visar sig på tre olika sätt som i sin tur leder till defekter samt cancer [51]. Figur 7. En sammanfattning av vad mutationer i BRCA1 kan medföra. Bilden är tagen från källa 51 i referenslistan. Genom att studera BRCT regionen har många olika mutationer som brukar förekomma i bröstcancer kartlagts. Ett exempel är nonsense mutationen som kan uppstå vid Tyr 1853. Denna mutation raderar de 11 sista aminosyrorna på BRCT domänen vilket är en typisk mutation för det tidiga stadiet för utvecklingen av bröst cancer. Det som händer är att de hydrofobiska delar som är i kontakt med den regionen som raderas, ändrar konformation och det leder till destabilisering av proteinet. Ett annat exempel är två missense mutationer i BRCT regionen. Dessa kallas för A1708E och M1775R. Båda är relaterade till bröst och äggstockscancer. Dessa mutationer skadar DNA regleringsfunktionen hos BRCA1 samtidigt som de försvagar BRCT domänens roll som transkriptions aktivator. Som figur 8 visar är Ala 1708 och Met1775 två hydrofobiska regioner mellan de två BRCT strängarna. Ala 1708 är belägen på 2 spiralen som även sitter ihop med 1’ och 3’ som är belägna I center av interaktionen. Denna region kan lätt attrahera negativt laddade Glu. Met1775 kan substitueras med en Arg. Dessa mutationer destabiliserar den hydrofobiska interaktionen mellan BRCT strängarna. 13 Figur 8. BRCT regionen. Bilden visar sekvenserna Ala1708 och Met1775 som är två hydrofobiska regioner mellan de två BRCT strängarna. Bilden är tagen från källa 50 i referenslistan. Williams et al. har gjort en studie för att påvisa konsekvenserna av dessa mutationer hos BRCT. Studien visar att destabilisering av BRCT regionen ökar risken för bröstcancer. Orsaken till de flesta missense mutationer som förekommer i BIC databasen är fortfarande okända. BIC står för breast cancer information core och är en databas [83], som tar upp de olika mutationer som identifierats inom bröstcancer. Men i de flesta fall ligger orsaken i destabilisering av BRCT domänen. Det förekommer även mutationer som ligger på ytan av BRCT och har inget med interaktionen mellan de två strängarna att göra. Dessa mutationer kan istället leda till att förändra en viktig bindningssite för BRCT regionen som är viktig för dess funktion [50]. BRCA1 splice varianter Som tidigare nämnts spelar alternativ splicing en stor roll för den genetiska diversiteten. En kartläggning av de olika splice varianterna av BRCA1 kan ge en bättre förståelse om dess funktion som bland annat tumörsuppressor. Tabell 1 visar de hittills kända splice varianterna av BRCA1. Tabellen visar även vilka organ dessa splicevarianter förekommer i. Än har det inte gjorts studier på varje specifik splicevariant men fyra av dessa förekommer ofta i olika vävnader och kallas för predominanta splicevarianter . De predominanta splicevarianterna är full length, D(9,10), D(11q), och D(9,10,11q) [59]. Dessa varianter används flitigt i olika studier. I vissa friska men även sjuka bröstvävnader förekommer splice typerna full length och D(11q) mer än typerna D(9,10) och D(9,10,11q). Hos de flesta bröst och äggstocks tumörer förekommer främst splice varianten D(9,10) men även mindre mängd D(11q). Dessa skillnader i resultat kan delvis bero på olika metoder som används samt heterogeniteten av de olika tumörbiopsierna. Det är dock bevisat att under G1 fasen i cellcykeln ökar transkriptionen av BRCA1 då ökar även mängden av fullängdsvarianten av BRCA1 jämfört med de andra splice varianterna. 14 Tabell 1. De kända BRCA1 splicevarianterna hos människan, indikerar vilken exon som saknas samt de organ där de främst förekommer [59]. Namn på splicevarianten Full legnth BRCA1 With exon 1a (NM_007294) With wxon 1b (NM_007295) ∆(2-10)(NM_007297) ∆(5) ∆(5q, 6) ∆(9,10)(NM_007302) ∆(9,10,11q) (NM_007305) ∆(9,10,11) (NM_007298) ∆(11q) (NM_007304) ∆(11) (NM_007303) ∆(14-17) (NM_007299) ∆(14-18) (NM_007300) ∆(3) ∆(3,5q) ∆(5q) ∆(6,7) ∆(9) ∆(15-17)(NM_007301) organ Bröst, äggstockar, testiklar, tymus m.fl. Bröst, äggstockar, testiklar, tymus Placenta Bröst, lymfocyter Bröst, äggstockar, lymfocyter Bröst, lymfocyter Bröst, äggstockar, lymfocyter Bröst, äggstockar, lymfocyter Bröst, lymfocyter Bröst, äggstockar, lymfocyter Äggstockar, tyroid Bröst, lymfocyter Bröst, lymfocyter Bröst, lymfocyter Lymfocyter Bröst, äggstockar, lymfocyter Lymfocyter Lymfocyter Bröst, lymfocyter BRCA2 Genen BRCA2 identifierades år 1995. Den klassades som en tumörsuppressor gen som stabiliserar DNA:t och är inblandad i olika regleringsprocesser. Den humana BRCA2 genen består av 27 exoner som kodar för 3418 aminosyror [60]. BRCA2 förekommer huvudsakligen i HR mekanismen. Som tidigare nämnts är HR en reparationsprocess för DNA:t där skadade dubbelsträngsbrott repareras och byts ut. Proteinet Rad51 är viktig och katalyserar HR mekanismen. Rad51 bildar ett nukleofilament på ssDNA:t vid dubbelsträngsbrott. BRCA2 hjälper till vid bindningen av RAD51 till DSB. Idag finns det över 1800 olika varianter av BRCA2. Mutationer i denna gen ökar risken för bröst och äggstockscancer. Det är fortfarande oklart vilka varianter som förekommer mest i cancervävnader [61]. 15 Figur 9. Mekanismen för hur BRCA2 kontrollerar Rad51. Skador på DNA:t triggar igång repareringsprocessen. Den inaktiva Rad51-BRCA2 komplexet aktiveras. Den aktiva formen bildar nukleoproteinfilament för rekombinationen. Mekanismen för hur detta går till är fortfarande oklart. Man vet inte än om det aktiva komplexet innefattar en konformationsändring eller Rad51 separation från BRCA2. Fosforylering kan vara ett steg till att aktivera Rad51-BRCA2 komplexet [62]. Vilka domäner har BRCA2? BRCA2 består av en central DNA binding-domän (DBD) samt åtta BRCT-sekvenser som binder till RAD51. Proteinet har även NLS-domäner som hjälper till vid lokalisering till cellkärnan [63]. DBD består av fem domäner; 190-amino-acid- α-helix , tre oligonukleotid bindandedomäner (OB) som binder till ssDNA samt en tower domän (TD), som skjuts ut från OB2 för att binda till dsDNA. Varje BRC sekvens har olika affinitet för RAD51. Studier har visat att mutationer inom interaktionen mellan BRC4 och RAD51 spelar en stor roll hos cancerpatienter. N-terminalen på BRCA2 binder till PALB2, vilket är ett protein som kopplar ihop BRCA1 och BRCA2. Vi återkommer till denna protein senare i texten. C-terminalen på BRCA2 består av nuclear localization sequence (NLS regionen) samt cyclin-dependentkinase (CDK) vilket är en fosforyleringsregion, som också binder till RAD51[64]. 16 Figur 10. De olika domänerna på BRCA2.Figuren visar även vilka proteiner som binder till de olika sekvenserna. Bilden är tagen från källa 64 i referenslistan. BRCA2 splicevarianter Som tidigare nämnt har avbrott i BRCA2 genen en stor påverkan för utvecklingen av bröstcancer. Man har hittat över 1800 splicevarianter av BRCA2. Studier har även visat kopplingar mellan vissa av dessa splicevarianter och bröstcancer [78]. Många av dessa mutationer har klassats som founder mutationer. Founder mutationer är mutationer som förekommer i DNA:t hos individer från en viss population. Dessa mutationer är ärftliga och kan oftast även visa åldern på mutationen. Ett slående exempel på dessa mutationer förekommer hos patienter från Island. Där förekommer mutationen BRCA2 999del5 hos nästan alla bröst/äggstocks cancerfall. I Sverige är mutationen BRCA24486delG vanligt förekommande hos svenska patienter [79]. En annan splicevariant av BRCA2 som har kopplats med bröstcancer är 8393C>G. Denna mutation innebär att kvävebas nr 8393 byts ut från cytosin till guanin. Detta medför att en ESE sekvens tas bort, vilket leder till att tre SRproteiner inte kan binda in. Då denna mutation ligger på exon 18 leder det hela till att exon 18 tas bort ur transkripten [77]. Kopplingen mellan BRCA1 ochBRCA2 Proteinet BRCA1 är inblandad i olika DNA reparerings processer bl.a. DDR signalering (DNA damage repair), HR, NHEJ och SSA (single strand annealing). Däremot är BRCA2 huvudsakligen involverad i HR mekanismen. De symptom som uppstår via ärftliga mutationer i BRCA1 och BRCA2 generna är oftast identiska. Den huvudsakliga länken mellan dessa två proteiner är HR mekanismen [65]. PALB2 är ett protein som förbinder BRCA1 och BRCA2. PALB2 binder direkt till båda proteinerna och skapar en fysisk länk mellan dem. Interaktionen mellan PALB2 och BRCA2 har visat sig vara viktig för att binda RAD51 till ssDNA. Dessutom är denna interaktion väsentlig för rekryteringen av BRCA2 och Rad51 till platsen för DNA-skador och för HR. Mutationer i alla dessa gener är relaterade till HBOC syndromen (Hereditary breast-ovarian cancer syndrom). HR är även en viktig mekanism för tumörsuppressor aktiviteten. Mutationer i BRCA1 och BRCA2 är dominanta för HBOC syndromen men det förekommer även andra gener där mutationer hos dessa är viktig för HBOC men dessa förekommer i mindre omfattning. Som exempel kan man nämna ATM och CHEK2. Kvinnor som bär på muterade 17 ATM gener löper dubbelt så hög risk att drabbas av bröstcancer. CHEK2 mutationer förekommer främst hos nord europeiska kvinnor. (66,67,68) Forskningen kring förebyggandet av bröstcancer Det har gjorts mycket forskning kring bröstcancer. Idag finns det många dokumenterade försök kring detta där man har olika tillvägagångssätt. Tills idag finns det inga skillnader mellan behandlingar för ärftliga och sporadiska fall av bröstcancer men det finns studier som visar att riktad terapi är mer effektiv för kvinnor med BRCA1-BRCA2 relaterade tumörer. Studier har gjorts på mekanismen homolog rekombination. De studier som har gjorts är bl.a. att man har hitta epigenetiska förändringar I HR mekanismen för cancer patienter bl.a. metylering. Därmed har man kunnat utnyttja specifika microarrays för DNA metylering vid HR. En fördel med denna metod är att DNA är stabilare än RNA och lättare att isolera. Man har nyligen påvisat att BRCA1 och BRCA2 är mycket känsliga mot PARP inhibitorer (poly ADP ribose polymerase) [69,70]. PARP är den viktigaste reglerings enzymet i repareringsmekanismen Base excision repair (BER) samt reparerar DNA vid enkelsträngsbrott (SSB) [71]. Minskad PARP aktivitet ändrar bildningen av SSBs som istället omvandlas till DSBs vid replikationen och startar igång HR mekanismen. [72]. Detta leder till att skadade BRCA1 och BRCA2 celler förstörs. PARP inhibitorer har visat antitumör aktivitet vid bl.a. bröst, äggstocks och prostata cancer som har mutationer i BRCA1 och BRCA2 [73]. Därav verkar dessa enzymer vara effektiva behandlingsalternativ för cancer patienter [74]. PARP aktiverar BER genom att snabbt rekryteras till skador på DNA siten och sätter sig på DNA:t via dess DNA-bindande domän. Den katalytiska aktiviteten ökar för PARP genom att poly(ADP-ribos) bildas och förs till acceptor proteiner vilket signalerar rekryteringen för andra inblandade proteiner som XRCC1 och DNA-ligase III som startar BER för att reparera SSBs. Om PARP inhiberas försämras BER mekansimen och SSBs omvandlas till DSBs vid celldelningen. HR mekanismen tar över och DSB:s repareras. Tumörceller som har en icke fungerande HR på grund av muterade BRCA1/2 är mycket känsliga för effekten av PARP hämning då oreparerade DNA skador leder till celldöd [75]. Tills idag har man framställt flera olika PARP-inhibitorer och många fler är under framställning. DNA reparering och PARP är viktiga forskningsområden för bröstcancer forskning men förståelsen för vilka tumörer som kan vara mest känsliga är viktigt och kräver vidare forskning. Splicingvarianter och läkemedel Alltfler sjukdomar har visats vara relaterade till någon form av alternativ splicing. Det kan vara allt ifrån inkludering av felaktiga splicesiter i transkriptionen eller nedreglering av den cellulära splicing mekanismen. Alternativ splicing har därför blivit ett viktigt område inom läkemedelsforskningen. Förändrade splicing mönster kan fungera som markörer för de cellulära förändringar som uppstår i samband med olika sjukdomar, vilket ger diagnosiskt och prognosiskt information. Exempel på nya behandlingsstrategier är (i) över exponering av 18 proteiner som ger upphov till splicing av den påverkade exonet (ii) användning av antisense oligonukleotider (iii) SiRNA baserade läkemedel för att dämpa gen uttryck (iv) transsplicing metoden vilket innebär att man ersätter det muterade exonet med en vildtyps exon [80]. En av de viktigaste behandlingsmetoden är antisense strategier. Principen för denna metod är bindningen av antisense oligonukleotider till target mRNA:t, vilket sätter stopp för translationen. Antisense oligonukleotider består oftast av 15-20 nukleotider som är komplementära till target DNA:t. Denna metod är mycket användbar då den har en hög specificitet samt är billig jämfört med andra metoder [81]. Nyligen har man även utvecklat antisense oligonukleotider till anti-apoptotiska splice varianter för att sänka den apoptotiska tröskeln för cancer tumörer. Detta ska ge en mer effektiv kemotrapeutisk behandling [82]. DATAS – differential analysis of transcripts with alternative splicing – är en mycket användbar teknik som används för att systematiskt identifiera RNA-splicing förändringar i ett genom. Detta leder till upptäckten av nya splice varianter som inte kan detekteras via andra metoder. Denna metod kan användas för jämförelse mellan RNA transkript för patienter som reagerar mot läkemedel och de patienter som inte reagerar mot det. Detta för att jämföra de alternativt splicade exoner och introner som skiljer sig mellan RNA transkripten för dessa patienter. Ökad förståelse för alternativ splicing samt karakterisering av olika splice varianter mha tekniker som DATAS kommer att ha en stor påverkan för forskningen inom cancer behandling [80,82] Sammanfattning Alternativ splicing är en process som ger upphov till flera olika proteinisoformer från en enda gen. Detta innebär att de kodande exonerna för en gen kan fogas ihop på olika sätt för att få olika proteiner. Vilka exoner som ska inkluderas och vilka exoner som ska tas bort avgörs via fyra olika cis-element; ESE, ESS, ISE samt ISS. Dessa cis-element interagerar med regleringsfaktorerna SR-proteiner och hnRNPs. SR-proteiner har en viktig roll vid splice site igenkänning och hnRNPs inhiberar splicing [10,11,12]. Studier har visat att alternativ splicing spelar en stor roll för tumörutvecklingen i olika cancersjukdomar. Bröstcancer är en av de mest förekommande cancersjukdomen hos kvinnor. Idag görs det mycket forskning kring utvecklingen av bröstcancer och man har funnit två mycket viktiga gener som är inblandade i denna sjukdom dvs. generna BRCA1 och BRCA2. Dessa gener är tumöresuppressorer där mutationer i dessa leder till tumörbildning i bröst och äggstockar [32,46]. Studier har gjorts på de olika splice varianterna för dessa två gener och detta har lett till fler och mer effektiva behandlingsmetoder. Vi har fortfarande inte tillräckligt med kunskap om alla de olika mutationer som uppstår vid bröstcancer. Det krävs fortfarande mer forskning för att veta hur de olika mutationerna påverkar olika cellulära signalvägar eller hur de ökar risken för tumörens spridning. 19 Framtidens utmaning är att kunna utnyttja dessa kunskaper för att förbättra behandling och förebyggandet av bröstcancer. ‘ 20 Referenser [1]. Shampo, M. A., Kyle, R. A. 2003. Richard J. Roberts--Nobel Laureate for discovery of split genes. Mayo Clin Proc. 78(2):132. [2]. Clancy, S. 2008. RNA splicing: introns, exons and spliceosome. Nature Education 1(1). [3]. Lewin, B. 2008. Genes IX. 10th ed. Sudbury: Jones and Bartlett Publishers, Inc. [4]. Chen, M. & Manley, J. L. 2009. Mechanisms of alternative splicing regulation: insights from molecular and genomics approaches. Nature Rev. Mol. Cell Biol. 10:741–754. [5]. Hui, J. 2009. Regulation of mammalian pre-mRNA splicing. Sci. China C Life Sci. 52: 253–260. [6]. Licatalosi, D. D. och Darnell, R. B. 2010. RNA processing and its regulation: global insights into biological networks. Nature Rev. Genet. 11:75–87 [7]. Schellenberg, M. J., Ritchie, D. B. och MacMillan, A. M. 2008. Pre-mRNA splicing: a complex picture in higher definition. Trends Biochem Sci. 33(6):243-6 [8]. Biamonti, G. och Caceres, J. F. 2009. Cellular stress and RNA splicing. Trends Biochem Sci. 34(3):146-53 [9]. Will, C. L. och Lührmann, R. 2001. Spliceosomal UsnRNP biogenesis, structure and function. Current Opinion in Cell Biology. 13:290–301 [10]. Matlin, A. J., Clark, F., och Smith, C. W. 2005. Understanding alternative splicing: towards a cellular code. Nat. Rev. Mol. Cell Biol. 6:386–398. [11]. Modrek, B. och Lee, C. 2002. A genomic view of alternative splicing. Nat Genet. 30(1):13-9. [12]. Kashyap, L och Tripathi, P. 2008. Alternative Splicing. Department of Biochemistry, Aligarh. Engineering and Biotechnology, New Delhi, India. Immunology Group, International Centre for Genetic. [13]. Schwartz, S., Meshorer, E. och Ast, G. 2009. Chromatin organization marks exon– intron structure. Nature Struct. Mol. Biol. 16: 990–995. [14]. Luca Cartegni, L., Wang, J., Zhu, Z., Zhang, M. Q. och Krainer, A. R. 2003. ESEfinder: a web resource to identify exonic splicing enhancers. Nucleic Acids Res. 31(13): 3568–3571. [15]. Black, D. L. 2003 Mechanism of alternative pre-messenger RNA splicing.Annual Review of Biochemistry 72: 291-336 [16]. Twyffels, L., Gueydan, C., Kruys, V. 2011. Shuttling SR proteins: more than splicing factors. FEBS J.278(18):3246-55 21 [17]. Collins, L. och Penny, D. 2006. Proceedings of the SMBE Tri-National Young Investigators' Workshop 2005. Investigating the intron recognition mechanism in eukaryotes.Mol Biol Evol. 23(5):901-10. [18] Graveley, B. R. 2000. Sorting out the complexity of SR-protein functions. RNA. 6(9):1197-211. [19]. Wang, Z., Rolish, E. M., Yeo, G. och Tung, V. 2004. Systematic identification and analysis of exonic splicing silencers. Cell. 119(6):831-45. [20]. Hagopian, J. C., Ma, C.T., Meade, B. R., Albuquerque, C. P., Ngo, J. C., Ghosh, G., Jennings, P. A., Fu, X. D., Adams, J. A. 2008. Adaptable molecular interactions guide phosphorylation of the SR protein ASF/SF2 by SRPK1 J. Mol. Biol. 382 (4): 894–909. [21]. Ghigna, C., De Toledo, M., Bonomi, S., Valacca, C., Gallo, S., Apicella, M., Eperon, I., Tazi, J., Biamonti, G. 2010. Pro-metastatic splicing of Ron proto-oncogene mRNA can be reversed: therapeutic potential of bifunctional oligonucleotides and indole derivatives. RNA Biol.7(4):495-503. [22]. Dreyfuss, G., Kim, V. N., Kataoka, N. 2002. Messenger-RNA-binding proteins and the messages they carry. Nat Rev Mol Cell Biol. 3(3):195-205. [23]. Dreyfuss, G., Matunis, M. J., Piñol-Roma, S., Burd, C. G. 1993. hnRNP proteins and the biogenesis of mRNA. Annu Rev Biochem.62:289-321. [24]. Martinez-Contreras, R., Cloutier, P., Shkreta, L., Fisette, J. F., Revil, T., Chabot, B. 2007. hnRNP proteins and splicing control. Advances in Experimental Medicine and Biology 623:123-47. [25]. Chen, M., Zhang, J., Manley, J. L. 2010. Turning on a fuel switch of cancer: hnRNP proteins regulate alternative splicing of pyruvate kinase mRNA.70(22):8977-80. [26]. Ward, A. J. och Cooper, T. A. 2010. The pathobiology of splicing. J Pathol. 220(2):15263. [27]. Srebrow, A. och Kornblihtt, A. R. 2006.The connection between splicing and cancer. Journal of Cell Science119: 2635-2641. [28]. Sugnet, C. W., Kent, W. J., Ares, M. Jr., Haussler, D. 2004. Transcriptome and genome conservation of alternative splicing events in humans and mice. Pac Symp Biocomput. 66-77. [29]. Kim, E., Magen, A., Ast, G. 2007. Different levels of alternative splicing among eukaryotes. Nucleic Acids Res. 35(1):125-31. [30]. Cartegni, L., Chew, S. L., Krainer, A. R. 2002. Listening to silence and understanding nonsense: exonic mutations that affect splicing. Nat Rev Genet. 3(4):285-98. 22 [31]. Skotheim, I. R. och Nees, M. 2007. Alternative splicing in cancer: Noise, functional, or systematic?.The International Journal of Biochemistry & Cell Biology 39:1432–1449. [32]. Lixia, M., Zhijian, C., Chao, S., Chaojiang, G., Congyi, Z. 2007. Alternative Splicing of Breast Cancer Associated Gene BRCA1 from Breast Cancer Cell Line. Journal of Biochemistry and Molecular Biology 40(1):15-21 [33]. Kim, E., Goren, A., Ast, G. 2008. Insights into the connection between cancer and alternative splicing. Trends Genet. 24(1):7-10. [34]. Fackenthal, J. D. och Godley, L. A. 2008. Aberrant RNA splicing and its functional consequences in cancer cells. Dis Model Mech.1(1):37-42. [35].Jones, P. L., Veenstra, G. J., Wade, P. A., Vermaak, D., Kass, S. U., Landsberger, N., Strouboulis, J., Wolffe, A. P. Methylated DNA and MeCP2 recruit histone deacetylase to repress transcription. 1998. Nat Genet. 19:187–191. [36].Nan, X., Ng, H. H., Johnson, C. A., Laherty, C. D., Turner, B. M., Eisenman, R. N., Bird, A. 1998. Transcriptional repression by the methyl-CpG-binding protein MeCP2 involves a histone deacetylase complex. Nature 393:386–389. [37]. Baylin, S. B., Esteller, M., Rountree, M. R., Bachman, K. E., Schuebel, K., Herman, J. G. 2001. Aberrant patterns of DNA methylation, chromatin formation and gene expression in cancer. Hum Mol Genet. 10: 687-692. [38] Santos, F. och Dean, W. 2004. Epigenetic reprogramming during early development in mammals. Reproduction 127:643-651 [39]. Miranda, T. B. och Jones, P. A. 2007. DNA Methylation: The Nuts and Bolts of Repression. J. Cell Physiol. 213(2):384–390. [40]. Fatemi, M., Pao, M. M., Jeong, S., Gal-Yam, E. N., Egger, G., Weisenberger, D. J., Jones, P. A. 2005. Footprinting of mammalian promoters: use of a CpG DNA methyltransferase revealing nucleosome positions at a single molecule level. Nucleic Acids Res 33 (20): e176. [41]. Saxonov, S. och Berg, P., Brutlag, D. L. 2006. A genome-wide analysis of CpG dinucleotides in the human genome distinguishes two distinct classes of promoters. Proc Natl Acad Sci USA 103(5): 1412–1417. [42]. Kurkjian, C., Kummar, S., Murgo, A. J. 2008. DNA Methylation: Its Role in Cancer Development and Therapy. Curr. Probl. Cancer 32:187–235. [43]. Rhee, I., Bachman, K. E., Park, B. H., Jair, K. W., Yen, R. W., Schuebel, K. E., Cui, H., Feinberg, A. P., Lengauer, C., Kinzler, K. W., Baylin, S. B., Vogelstein, B. 2002. DNMT1 and DNMT3b Cooperate to Silence Genes in Human Cancer Cells. Nature 416: 552–526. 23 [44]. Saito, Y., Kanai, Y., Sakamoto, M., Saito, H., Ishii, H., Hirohashi, S. 2002. Overexpression of a Splice Variant of DNA Methyltransferase 3b, DNMT3b4, Associated with DNA Hypomethylation on Pericentromeric Satellite Regions during Human Hepatocarcinogenesis. Proc. Natl. Acad. Sci. U. S. A. 99: 10060–10065. [45]. Taberlay, P. C. och Jones, P. A. 2011. DNA Methylation and Cancer. Prog. Drug Res. 67: 1–23. [46]. Neve, R. M., Chin, K., Fridlyand, J., Yeh, J., Baehner, F. L., Fevr, T., Clark, L., Bayani, N., Coppe, J. P., Tong, F., Speed, T., Spellman. P. T., DeVries, S., Lapuk, A., Wang, N. J., Kuo, W. L., Stilwell, J. L., Pinkel, D., Albertson, D. G., Waldman, F. M., McCormick, F., Dickson, R. B., Johnson, M. D., Lippman, M., Ethier, S., Gazdar, A., Gray, J. W. 2006 A collection of breast cancer cell lines for the study of functionally distinct cancer subtypes. Cancer Cell. 10(6):515-27. [47] Shen, C., Gu, M., Liang, D., Miao, L., Hu, L., Zheng, C., Chen, J. 2009. Establishment and characterization of three new human breast cancer cell lines derived from Chinese breast cancer tissues. Cancer Cell Int. 9:2. [48]. Struewing, J. P., Hartge, P., Wacholder, S., Baker, S. M., Berlin, M., McAdams, M., Timmerman, M. M., Brody, L. C., Tucker, M, A. 1997. The Risk of Cancer Associated with Specific Mutations of BRCA1 and BRCA2 among Ashkenazi Jews. N Engl J Med 336:14011408 [49]. Deng, C. X. och Brodie, S. G. 2000. Roles of BRCA1 and its interacting proteins. Bioessays. 22(8):728-37. [50]. Williams, R. S., Green, R., Glover, J. N. 2001. Crystal structure of the BRCT repeat region from the breast cancer-associated protein BRCA1. Nat Struct Biol. 8(10):838-42. [51]. Deng, C. X. 2006. BRCA1: cell cycle checkpoint, genetic instability, DNA damage response and cancer evolution. Nucleic Acids Res.34(5):1416-26. [52]. Scully, R., Chen, J., Ochs, R. L., Keegan, K., Hoekstra, M., Feunteun, J., Livingston, D. M. 1997. Dynamic changes of BRCA1 subnuclear location and phosphorylation state are initiated by DNA damage Cell. 90(3):425-35. [53]. Wu, J., Lu, L. Y., Yu, X. 2010. The role of BRCA1 in DNA damage response. Protein Cell.1(2):117-23. [54]. Nussenzweig A, et al. 2010. 53BP1 Inhibits Homologous Recombination in Brca1Deficient Cells by Blocking Resection of DNA Breaks. Cell DOI 10.1016. 24 [55]. Cerbinskaite, A., Mukhopadhyay, A., Plummer, E. R., Curtin, N. J., Edmondson, R. J. 2012. Defective homologous recombination in human cancers. Cancer Treat Rev.38(2):89100 [56]. Bau, D. T., Fu, Y. P., Chen, S. T., Cheng, T. C., Yu, J. C., Wu, P. E., Shen, C. Y. 2004. Breast cancer risk and the DNA double-strand break end-joining capacity of nonhomologous end-joining genes are affected by BRCA1. Cancer Res.64(14):5013-9. [57]. Zhong, Q., Boyer, T. G., Chen, P. L., Lee, W. H. 2002. Deficient nonhomologous endjoining activity in cell-free extracts from Brca1-null fibroblasts. Cancer Res. 62: 3966-70 [58]. Zhong, Q., Chen, C. F., Chen, P. L., Lee, W. H. 2002. BRCA1 facilitates microhomology-mediated end joining of DNA double strand breaks. J Biol Chem, 277: 28641-7. [59]. Orban, T.I. och Olah, E. 2003 Emerging roles of BRCA1 alternative splicing. Mol Pathol.56(4):191-7. [60]. Speevak, M. D., Young, S. S., Feilotter, H., Ainsworth, P. 2003. Alternatively spliced, truncated human BRCA2 isoforms contain a novel coding exon. Eur J Hum Genet.11(12):951-4. [61]. Pettigrew, C. A., Wayte, N., Wronski, A., Lovelock, P.K., Spurdle, A.B., Brown, M. A. 2008. Colocalisation of predicted exonic splicing enhancers in BRCA2 with reported sequence variants. Breast Cancer Res Treat.110(2):227-34. [62]. Venkitaraman, A. R. 2001. Chromosome stability, DNA recombination and the BRCA2 tumour suppressor. Curr Opin Cell Biol.13(3):338-43. [63]. Narod, S. A. och Foulkes, W. D. 2004. BRCA1 and BRCA2: 1994 and beyond. Nature Reviews Cancer pp. 665-676. [64]. Roy, R., Chun, J., Powell, S. N. 2011. BRCA1 and BRCA2: different roles in a common pathway of genome protection. Nat Rev Cancer. 12(1):68-78. [65]. Alter, B. P. och Kupfer, G. Fanconi Anemia. 2002 [Updated 2011 Nov 3]. In: Pagon, R. A., Bird, T. D., Dolan, C. R., et al., editors. GeneReviews™ [Internet]. Seattle (WA): University of Washington, Seattle; 1993-. [66]. Sy, S. M., Huen, M. S., Chen, J. PALB2 is an integral component of the BRCA complex required for homologous recombination repair. 2009. Proc. Natl Acad. Sci. USA 106:7155– 7160. [67]. Zhang, F., Fan, Q., Ren, K., Andreassen, P. R. 2009. PALB2 functionally connects the breast cancer susceptibility proteins BRCA1 and BRCA2. Mol. Cancer Res. 7:1110–1118. [68]. Zhang, F., Ma, J., Wu, J., Ye, L., Cai, H., Xia, B., Yu, X. 2009. PALB2 links BRCA1 and BRCA2 in the DNA-damage response. Curr. Biol. 19(6):524–529. 25 [69]. Bryant, H. E., Schultz, N., Thomas, H. D., Parker, K. M., Flower, D., Lopez, E., Kyle, S., Meuth, M., Curtin, N. J., Helleday, T. 2005. Specific killing of BRCA2-deficient tumours with inhibitors of poly (ADP-ribose) polymerase. Nature.434:913–917. [70]. Farmer, H., McCabe, N., Lord, C. J., Tutt, A. N., Johnson, D. A., Richardson, T. B., Santarosa, M., Dillon, K. J., Hickson, I., Knights, C., Martin, N. M., Jackson, S. P., Smith, G. C., Ashworth, A. 2005. Targeting the DNA repair defect in BRCA mutant cells as a therapeutic strategy. Nature. 434:917–921. [71]. Bouchard, V. J., Rouleau, M., Poirier, G. G. 2003. PARP-1, a determinant of cell survival in response to DNA damage. Exp Hematol. 31:446–454. [72].Curtin, N. J. 2005. ARP inhibitors for cancer therapy. Expert Rev Mol Med. 7:1–20. [73]. Fong, P. C., Boss, D. S., Yap, T. A., Tutt, A., Wu, P., Mergui-Roelvink, M., Mortimer, P., Swaisland, H., Lau, A., O'Connor, M. J., Ashworth, A., Carmichael, J., Kaye, S. B., Schellens, J. H., de Bono, J. S. 2009. Inhibition of poly(ADP-ribose) polymerase in tumors from BRCA mutation carriers. N Engl J Med. 361(2):123-34. [74]. Bolderson, E., Richard, D. J., Zhou, B. B., Khanna, K. K. 2009. Recent advances in cancer therapy targeting proteins involved in DNA double-strand break repair. Clin Cancer Res.15:6314–6320. [75]. Kaelin, W. G. Jr. 2005. The concept of synthetic lethality in the context of anticancer therapy. Nat Rev Cancer. 5(9):689-98. [76]. Soule, H. D., Vazquez, J., Long, A., Albert, S., Brennan, M. 1973. A human cell line from a pleural effusion derived from a breast carcinoma. Journal of the National Cancer Institute. 51(5): 1409–1416. [77]. Fackenthal, J. D., Cartegni, L., Krainer, A. R., Olopade, O. I. 2002. BRCA2 T2722R is a deleterious allele that causes exon skipping. American Journal of Human Genetics, pp. 625631. [78]. Pettigrew, C. A., Wayte, N., Wronski, A., Lovelock, P. K, Spurdle, A. B., Brown, M. A. 2008. Colocalisation of Predicted Exonic Splicing Enhancers in BRCA2 with Reported Sequence Variants. Breast Cancer Research and Treatment, pp. 227-234. [79]. Neuhausen, S. L. 2000. Founder populations and their uses for breast cancer genetics. Breast Cancer Res. 2(2): 77–81. [80]. Ravindra, T., Lakshmi, N. K., Chaitanya, K., Surender, V., Ahuja, Y. R. 2006. Clinical relevance of alternative splicing. Indian Journal of Human Genetics 12(2). [81]. Kurreck, J. 2003. Antisense technologies- Improvement through chemical modifications. Eur J Biochem 270:1628-44. 26 [82]. Bracco L., Kearsey J. 2003. The relevance of alternative RNA splicing to pharmacogenomics Trends in Biotechnology, 21 (8) , pp. 346-353. [83]. BIC (Breast Cancer Information Core)[Elektronisk]. Tillgänglig: <http://research.nhgri.nih.gov/bic/>. . . . 27