Laborationer för gymnasiet
advertisement

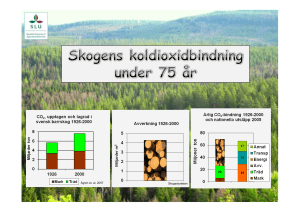
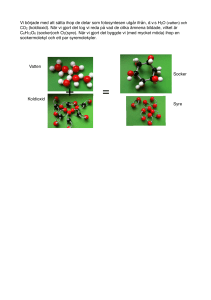
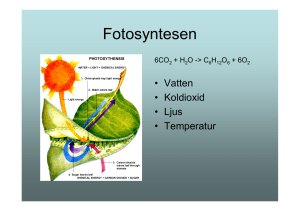
Månadstema Mars: Klimat och Energi Laborationer för gymnasiet Se även laborationer för åk 7-9 Innehåll: Lek och allvar med koldioxid Återvinning av aluminium ur läskedrycksburk Kalorimeter vad är det? kan is brinna eller risker med kaciumkarbid Koppling till kursplaner i Kemi 1: Koppling till kursplaner i Kemi 2: s. 1 s. 1 s. 2 s. 4 s. 5 s. 6 Lek och allvar med koldioxid Teori: Många lärare släcker nog ett ljus med koldioxid för att påvisa att koldioxid är tyngre än luft och förtränger syret. En typ av brandsläckare använder ju koldioxid! Här kommer ett mera lekfullt experiment för er som har tillgång till torris, eller koldioxid på tub. Att tillverka koldioxid från syra och natriumvätekarbonat är svårt, vi lyckades inte. Material: Ett stort glaskärl, såpbubblor och torris eller koldioxid på gastub. Risker: Torris kan ge förfrysningsskador om man tar på den, koldioxid ska inte inandas. En fullständig riskbedömning ges av undervisande lärare Utförande: Om du har torris sätts den i bottnen på kärlet. Låt det stå en liten stund, så kärlet fylls med koldioxid i gasform. Blås en (stor) såpbubbla och försök få den att landa i kärlet! Om den inte berör kärlets kanter kommer den att sväva som en genomskinlig skimrande boll mitt i kärlet en lång stund p.g.a. att bubblan ”vilar” på ett tyngre gaslager, koldioxid! Om du har en gastub måste du släppa ut gasen med svagt tryck (och med lock som skydd mot läckage) för att kärlet skall fyllas. Efter det följer samma procedur som ovan, dvs. du blåser en såpbubbla som skall landa i kärlet. I båda fallen gäller det att inte blåsa in i kärlet, så koldioxiden blåser bort. Små bubblor kan t.o.m. frysa fast i isen, så du får en frusen såpbubbla! P.S. Det går inte att flytta på kärlet för att fånga in bubblan. 1 Återvinning av aluminium ur läskedrycksburk Teori: En aluminiumburk som slängs ut i naturen tar i genomsnitt ca 100 år att brytas ned! Den energimängd som åtgår att återvinna aluminium är 5 % jämfört med vad som krävs för att framställa aluminium ur bauxit. Så nog kan återvinning löna sig. Läs mer om metallåtervinning på http://www.metallkretsen.se/ Material: Bit av läskedrycksburk Kaliumhydroxidlösning, 4 mol/dm3 KOH Svavelsyra-lösning, 9 M H2 SO4 2 stycken 100 cm3 bägare tratt och filtrerpapper glasstav Riskbedömning: Svavelsyra och kaliumhydroxid är starkt frätande. Arbetet görs i dragskåp. Skyddsglasögon och skyddskläder är nödvändiga. En fullständig riskbedömning görs av undervisande lärare. Utförande 1. Skrapa bort målarfärg och inre plastbeläggning från en bit läskedrycksburk 2. Klipp aluminium från burken i små bitar och väg upp ca 0.3 g 3. Placera bitarna i en bägare och häll på 14 cm3 av kaliumhydroxiden. 4. Iaktta förloppet och låt det fortsätta tills gasutvecklingen upphör. Filtrera lösningen 5. Av svavelsyran hälls ca 7 cm3 långsamt och försiktigt på filtratet. Iaktta förloppet. 6. Häll därefter i resten av syran, vad händer nu? 7. Placera blandningen på isbad. Kristallisationen kan underlättas genom skrapning med en glasstav av kärlets insidor. Reaktionslikheter 1. 2 Al (s) + 2 OH-(aq) + 6 H2O (l) 2 Al(OH)-4 (aq) + 3 H2 (g) 2. Al(OH)-4 (aq) + H+ (aq) Al(OH)3 (s) + H2O (l) 3. Al(OH)3 (s) + H+ (aq) Al3+ + 3 H2O (l) 4. K+ + Al3+ + 2 SO42- (aq) + 12 H2O (l) Kal(SO4)2 . 12 H2O (s) Först reagerar aluminium med KOH och bildar ett vattenlösligt tetrahydroxialuminium komplex och vätgas. Det ses som avgående bubblor i lösningen.Vid syratillsats bildas en fällning av aluminiumhydroxid som övergår i lösta Al3+ joner när mera syra tillsätts och hydroxiden först neutraliseras. Nu bildas en klar lösning. För att få alun att falla ut används gärna isbad och skrapning med glasstav. Alun kan t.ex. användas vid rening av vatten och vid konservering. Kalorimeter, vad är det? Bakgrund: Dagligen diskuteras olika bränslen, deras energiinnehåll och klimatpåverkan. Vi ska diskutera frågan med våra elever enligt kursplanerna. Teoretiskt är det ganska lätt att förstå att bränslen kan ha olika energiinnehåll, men hur mäter man det? Kan man dra paralleller till förbränning av mat? Mat är ju bränsle till de kemiska reaktioner som sker i 2 kroppen. Teori: Genom att förbränna bränslen och med erhållen energi värma vatten, kan man jämföra olika bränslens energiinnehåll. Ju större temperaturökning desto större energiinnehåll, under förutsättning att alla övriga parametrar är lika. Förbränningsentalpin kan beräknas med hjälp av vattnets värmekapacitet. Material och utrustning: Bränslen, t.ex. metanol, etanol, propanol eller torkade jordnötter. Kalorimeter: Konservburk isolerad med cellplast (finns att köpa på byggvaruhus), E-kolv (ska exakt passa in i burken), mätglas (eller pipett) porslinsdegel med lock, gem, kork, termometer, muff, klämma, stativring, degeltång och tändstickor. Utförande: Bygg upp anordningen enligt figuren. Se till att man kan föra ned E-kolven i burken mot degeln och den öppna lågan utan problem. Degeln med lock bör stå stadigt, med tillräckligt stort avstånd till burken, så att elden underhålls med syre. Planera hur du antänder bränslet utan att värmeförlusten blir för stor. Bränsle i vätskeform mäts enklast genom att mäta volymen. Hanterbara volymer är 1 cm3. En del av ämnena sotar rejält, utför därför experimentet i dragskåp. Vill man bränna en jordnöt kan den fästas på ett gem, som läggs på degellocket. Väg jordnöten före och efter att du bränt den. Välj en E-kolv med glas som tål upphettning och fyll den med lämplig volym vatten (t.ex.100 cm3). Anteckna utgångstemperaturen, antänd ämnet, för ned E-kolven i burken och låt vattnet värmas upp av bränslet. Vänta tills vattnet nått sin högsta temperatur när lågan har slocknat. För riskbedömningen: Notera R- och S-fraser för respektive bränslen. Ha inte förrådsflaskor med brännbara vätskor nära öppen låga. T.ex. propanol och bensin sotar kraftigt, experimentet bör utföras i dragskåp. Resultat: Vi gjorde en mätserie med 5 olika lösningsmedel (1 cm3 av vardera) och värmde 75 cm3 vatten. Med hjälp av vattnets specifika värmekapacitivitet (4.17 Jg-1 K-1) och temperaturskillnaderna beräknades förebränningsentalpin. Värdena kan jämföras med litteraturvärdena. De uppmätta värdena blir mellan 40-50 % av litteraturvärdena. Vi brände även torkade jordnötter. Det uppmätta värdet blev 60 % av litteraturvärdet, utan hänsyn taget till de produkter som bildats vid förbränningen. Ämne metanol Etanol 1-propanol 2-propanol 1-butanol Jordnöt temperaturhöjning, bränt grader, ämne, g 75 cm3 vatten 0,793 0,789 0,804 0,787 0,81 0,2 25,9 31,7 45,6 41,2 38,8 9,1 förbränningsentalpi, förbränningsentalpi, uppmätt värde uppmätt & litteraturvärde / beräknat värde kJ/mol litteraturvärde kJ/mol -327 -726 0,45 -579 -1367,3 0,42 -1066 -2021 0,53 -984 -2005,8 0,49 -1110 -2675,6 0,41 30,6 1423 kJ/100g 2387,6 kJ/100g Förbränningsentalpi 0 -500 metanol -1000 kJ/mol -1500 -2000 metanol etanol etanol 1-propanol 2-propanol 1-propanol 2-propanol -2500 -3000 1-butanol -3500 1-butanol -4000 litteraturvärden uppmätta värden Till läraren: Beroende på vilka elever som ska utföra experimentet och vilket syftet är, kan man i förväg bestämma vilken noggrannhet man vill ha på resultaten. Vill man jämföra energiinnehållet hos de olika ämnena, utan att utföra några beräkningar, behöver man inte lägga så mycket tid på att isolera burken. Det går alldeles utmärkt att klippa upp en aluminiumburk, som tidigare använts till någon dryck. Metanol och etanol sotar inte och ger bra jämförbara värden. Det kan vara lite svårt att se när metanol brinner med en blå låga, men det blir lättare om man låter ämnet vara på degellocket och inte i degeln. Vi har även testat att bränna bensin, men då bör man hålla till i dragskåp. Bensin sotar väldigt och hanterbar volym är 0,5 cm3. Jordnöten kan vara lite svår att få eld på, använd tändare. Den brinner bara en liten stund. Man väger nöten före och efter förbränningen och bortser från att det bildats ofullständigt förbrända produkter ämnen vid förbränningen. Tänk på att det finns elever som lan vara allergiska mot jordnötter. Att diskutera: Varför uppnår man inte litteraturvärdena? Varför sotar visa ämnen mer än andra? Vad är det svarta som bildas på jordnöten? Kan is brinna? - Eller risker med kalciumkarbid Teori: År 2006 uppstod en brand på SSAB:s stålverk i Luleå. Branden uppstod för att en bult hade släppt från sitt fäste i en cistern innehållande kalciumkarbid. Förlusten av bulten gav upphov till ett centimeterstort hål, varvid omkring tre ton kalciumkarbid läckte ut. Kalciumkarbid används vid svavelrening av råjärn. Karbiden tillsätts i smältan av råjärn, kalcium reagerar med svavel i råjärnet och binds i slagg som sedan kan skrapas av från ytan på smältan. Branden berodde på en reaktion mellan karbid och vatten (eller snarare yrsnö som hade blåst in i byggnaden). Då karbid och vatten reagerar med varandra bildas bl.a. den extremt brandfarliga gasen acetylen (etyn). CaC2 2 H 2O C2 H 2 Ca(OH )2 4 Hur gjorde man för att släcka branden? Vanligtvis använder man torr sand. Snöovädret orsakade inte bara branden utan försvårade även möjligheterna att få tag på torr sand, men efter ett halvt dygn var branden släckt. Nedan följer en beskrivning på en demonstration av brinnande is eller vilka risker som finns med kalciumkarbid. Idén kommer från Chemistry in action No 85 2008. Material: Kalciumkarbid, isbitar, kärl som tål eld. Riskbedömning: Använd små bitar kalciumkarbid. Vid kontakt med vatten bildas extremt brandfarliga gaser. Riskfras 15. Skyddsfraser (2), 8, 43c. Förpackningen förvaras torrt. Vid brandsläckning används pulver eller kvävning. Använd aldrig vatten. Efter reaktion kan bildad kalciumhydroxid spädas och slängas i vasken. Utförande: Placera en liten bit kalciumkarbid i botten på en torr skål. Lägg isbitar ovanpå, krossad underst och hela bitar ovanpå. Vänta några sekunder och tänd sedan den bildade gasen. Acetylen brinner med en sotande låga. Lågan kan kvävas med en brandfilt, lock eller liknande. Man kan göra experimentet mer spektakulärt genom att visa att skålen från början är tom. Sedan lägger man snabbt i en bit kalciumkarbid, utan att någon ser och därefter lägger man i isen. Åskådarna tror att det är isen som brinner! Koppling till kursplaner i Kemi 1: Centralt innehåll: Materia och kemisk bindning Modeller och teorier för materiens uppbyggnad och klassificering. Kemisk bindning och dess inverkan på till exempel förekomst, egenskaper och användningsområden för organiska och oorganiska ämnen. Reaktioner och förändringar Energiomsättningar vid fasomvandlingar och kemiska reaktioner. Stökiometri Tolkning och skrivning av formler för kemiska föreningar och reaktioner. Analytisk kemi Kvalitativa och kvantitativa metoder för kemisk analys, till exempel kromatografi och titrering. Kemins karaktär och arbetssätt Vad som kännetecknar en naturvetenskaplig frågeställning. 5 Modeller och teorier som förenklingar av verkligheten. Hur modeller och teorier kan förändras över tid. Hur problem och frågor avgränsas och studeras med hjälp av kemiska resonemang. Det experimentella arbetets betydelse för att testa, omvärdera och revidera hypoteser, teorier och modeller. Planering och genomförande av experiment samt formulering och prövning av hypoteser i samband med dessa. Utvärdering av resultat och slutsatser genom analys av metodval, arbetsprocess och felkällor. Ställningstagande i samhällsfrågor utifrån kemiska modeller, till exempel frågor om hållbar utveckling. Koppling till kursplaner kemi 2: Centralt innehåll Reaktionshastighet och kemisk jämvikt Reaktionshastighet, till exempel katalysatorers och koncentrationers inverkan på hur fort kemiska reaktioner sker. Resonemang om jämviktssystem i olika miljöer, till exempel jämviktssystem i världshaven, i människokroppen och inom industriella processer. Organisk kemi Reaktionsmekanismer, inklusive kvalitativa resonemang om, hur och varför reaktioner sker och om energiomsättningar vid olika slags organiska reaktioner. Analytisk kemi Kvalitativa och kvantitativa metoder för kemisk analys Resonemang om provtagning, detektionsnivå, riktighet och precision samt systematiska och slumpmässiga felkällor. Kemins karaktär och arbetssätt Modeller och teorier som förenklingar av verkligheten. Modellers och teoriers giltighetsområden och hur de kan utvecklas, generaliseras eller ersättas av andra modeller och teorier över tid. Avgränsning och studier av problem och frågor med hjälp av kemiska resonemang. Det experimentella arbetets betydelse för att testa, omvärdera och revidera hypoteser, teorier och modeller. Planering och genomförande av experimentella undersökningar och observationer samt formulering och prövning av hypoteser i samband med dessa. Utvärdering av resultat och slutsatser genom analys av metodval, arbetsprocess och felkällor. Frågor om etik och hållbar utveckling kopplade till kemins olika arbetssätt och verksamhetsområden. 6