antifibrinolytics art 31(TXA)
advertisement

Bilaga I
Förteckning över läkemedlets namn, läkemedelsform,
styrkor, administreringssätt av läkemedlet samt sökande
och innehavare av godkännande för försäljning i
medlemsstaterna
1
Läkemedel som innehåller tranexamsyra med godkännande för försäljning i den Europeiska Unionen.
Medlemsstat
EU/EES
Innehavare av
godkännande för
försäljning
Läkemedlets namn
Strength
Läkemedelsform
Administreringssätt
AT - Österrike
Pfizer Corporation Austria
GmbH
Floridsdorfer Hauptstraße 1
A-1210 Wien
Austria
Cyklokapron - Ampullen
0,5 g/5 ml
injektionsvätska,
lösning
intravenös injektion
BE - Belgien
PFIZER S.A.N.V.
Bld de la Plaine 17
1050 Brussels
Belgium
Cyklokapron
100 mg/5 ml
injektionsvätska,
lösning
intravenös injektion
BE - Belgien
Eumedica S.A.
Winston Churchilllaan 67
1180 Brussels
Belgium
Exacyl 500
500 mg/5 ml
injektionsvätska,
lösning
intravenös injektion
CY - Cypern
Medochemie Ltd, 1-10
Constantinoupoleos Street,
P.O.Box 51409,
3505 Lemesos, Cyprus
Azeptil injection 500 mg/5 ml
500 mg/5ml
Injektion
intravenös injektion
CY - Cypern
Medochemie Ltd, 1-10
Constantinoupoleos Street,
P.O.Box 51409,
3505 Lemesos, Cyprus
Azeptil Injection 250mg/5ml
250 mg/5 ml
Injektion
intravenös injektion
2
Medlemsstat
EU/EES
Innehavare av
godkännande för
försäljning
Läkemedlets namn
Strength
Läkemedelsform
Administreringssätt
CZ - Tjeckien
Sanofi-Aventis, s.r.o.,
Evropská 846/176a, 160 00
Praha 6, Czech Republic
Exacyl
100 mg/ml
injektionsvätska,
lösning
intravenös injektion
DE - Tyskland
Pharmacia GmbH
Linkstr. 10
D-10785 Berlin
Cyklokapron-Injektionslösung
500mg /5ml
injektionsvätska,
lösning
intravenös injektion
DK - Danmark
Pfizer ApS, Lautrupvang 8,
DK-2750 Ballerup,
Denmark
Tranexamsyre "Pfizer"
100 mg/ml
injektionsvätska,
lösning
intravenös injektion
EL - Grekland
A. Nikolakopoulos A.E.
Galatsiou Avenue 115,
Athens 11146
Transamin
500 mg/5 ml
Injektions infusionsvätska,
lösning
intravenös injektion
3
Medlemsstat
EU/EES
Innehavare av
godkännande för
försäljning
Läkemedlets namn
Strength
Läkemedelsform
Administreringssätt
ES – Spanien
Rottapharm S.L.
Avda. Diagonal 67-69
08019 Barcelona
España
Amchafibrin
500 mg Solución Inyectable
500mg/5 ml
injektionsvätska,
lösning
intravenös injektion
ET - Estland
Pfizer Enterprises SARL
Round-Point du Kirchberg
51, Avenue J.F. Kennedy
L-1855 Luxembourg
Cyklokapron
100mg/ml
injektionsvätska,
lösning
intravenös injektion
FI – Finland
Oy Leiras Finland Ab
Paciuksenkatu 21
PL 1406
00101 Helsinki
Finland
Caprilon
100 mg/ml
injektionsvätska,
lösning
intravenös injektion
FR – Frankrike
Sanofi Aventis France
1-13, bd Romain Rolland
75014 Paris
France
Exacyl 0,5 g/5 ml I.V.,
solution injectable
0,5 g/5 ml
injektionsvätska,
lösning
intravenös injektion
4
Medlemsstat
EU/EES
Innehavare av
godkännande för
försäljning
Läkemedlets namn
Strength
Läkemedelsform
Administreringssätt
HU – Ungern
Sanofi-aventis Zrt.
Tó u. 1-5.
1045 Budapest, Hungary
Exacyl
0,5g/5ml
injektionsvätska,
lösning
intravenös injektion
IE – Irland
Pharmacia Ireland Ltd,
9 Riverwalk, National
Digital Park,
Citywest Business Campus,
Dublin 24
Ireland
Cyklokapron 500mg/5ml
solution for injection or
infusion
100mg/ml
injektionsvätska,
lösning
intravenös injektion
IS - Island
Pfizer ApS, Lautrupvang 8,
DK-2750 Ballerup,
Denmark
Tranexamsyre "Pfizer"
100 mg/ml
injektionsvätska,
lösning
intravenös injektion
IT –Italien
Rottapharm S.p.A.
Via Valosa di Sopra, 9
20052 Monza - Italy
Ugurol
500 mg/5 ml
injektionsvätska,
lösning
intravenös injektion
IT –Italien
Istituto Farmacobiologico
Malesci S.p.A.
Via Lungo l'Ema 7
50015 Bagno a Ripoli
(Firenze)
Italy
Tranex
500 mg/5 ml
injektionsvätska,
lösning
intravenös injektion
5
Medlemsstat
EU/EES
Innehavare av
godkännande för
försäljning
Läkemedlets namn
Strength
Läkemedelsform
Administreringssätt
IT –Italien
Bioindutria Laboratorio
Italiano Medicinali spa
Via De Ambrosiis, 2
15067 Novi Ligure
Alessandria
Italy
Acido tranexamico bioindutria
L.I.M.
500 mg/5 ml
injektionsvätska,
lösning
intravenös injektion
LU Luxemburg
Eumedica SA
67, Avenue Winston
Churchill
B- 1180 Bruxelles
Exacyl
500mg/5ml
injektionsvätska,
lösning
intravenös injektion
LU Luxemburg
Pfizer S.A.N.V.
Bld de la Plaine 17
1050 Brussels
Belgium
Cyklokapron
100 mg/ml
injektionsvätska,
lösning
intravenös injektion
NL –
Nederländerna
Pfizer B.V.
Rivium Westlaan 142
2909 LD, Capelle a/d Ijssel
Cyklokapron, oplossing voor
injectie 100 mg/ml
100 mg/ml
injektionsvätska,
lösning
intravenös injektion
NO – Norge
Pfizer AS
Postboks 3
1324 Lysaker Norway
Cyklokapron
100mg/ml
injektionsvätska,
lösning
intravenös injektion
6
Medlemsstat
EU/EES
Innehavare av
godkännande för
försäljning
Läkemedlets namn
Strength
Läkemedelsform
Administreringssätt
PL – Polen
Warszawskie Zakłady
Farmaceutyczne POLFA
S.A.
22/24 karolkowa st.
01-207 Warsaw, Poland
Exacyl
100 mg/ml
infusionsvätska,
lösning
intravenös injektion
PL – Polen
Sanofi-Aventis France
Boulevard Romain Rolland
1-13, F-75014 Paris, France
Exacyl
100 mg/ml
injektionsvätska,
lösning
intravenös injektion
SE – Sverige
Pfizer AB
191 90 Sollentuna
Sweden
Cyklokapron
100mg/ml
injektionsvätska,
lösning
intravenös injektion
UK Storbritanien
Pharmacia Limited
Walton Oaks, Dorking
Road, Tadworth
Surrey KT20 7NS
United Kingdom
Cyklokapron injection 500
mg/ml
500mg/ml
injektionsvätska,
lösning
intravenös injektion
7
Bilaga II
EMA:s vetenskapliga slutsatser och skäl till ändring av
villkoren för godkännandena för försäljning av läkemedel
som innehåller tranexamsyra
8
Vetenskapliga slutsatser
Övergripande sammanfattning av den vetenskapliga utvärderingen av
hänskjutningsförfarandet för antifibrinolytiska läkemedel
Läkemedel som innehåller tranexamsyra (se bilaga I)
Antifibrinolytiska läkemedel (t.ex. aprotinin, aminokapronsyra och tranexamsyra) är en
hemostatisk klass av läkemedel som används för att förhindra kraftig blodförlust. Aprotinin, som är
en naturligt förekommande polypeptid, hämmar proteolytiska enzym. Det har en bred effekt på
proteolytiska enzym såsom plasmin, trypsin och kallikrein. Lysinanalogerna epsilonaminokapronsyra (EACA, eller aminokapronsyra) och tranexamsyra (TXA) hämmar mer specifikt
omvandlingen av plasminogen till plasmin.
I mars 2010 inledde Tyskland ett hänskjutningsförfarande i enlighet med artikel 31 för att bedöma
nyttan och riskerna med de antifibrinolytiska läkemedlen aprotinin, EACA och TXA vid alla deras
godkända indikationer. Godkännandena för försäljning av aprotinin upphävdes tillfälligt när
farhågor uttrycktes över dess säkerhet i en tidigare granskning år 2007. De preliminära resultaten
av en randomiserad kontrollerad klinisk prövning, ”Blood conservation using antifibrinolytics: a
randomised trial in a cardiac surgery population” (BART-studien), hade visat att användningen av
aprotinin visserligen var förknippad med en mindre allvarlig blödning än något av
jämförelseläkemedlen, men att en ökning hade setts av 30 dagars totaldödlighet bland patienter
som fick aprotinin jämfört med patienter som fick andra läkemedel. Dessa farhågor speglade dem i
vissa publicerade observationsstudier. Godkännandena för försäljning av EACA och TXA påverkades
inte av den första granskningen från 2007.
Flera uppgiftskällor låg bakom kommitténs yttrande, däribland tillgängliga data från kliniska
studier, den publicerade litteraturen, spontana rapporter och andra data som lämnats in av
innehavare av godkännanden för försäljning av läkemedel som innehåller aprotinin, EACA eller
TXA. CHMP:s vetenskapliga rådgivande grupp (SAG) höll ett möte i oktober 2011 och CHMP tog
hänsyn till dess synpunkter inom ramen för denna granskning.
Separata yttranden och slutsatser utfärdades av CHMP för de tre antifibrinolytiska läkemedlen
(aprotinin, EACA och TXA). Detta dokument innehåller slutsatserna om tranexamsyra.
Tranexamsyra
Säkerhetsprofilen för TXA har utvecklats sedan godkännandet för försäljning beviljades, och
säkerhetsdata har samlats under årens lopp. Tromboemboliska händelser, inklusive interaktion
med östrogener, har rapporterats. Akut venös eller arteriell trombos bör utgöra en
kontraindikation. Detsamma gäller för fibrinolytiska tillstånd efter konsumtionskoagulopati, förutom
i de fall där huvudsakligen aktivering av fibrinolytiska system med akut, allvarlig blödning
föreligger. Även hematuri och risken för uretraobstruktion bör inkluderas som varningar. Dessutom
är kramper och synstörningar, bland annat nedsatt färgseende, oönskade händelser som kan vara
allvarliga och har rapporterats, men dessa risker hade inte tagits upp i den gällande godkända
produktinformationen. Tranexamsyra har också förknippats med gastrointestinala biverkningar
såsom illamående, diarré och kräkningar. Allergisk dermatit, kärlsjukdomar såsom sjukdomskänsla
med hypotoni, med eller utan medvetandeförlust och arteriell eller venös trombos samt
överkänslighetsreaktioner, inklusive anafylaxi, har rapporterats. Resultaten av BART-prövningen
hade ingen negativ inverkan på nytta-riskförhållandet för TXA. Tranexamsyra hade inte tidigare
förknippats med någon ökad dödlighetsrisk och denna har förblivit oförändrad efter publiceringen
av BART-studien. CHMP ansåg att information om disseminerad intravasal koagulation,
synrubbningar inräknat nedsatt färgseende, tromboembolism, hematuri och kramper ska speglas
genom varningar och rekommendationer i produktinformationen.
Tranexamsyra är en lysinanalog som har godkänts för flera indikationer sedan 1969. Tillgängliga
data från randomiserade kliniska prövningar och observationsstudier, inklusive metaanalyser, har
beaktats. Utöver hjärtkirurgi fann CHMP att det finns tillräckliga bevis för TXA:s säkerhet och effekt
vid andra indikationer, inräknat hos patienter som genomgår dentala eller kirurgiska ingrepp eller
löper risk för blödningskomplikationer. För vissa tillstånd föreslogs ändrade lydelser för att anpassa
informationen till aktuell vetenskaplig kunskap om användningen av TXA. Mot bakgrund av de
allvarliga begränsningar som identifierats när det gäller effektdata, nya rön som framkommit och
ny medicinsk kunskap som blivit tillgänglig om användning av TXA, och med tanke på
biverkningsprofilen (med vissa allvarliga biverkningar) för TXA, ansåg CHMP att vissa av
indikationerna skulle strykas. En förteckning över de indikationer för vilka CHMP ansåg att nyttariskförhållandet är positivt presenteras nedan.
9
Produktinformationen ändrades för att se till att informationen till hälso- och sjukvårdspersonal och
till patienter är aktuell. Bland annat uppdaterades behandlingsindikationerna för att spegla aktuell
vetenskaplig kunskap om användningen av TXA. Andra ändringar i produktinformationen var att
information om disseminerad intravasal koagulation, synstörningar inräknat nedsatt färgseende,
tromboembolism, hematuri och kramper infördes i form av varningar och rekommendationer.
Hänsyn togs till den senaste kvalitetsgranskningen av dokumentmallar under denna granskning.
Efter att ha beaktat all tillgänglig information om säkerhet och effekt enades kommittén om att
ändra godkännandet för försäljning då nytta-riskförhållandet bedömdes vara positivt i följande
reviderade indikationer för TXA:
Förebyggande och behandling av blödningar till följd av allmän eller lokal fibrinolys hos vuxna och
barn från ett år.
Till specifika indikationer hör
- Blödning orsakad av lokal eller allmän fibrinolys såsom:
- Menorragi och metrorragi,
- Gastrointestinal blödning,
- Hemorragiska urinvägsstörningar, efter prostataoperation eller kirurgiska ingrepp som påverkar
urinvägarna,
- Öron-, näs- och halskirurgi (adenoidektomi, tonsillektomi, tandextraktion),
- Gynekologisk operation eller obstetriska störningar,
- Thorax- och bukkirurgi och andra större kirurgiska ingrepp såsom hjärt- och kärlkirurgi,
- Behandling av blödning till följd av administrering av ett fibrinolytiskt medel.
Detaljerade skäl till omprövning inlämnad av innehavaren av godkännande för
försäljning
En innehavare av godkännande för försäljning av läkemedel innehållande tranexamsyra uttryckte
oenighet med CHMP:s yttrande och inriktade sina skäl till omprövning på följande punkter:
•
Innehavaren av godkännandet för försäljning var inte övertygad om att en säker och
effektiv användning av tranexamsyra intravenöst hos vuxna kräver att ett villkor såsom att utföra
en farmakokinetisk studie med barn uppfylls. Den farmakokinetiska studien hade begärts av CHMP
under hänskjutningsförfarandet enligt artikel 31 avseende antifibrinolytiska läkemedel som
innehåller aprotinin, aminokapronsyra och tranexamsyra.
•
Innehavaren av godkännandet för försäljning meddelade att vissa nyligen genomförda
farmakokinetiska studier med tranexamsyra på den pediatriska populationen skulle ge relevant
information när det gäller barn.
Efter att ha granskat de data som presenterats observerade CHMP att det rörde sig om pågående
farmakokinetiska studier med barn som skulle kunna ge värdefull information. Slutresultaten från
dessa kliniska prövningar bör beaktas innan behov av ytterligare studier rekommenderas. Därför
drog CHMP slutsatsen att ingen farmakokinetisk studie bör begäras som ett villkor vid denna
tidpunkt.
Innehavarna av godkännanden för försäljning erinras om att ny information om användning av TXA
på barn anses värdefull. De pågående studierna bör ge en del relevanta farmakokinetiska data för
olika åldersgrupper och vissa farmakodynamiska data, vilket anses vara av intresse. Innehavarna
av godkännanden för försäljning bör presentera denna information för nationella behöriga
myndigheter när slutresultaten från studierna blir tillgängliga.
10
Skäl till ändring av godkännandena för försäljning av tranexamsyrainnehållande
läkemedel enligt förteckningen i bilaga I
Skälen är följande:
Kommittén beaktade förfarandet enligt artikel 31 i direktiv 2001/83/EG för aprotinin,
aminokapronsyra och tranexamsyra (se bilaga I).
Kommittén beaktade alla data som innehavarna av godkännanden för försäljning lämnat in,
inklusive data från litteraturgranskningar.
Kommittén fann att fynden från randomiserade kliniska prövningar och observationsstudier
stöder användningen av tranexamsyra hos patienter som genomgår dentala eller kirurgiska
ingrepp eller löper risk för blödningskomplikationer.
Kommittén beaktade tillgängliga forskningsdata, inklusive rön från nya studier om TXA:s effekt.
CHMP beaktade även den biverkningsprofil, inklusive nya biverkningar (varav vissa allvarliga),
som är förknippad med TXA.
Mot bakgrund av de allvarliga begränsningar som identifierats när det gäller effektdata, nya rön
som framkommit och ny medicinsk kunskap som blivit tillgänglig om användning av TXA, och
med tanke på biverkningsprofilen (med vissa allvarliga biverkningar) för TXA, ansåg CHMP att
nyttan inte längre uppväger riskerna för vissa av behandlingsindikationerna och att dessa därför
bör strykas.
Kommittén ansåg att produktinformationen borde uppdateras. Bland annat uppdaterades
behandlingsindikationerna för att spegla aktuell vetenskaplig kunskap om användningen av
TXA. Andra ändringar av produktinformationen var att information om disseminerad intravasal
koagulation, synstörningar inräknat nedsatt färgseende, tromboembolism, hematuri och
kramper infördes i form av varningar och rekommendationer.
Därför fann CHMP att nytta-riskförhållandet för tranexamsyra är positivt under normala
användningsbetingelser, under förutsättning att indikationen ändras som följer:
förebyggande och behandling av blödningar till följd av allmän eller lokal fibrinolys hos vuxna och
barn från ett år.
Till specifika indikationer hör
- Blödning orsakad av lokal eller allmän fibrinolys såsom:
- Menorragi och metrorragi,
- Gastrointestinal blödning,
- Hemorragiska urinvägsstörningar, efter prostataoperation eller kirurgiska ingrepp som påverkar
urinvägarna,
- Öron-, näs- och halskirurgi (adenoidektomi, tonsillektomi, tandextraktion),
- Gynekologisk operation eller obstetriska störningar,
- Thorax- och bukkirurgi och andra större kirurgiska ingrepp såsom hjärt- och kärlkirurgi,
- Behandling av blödning till följd av administrering av ett fibrinolytiskt medel.
Mot bakgrund av ovanstående rekommenderade kommittén att villkoren för godkännandet för
försäljning ändras för de tranexamsyrainnehållande läkemedlen i bilaga I, där ändringarna i
produktinformationen återfinns i bilaga III till yttrandet.
Efter att ha övervägt de detaljerade skäl till omprövning som lämnats in skriftligen av innehavaren
av godkännandet för försäljning ansåg CHMP att inga ytterligare villkor behövdes för att säkerställa
en säker och effektiv användning av tranexamsyra.
11
Bilaga III
Produktresumé, märkning och bipacksedel
12
PRODUKTRESUMÉ
OCH BIPACKSEDEL
13
PRODUKTRESUMÉ
14
1.
LÄKEMEDLETS NAMN
Cyklokapron 100 mg/ml injektionsvätska, lösning
[Se bilaga I. - Kompletteras nationellt]
2.
KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
[Se bilaga I. - Kompletteras nationellt]
3.
LÄKEMEDELSFORM
[Kompletteras nationellt]
4.
KLINISKA UPPGIFTER
4.1
Terapeutiska indikationer
Prevention och behandling av blödningar orsakade av generell eller lokal fibrinolys hos vuxna och
barn över 1 år.
Specifika indikationer inkluderar:
- Blödning orsakad av generell eller lokal fibrinolys, t ex:
Menorragi och metrorragi
Gastrointestinal blödning
Blödningstillstånd i urinvägarna i samband med prostataoperation eller kirurgiska
ingrepp som påverkar urinvägarna.
- Öron-, näs-, halsoperation (adenoidektomi, tonsillektomi och tandextraktion).
- Gynekologisk operation eller sjukdomstillstånd med obstetriskt ursprung.
- Torax- och bukoperation samt andra större kirurgiska ingrepp i t ex hjärta/kärl.
- Hantering av blödning orsakad av administrering av ett fibrinolytiskt medel.
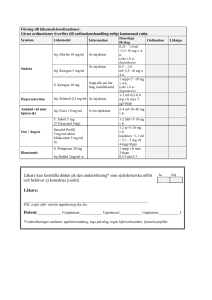
4.2
Dosering och administreringssätt
Dosering
Vuxna
Såvida inte annat förskrivs rekommenderas följande doser:
1.
Standardbehandling av lokal fibrinolys:
0,5 g (1 ampull à 5 ml) till 1 g (1 ampull à 10 ml eller 2 ampuller à 5 ml) tranexamsyra
genom långsam intravenös injektion (= 1 ml/minut) 2-3 gånger dagligen.
2.
Standardbehandling av generell fibrinolys:
1 g (1 ampull à 10 ml eller 2 ampuller à 5 ml) tranexamsyra genom långsam intravenös
injektion (= 1 ml/minut) var 6-8: e timme, motsvarande 15 mg/kg kroppsvikt.
Nedsatt njurfunktion
Vid njursvikt som medför en risk för ackumulering är användning av tranexamsyra kontraindicerat
hos patienter med gravt nedsatt njurfunktion (se avsnitt 4.3). För patienter med milt till måttligt
nedsatt njurfunktion ska dosen av tranexamsyra reduceras med hänsyn till serumkreatininnivån:
Serumkreatinin
μmol/l
120-249
Intravenös dos
Administrering
mg/10 ml
1,35 – 2,82
10 mg/kg kroppsvikt
Var 12:e timme
250-500
> 500
2,82 – 5,65
> 5,65
10 mg/kg kroppsvikt
5 mg/kg kroppsvikt
Var 24:e timme
Var 24:e timme
15
Nedsatt leverfunktion
Ingen dosjustering krävs för patienter med nedsatt leverfunktion.
Pediatrisk population
För nuvarande godkända indikationer som beskrivs i avsnitt 4.1, är dosen för barn från 1 år i
området 20 mg/kg/dag. Uppgifter om effekt, dosering och säkerhet för dessa indikationer är
emellertid begränsade.
Effekt, dosering och säkerhet av tranexamsyra till barn som genomgår hjärtkirurgi har inte
fastställts. Tillgängliga data är begränsade och beskrivs i avsnitt 5.1.
Äldre
Ingen dosreducering behövs, såvida det inte finns tecken på njursvikt.
Administreringssätt
Administreringen måste strikt ske genom långsam intravenös injektion.
4.3
Kontraindikationer
-
Överkänslighet mot den aktiva substansen eller mot något hjälpämne som anges i avsnitt
6.1.
Akut venös eller arteriell trombos (se avsnitt 4.4).
Fibrinolytiska tillstånd efter konsumtionskoagulopati med undantag för de som har en
dominant aktivering av det fibrinolytiska systemet med akut svår blödning (se avsnitt 4.4).
Svårt nedsatt njurfunktion (risk för ackumulation).
Konvulsioner i anamnesen.
Intratekal och intraventrikulär injektion, intracerebral applikation (risk för cerebralt ödem
och konvulsioner).
4.4
Varningar och försiktighet
Indikationerna och administreringssättet ovan ska följas strikt:
Intravenösa injektioner ska ges mycket långsamt.
Tranexamsyra ska inte ges intramuskulärt.
Konvulsioner
Fall av konvulsioner har rapporterats i samband med tranexamsyrabehandling. Vid
kranskärlskirurgi (CABG) rapporterades de flesta fallen efter en intravenös injektion av
tranexamsyra i hög dos. Vid användning av de rekommenderade lägre doserna av tranexamsyra
var förekomsten av postoperativa anfall densamma som hos obehandlade patienter.
Synstörningar
Uppmärksamhet ska riktas mot eventuella synstörningar inklusive nedsatt syn, dimsyn, nedsatt
färgseende och vid behov ska behandlingen sättas ut. Vid kontinuerlig långtidsanvändning av
tranexamsyra injektionsvätska, lösning, är regelbundna oftalmologiska undersökningar
(ögonundersökningar inklusive synskärpa, färgseende, ögonbotten, synfält etc.) indicerade. Vid
patologiska oftalmiska förändringar, i synnerhet sjukdomar i näthinnan, måste läkaren för varje
enskilt fall besluta, i samråd med specialist, om det är nödvändigt att långtidsbehandla med
tranexamsyra injektionsvätska, lösning.
Hematuri
Vid hematuri från de övre urinvägarna, finns det en risk för uretral obstruktion.
Tromboemboliska händelser
Riskfaktorerna för tromboembolisk sjukdom ska beaktas innan tranexamsyra används. Hos
patienter med tromboemboliska sjukdomar i anamnesen eller hos patienter med ökad familjär
förekomst av tromboemboliska händelser (patienter med hög risk för trombofili) ska tranexamsyra
injektionsvätska, lösning endast ges då en stark medicinsk indikation finns, i samråd med en läkare
med erfarenhet inom hemostas och under strikt medicinsk övervakning (se avsnitt 4.3).
Tranexamsyra ska ges med försiktighet till patienter som använder perorala antikonceptionsmedel,
på grund av den ökade risken för blodproppar (se avsnitt 4.5).
Disseminerad intravasal koagulation
Patienter med disseminerad intravasal koagulation (DIC) ska i de flesta fall inte behandlas med
tranxamsyra (se avsnitt 4.3). Om tranexamsyra ges måste det begränsas till de som har en
dominant aktivering i det fibrinolytiska systemet med en akut svår blödning. Den hematologiska
16
profilen karakteriseras ungefär enligt följande: minskad lys-tid för euglobulintromben; förlängd
protrombintid; minskade plasmanivåer av fibrinogen, faktor V och VIII, plasminogen-fibrinolysin
och alfa-2 makroglobulin; normala plasmanivåer av P och P-komplex; dvs. faktor II (protrombin),
VIII och X; ökade plasmanivåer av degenererade fibrinogenprodukter; normalt trombocytantal. Det
som nämns ovan förutsätter att den bakomliggande sjukdomen inte själv ändrar de olika
beståndsdelarna i denna profil. I sådana akuta fall räcker det ofta med en engångsdos om 1 g
tranexamsyra för att få kontroll över blödningen. Administrering av tranexamsyra vid DIC ska
endast övervägas när lämpliga hematologiska laboratoriefaciliteter och kompetens finns tillgängligt.
4.5
Interaktioner med andra läkemedel och övriga interaktioner
Inga interaktionsstudier har genomförts. Samtidig behandling med antikoagulantia måste ske
under strikt övervakning av en läkare med erfarenhet inom detta område.
Läkemedel som påverkar hemostas ska ges med försiktighet till patienter som behandlas med
tranexamsyra. Det finns en teoretisk risk för ökad blodproppsbildning, såsom vid
östrogenbehandling. Alternativt kan läkemedlets antifibrinolytiska effekt motverkas av
trombolytiska läkemedel.
4.6
Fertilitet, graviditet och amning
Fertila kvinnor skall använda effektiv preventivmetod under behandling.
Graviditet
Kliniska data är otillräckliga vad gäller användning av tranexamsyra hos gravida kvinnor. Även om
djurstudier inte tyder på några teratogena effekter rekommenderas inte tranexamsyra under den
första trimestern som en försiktighetsåtgärd.
Begränsade kliniska data om användningen av tranexamsyra vid olika kliniska blödningstillstånd
under andra och tredje trimestern har inte identifierat några skadliga effekter på foster.
Tranexamsyra ska endast användas under graviditet om den förväntade nyttan överväger de
eventuella riskerna.
Amning
Tranexamsyra utsöndras i modersmjölk. Amning rekommenderas därför inte.
Fertilitet
Det finns inga kliniska data om hur tranexamsyra påverkar fertilitet.
4.7
Effekter på förmågan att framföra fordon och använda maskiner
Inga studier har utförts på förmågan att framföra fordon och använda maskiner.
4.8
Biverkningar
De biverkningar som rapporterats från kliniska studier och efter marknadsföring listas nedan enligt
organsystemklass.
Tabell över biverkningar
De rapporterade biverkningarna presenteras i tabellen nedan. Biverkningarna är listade efter
MedDRA organsystemklass. Inom varje organsystem är biverkningarna rangordnade efter
frekvens. Inom varje frekvensgrupp är biverkningarna presenterade efter fallande
allvarlighetsgrad. Frekvenserna är definierade enligt följande: Mycket vanliga (≥1/10), Vanliga
(≥1/100, <1/10), Mindre vanliga (≥1/1 000, <1/100), Ingen känd frekvens (kan inte beräknas
från tillgängliga data).
17
MedDRA
Organsystemklass
Frekvens
Biverkningar
Hud och subkutan vävnad
Mindre vanliga
-Allergisk dermatit
Magtarmkanalen
Vanliga
Centrala och perifera
nervsystemet
Ingen känd frekvens
Ögon
Ingen känd frekvens
-Diarré
-Kräkningar
-Illamående
-Konvulsioner, i synnerhet vid
felaktig användning (se avsnitt
4.3 och 4.4)
-Synstörningar inklusive
nedsatt färgseende
Blodkärl
Ingen känd frekvens
Immunsystemet
Ingen känd frekvens
4.9
-Sjukdomskänsla med
hypotoni, med eller utan
medvetandeförlust (vanligen
följande en alltför snabb
intravenös injektion, sällsynt
efter oral administrering)
- Arteriell eller venös embolism
på något ställe
-Överkänslighetsreaktioner,
inklusive anafylaxi
Överdosering
Inga fall av överdosering har rapporterats.
Tecken och symptom kan inkludera yrsel, huvudvärk, hypotoni och konvulsioner. Det har visats att
konvulsioner tenderar att uppträda i högre frekvens vid ökad dos.
Understödjande behandling bör ges vid överdosering.
5.
FARMAKOLOGISKA EGENSKAPER
5.1
Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: Hemostatika, Fibrinolyshämmande medel
ATC-kod: B02AA02
Tranexamsyra utövar en blödningshämmande effekt på plasmins fibrinolytiska egenskaper.
Plasminogen bildas genom ett komplex där tranexamsyra ingår, tranexamsyra är kopplat till
plasminogen när det omvandlas till plasmin.
Aktiviteten av tranexamsyra-plasmin komplexet på fibrins aktivitet är lägre än aktiviteten från
enbart fritt plasmin.
In vitro-studier har visat att höga doser av tranexamsyra minskar aktiviteten av komplexet.
Pediatrisk population
Hos barn äldre än 1 år:
En litteraturgenomgång identifierade 12 effektstudier för pediatriska hjärtoperationer som
inkluderade totalt 1 073 barn varav 631 hade fått tranexamsyra. De flesta var
placebokontrollerade. Den undersökta populationen var heterogen i fråga om ålder, operationstyp
och doseringsschema. Resultaten från studierna med tranexamsyra tyder på reducerad blodförlust
och reducerat behov av blod vid hjärtoperation på barn, under kardiopulmonal bypass (CPB) där
det finns en hög risk för blödning, särskilt hos cyanotiska patienter eller patienter som genomgår
upprepad operation. Det mest använda doseringsschemat syntes vara enligt följande:
En första bolusdos om 10 mg/kg efter insättandet av anestesi och före hudsnittet.
Kontinuerlig infusion om 10 mg/kg/timme eller injektion i den grundläggande CPB-pumpen
med en dos som anpassats vid CPB-proceduren, antingen med hänsyn till patientens vikt
med en dos om 10 mg/kg eller till grundvolymen i CPB-pumpen, den sista injektionen i slutet
av CPB-doseringen.
Även om studien utfördes på mycket få patienter, tyder de begränsade data som finns på att
kontinuerlig infusion är att föredra, eftersom den terapeutiska plasmakoncentrationen då skulle
upprätthållas under hela operationen.
18
Ingen specifik studie av dos-effekt eller av farmakokinetiken har utförts på barn.
5.2
Farmakokinetiska egenskaper
Absorption
Maximala plasmakoncentrationer av tranexamsyra erhålls snabbt efter en kort intravenös infusion,
varefter plasmakoncentrationerna minskar på ett multiexponentiellt sätt.
Distribution
Plasmaproteinbindning för tranexamsyra är cirka 3 % vid terapeutiska plasmanivåer och tycks helt
förklaras av dess bindning till plasminogen. Tranexamsyra binder inte till serumalbumin. Den
initiala distributionsvolymen är 9-12 liter.
Tranexamsyra passerar placenta. Efter administrering av en intravenös injektion om 10 mg/kg till
12 gravida kvinnor uppgick koncentrationen av tranexamsyra i serum till mellan 10 och 53 μg/ml,
medan den i blod från navelsträngen uppgick till mellan 4 och 31 μg/ml. Tranexamsyra diffunderar
snabbt in i ledvätska och ledhinna. Efter administrering av en intravenös injektion om 10 mg/kg till
17 patienter som genomgick knäoperation liknade koncentrationerna i ledvätskorna de som ses i
motsvarande serumprover. Koncentrationen av tranexamsyra i ett antal andra vävnader är en
bråkdel av den som observerades i blod (bröstmjölk en hundradel, cerebrospinalvätska en tiondel,
kammarvatten en tiondel). Tranexamsyra har upptäckts i sperma där det hämmar den
fibrinolytiska aktiviteten, dock utan att påverka spermamigrationen.
Utsöndring
Utsöndras huvudsakligen som oförändrat läkemedel i urinen. Urinutsöndring via glomerulär
filtration är den huvudsakliga elimineringsvägen. Njurclearance motsvarar plasmaclearance (110116 ml/minut). Utsöndringen av tranexamsyra är cirka 90 % inom de första 24 timmarna efter en
intravenös administrering av 10 mg/kg kroppsvikt. Tranexamsyras elimineringshalveringstid är
cirka 3 timmar.
Speciella populationer
Plasmakoncentrationerna ökar hos patienter med njursvikt.
Ingen specifik farmakokinetisk studie har genomförts på barn.
5.3
Prekliniska säkerhetsuppgifter
Baserat på prekliniska data från konventionella studier av säkerhetsfarmakologi, allmäntoxicitet,
gentoxicitet, karcinogenicitet och reproduktionseffekter visades inga särskilda risker för människa.
Epileptogen aktivitet har observerats hos djur vid intratekal användning av tranexamsyra.
6.
FARMACEUTISKA UPPGIFTER
6.1
Förteckning över hjälpämnen
[Kompletteras nationellt]
6.2
Inkompatibiliteter
[Kompletteras nationellt]
6.3
Hållbarhet
[Kompletteras nationellt]
6.4
Särskilda förvaringsanvisningar
[Kompletteras nationellt]
6.5
Förpackningstyp och innehåll
[Kompletteras nationellt]
6.6
Särskilda anvisningar för destruktion
[Kompletteras nationellt]
19
7.
INNEHAVARE AV GODKÄNNANDE FÖR FÖRSÄLJNING
[Se Annex I – kompletteras nationellt]
8.
NUMMER PÅ GODKÄNNANDE FÖR FÖRSÄLJNING
[Kompletteras nationellt]
9.
DATUM FÖR FÖRSTA GODKÄNNANDE/FÖRNYAT GODKÄNNANDE
Datum för det första godkännandet: DD månad ÅÅÅÅ
Datum för den senaste förnyelsen: DD månad ÅÅÅÅ
[Kompletteras nationellt]
10.
DATUM FÖR ÖVERSYN AV PRODUKTRESUMÉN
MM ÅÅÅÅ
[Kompletteras nationellt]
Ytterligare information om detta läkemedel finns på Europeiska läkemedelsmyndighetens
webbplats http://www.ema.europa.eu/
[Kompletteras nationellt]
20
BIPACKSEDEL
21
BIPACKSEDEL
Bipacksedeln: Information till användaren
Cyklokapron 100 mg/ml injektionsvätska, lösning
tranexamsyra
Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller
information som är viktig för dig.
Spara denna information, du kan behöva läsa den igen.
Om du har ytterligare frågor vänd dig till läkare eller apotekspersonal.
Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem,
även om de uppvisar sjukdomstecken som liknar dina.
Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även eventuella
biverkningar som inte nämns i denna information.
I denna bipacksedel finns information om följande:
1.
2.
3.
4.
5.
6.
Vad Cyklokapron är och vad det används för
Vad du behöver veta innan du tar Cyklokapron
Hur du tar Cyklokapron
Eventuella biverkningar
Hur Cyklokapron ska förvaras
Förpackningens innehåll och övriga upplysningar
1.
Vad Cyklokapron är och vad det används för
Cyklokapron innehåller tranexamsyra, som tillhör en grupp läkemedel som kallas hemostatika;
fibrinolyshämmande medel, aminosyror.
Cyklokapron används hos vuxna och barn över 1 år för att förebygga och behandla blödningar på
grund av fibrinolys, vilket innebär att blodet har svårt att koagulera.
Specifika användningsområden inkluderar:
Kraftiga menstruationer hos kvinnor
Blödning i mage/tarm
Blödningar i urinvägarna efter prostataoperation eller kirurgiska ingrepp som påverkar
urinvägarna
Öron-, näsa- eller halsoperation
Hjärt-/kärloperation, bukoperation eller gynekologisk operation
Blödning efter att du har behandlats med ett annat blodproppshämmande läkemedel.
2.
Vad du behöver veta innan du tar Cyklokapron
Ta inte Cyklokapron
om du är allergisk mot tranexamsyra eller något annat innehållsämne i detta läkemedel
(anges i avsnitt 6)
om du har en sjukdom som gör att du får blodproppar
om du har en sjukdom som kallas för ”konsumtionskoagulopati”, där blodet i hela kroppen
börjar bilda blodproppar
om du har problem med njurarna
om du tidigare har haft kramper.
På grund av risken för ödem i hjärnan och kramper rekommenderas inte användning i hjärnan
(intratekal och intraventrikulär injektion eller intracerebral applikation).
Om du tror att något av ovanstående stämmer in på dig, eller om du tvekar över något, tala med
läkare innan du tar Cyklokapron.
Varningar och försiktighet
Tala om för läkaren om något av nedanstående stämmer in på dig för att hjälpa honom eller henne
att bestämma om Cyklokapron är lämpligt för dig:
22
Om du har haft blod i urinen: Cyklokapron ska inte ges på grund av risken för flödeshinder
i urinröret.
Om du har en ökad risk för att få blodproppar.
Om du har en kraftig koagulering eller blödning i hela kroppen (disseminerad intravaskulär
koagulation) är Cyklokapron kanske inte lämplig för dig, förutom om du har akut allvarlig
blödning och blodprov har visat den process som hämmar blodets förmåga att koagulera
(fibrinolys) har aktiverats.
Om du tidigare har haft kramper ska du inte behandlas med Cyklokapron. Läkaren ska
använda minsta möjliga dos för att undvika kramper vid behandling med Cyklokapron.
Om du står på långtidsbehandling med Cyklokapron ska eventuella förändringar i
färgseendet bevakas, och vid behov ska behandlingen avbrytas.
Vid fortsatt långtidsanvändning av Cyklokapron bör du gå på regelbundna
ögonundersökningar (kontroll av synskärpa, färgseende, ögonbotten, synfält etc.).
Vid ögonförändringar, i synnerhet sjukdomar i näthinnan ska läkaren efter rådgörning med
en specialist besluta om långtidsbehandling med Cyklokapron är nödvändig i ditt fall.
Andra läkemedel och Cyklokapron
Tala om för läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra
läkemedel, även receptfria läkemedel, vitaminer, mineraler, örtmediciner eller bantningspreparat.
Tala i synnerhet om för läkaren om du tar:
andra läkemedel för att få blodet att koagulera, så kallade antifibrinolytiska medel
läkemedel som förhindrar blodproppsbildning, så kallade trombolytiska läkemedel
p-piller.
Graviditet och amning
Om du är gravid eller ammar, rådfråga läkare eller apotekspersonal innan du tar Cyklokapron.
Tranexamsyra utsöndras i bröstmjölk. Användning av Cyklokapron under amning rekommenderas
därför inte.
Körförmåga och användning av maskiner
Inga studier har utförts på förmågan att köra bil eller använda maskiner.
3.
Hur du tar Cyklokapron
Användning för vuxna
Cyklokapron kommer att ges till dig genom en långsam injektion i ett blodkärl. Läkaren bestämmer
vilken dos som passar för dig och hur länge du ska behandlas.
Användning för barn
Till barn från 1 år baseras dosen på barnets vikt. Läkaren bestämmer vilken dos som passar och
hur länge barnet ska behandlas.
Användning för äldre
Ingen dosreducering behövs, såvida det inte finns tecken på njursvikt.
Användningar för patienter med nedsatt njurfunktion
Vid nedsatt njurfunktion kommer dosen av tranexamsyra minskas med hänsyn till ett blodprov
(serumkreatininvärdet).
Användning för patienter med nedsatt leverfunktion
Ingen dosreducering behövs.
Administreringssätt
Cyklokapron ska endast injiceras långsamt i ett blodkärl.
Cyklokapron får inte injiceras i en muskel.
Om du har tagit för stor mängd av Cyklokapron
Om du får mer Cyklokapron än du ska kan du få ett övergående blodtrycksfall. Tala omedelbart
med läkare eller apotekspersonal.
4.
Eventuella biverkningar
23
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte
få dem.
Vanliga (kan drabba upp till 1 av 10 användare)
besvär i mage/tarm (illamående, kräkningar, diarré)
Mindre vanliga (kan drabba upp till 1 till 10 av 1000 användare)
Påverkan på huden: utslag
Ingen känd frekvens (frekvensen kan inte beräknas från tillgängliga data)
Sjukdomskänsla med lågt blodtryck, särskilt om injektionen har givits för snabbt
Blodproppar
Påverkan på nervsystemet: kramper
Påverkan på ögonen: synförändringar inklusive försämrat färgseende
Påverkan på immunsystemet: allergiska reaktioner
Om några biverkningar blir värre eller om du märker några biverkningar som inte nämns i denna
information, kontakta läkare eller apotekspersonal.
5.
Hur Cyklokapron ska förvaras
[Kompletteras nationellt]
6.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
[Kompletteras nationellt]
Läkemedlets utseende och förpackningsstorlekar
[Kompletteras nationellt]
Innehavare av godkännande för försäljning och tillverkare
[Se bilaga I. - Kompletteras nationellt]
{Namn och adress}
<{tfn}>
<{fax}>
<{e-post}
Denna bipacksedel ändrades senast
[Kompletteras nationellt]
24