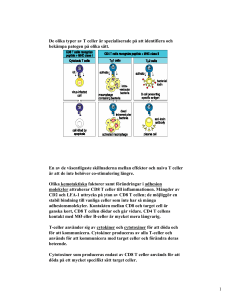
Analysis of CD4+ and CD8+ T-lymphocytes
advertisement

UPPSALA UNIVERSITET Examensarbete 10 poäng C-nivå Vt. 2006 Institutionen för medicinsk biokemi och mikrobiologi Biomedicinska analytikerprogrammet Analysis of CD4+ and CD8+ T-lymphocytes A comparison between EPICS XL and Celldyn Sapphire Haleh Yazdan Panah Handledare: Lena Douhan Håkansson, Anders Larsson Akademiska laboratoriet, klinisk kemi och farmakologi 1 ABSTRACT Flowcytometric technology has been widely used for measurement of the absolute numbers of T-lymphocytes subsets in Human Immunodeficiency virus (HIV), defining the disease state, monitoring antiviral treatment, and identifying any risk for opportunistic infections. A manual preparing of the samples is required. More recently an automated and enclosed blood cell counting, Celldyn Sapphire has been introduced. In this study the performance of the Flow cytometer EPICS XL as a reference method for analysis of CD3+, CD4+ and CD8 T-lymphocytes was evaluated with blood from 40 individual’s samples. EPICS XL was also compared with Celldyn Sapphire in the analysis of T-lymphocyte subsets in 39 blood samples from patients with low, high and normal lymphocyte counts. The result showed that the precision was high for both EPICS XL (<2.5%) and Celldyn (<10%). The method was linear over a wide range. Comparisons of CD3+, CD4+, and CD8+ T-lymphocytes analysis showed high coefficients of correlation (r>0.9) and agreement (y>0.9x) between two instruments. A lower degree of agreement was observed at low concentration of CD3+ and CD4+ T-lymphocytes (0.757, 0.739). This means that cell counts obtained by Celldyn were ∼30% lower than those obtained with EPICS XL. This study shows that both EPICS XL and Celldyn Sapphire were suitable for CD4+ and CD8+ T cell counts. It is however preferable to use Flowcytometry for counting of low concentration of CD4+ T-lymphocytes (<200 cells/µL). Key words: EPICS XL, Celldyn Sapphire, Human immunodeficiency virus (HIV), flowcytometry, Celldyn 4000 2 INTRODUKTION Immunsystemet består av många olika celler, proteiner och lymfatiska organ, som verkar tillsammans för att skydda vår kropp mot patogena mikroorganismer. De viktigaste cellerna i immunsystemet är leukocyter (5-10 x 10⁶ celler/mL). Leukocyterna består av lymfocyter (2025%), monocyter (3-8%) och granulocyter (neutrofila 60-70%, eosinofila 2-4% och basofila 0,5-1,0 %). Lymfocyterna kan i sin tur delas in i B-lymfocyter (B-celler), T-lymfocyter (Tceller) och NK-celler. B-lymfocyter har förmåga att bilda plasmaceller som tillverkar och utsöndrar stora mängder antikroppar mot kroppsfrämmande ämnen. NK-cellerna har en cytotoxisk funktion. T-lymfocyterna består till större delen av två subpopulationer : T-hjälparceller (Thlymfocyter) som har CD4- molekyler på sin yta och cytotoxiska T-celler (Tc-lymfocyter, Tsupressor) som har CD8 molekyler på sin yta. Tc-lymfocyter aktiveras framförallt vid virusinfektioner och har som funktion att avdöda infekterade kroppsegna celler som presenteras på MHCI molekyler. Th-lymfocyterna känner igen kroppsfrämmande peptider som presenteras på MHCII molekyler hos APC (Antigenpresenterande Celler) och har som huvudfunktion att producera cytokiner, som B-cellen också behöver för att aktiveras. Mogna lymfocyter av B-respektive T-typ karaktäriseras av specifika glykoproteiner på cellytan, vilka är viktiga för lymfocyternas funktion. Sådana antigen benämns cluster of differentitation (CD). Alla leukocyter har CD45 på sin yta. T-lymfocyter igenkänns genom att de är CD3 positiva. Th- lymfocyter uttrycker CD3 och CD4 antigen (CD3/CD4 positiva), medan cytotoxiska T-celler uttrycker CD3 och CD8 antigen (CD3/CD8 positiva). I blodet har man normalt cirka dubbelt så många CD4+ som CD8+ T-lymfocyter. CD4/ CD8 relationen kan således beskriva mängdförhållandet i blodet mellan hjälpar-celler och cytotoxiska Tlymfocyter. Summan av CD8+ och CD4+ skall bli lika med, eller strax under, totala CD3+ Tlymfocyter. I en studie utförd på vuxna kaukasier i USA har rapporterats att lymfocytpopulationer består av 61-85% CD3, 28-58% CD4 och 19-48% CD8 [1]. Ungefär likadana siffror har rapporterats i Storbritannien och Indien [2,3]. Vid många olika typer av sjukdomar är kvantifiering av lymfocyter- och lymfocytsubpopulationer viktiga som till exempel immunologiska anomalier (Hyper-IgM syndrom), lymfoproliferativa sjukdomar (leukemier) och immunologiska sjukdomar (HIV och AIDS). 3 Sedan 1981 då de första fallen av sjukdomen AIDS beskrevs, har HIV infektion (Human Immunodeficiency Virus) spridits i många länder i världen. HIV infektioner är idag ett stort globalt problem. United Nations Program on AIDS (UNAIDS) beräknar att idag lever cirka 40 miljoner människor i världen med HIV och infektionen orsakar årligen tre miljoner dödsfall. Omkring 70 procent av de infekterade bor i Afrika söder om Sahara och i Asien. Situationen kommer att bli värre om tio år med troligen 100 miljoner infekterade människor i hela värden om man inte satsar mer på effektiva förebyggande åtgärder [4]. Enligt Läkemedelsverkets hemsida rapporterades i Sverige sammanlagt 6703 HIV-infekterade patienter t.o.m. december 2004. Av dessa hade 1981 patienter insjuknat i AIDS och 1285 avlidit, men det verkliga antalet avlidna är troligen högre. Uppskattningsvis kontrolleras cirka 3500 personer vid hiv-kliniker i Sverige idag och av dessa står cirka 2/3 på antiretroviral behandling. HIV är ett retrovirus som infekterar framförallt Th-lymfocyter (CD4+) och vissa makrofager (en del är CD4+). Detta virus förstör inte bara CD4 celler, utan infekterar andra celler i immunsystemet [5]. Primär infektion med HIV är troligen symptomfri i de flesta fall men ger ibland influensaliknande symptom. Infektionen ger upphov till stora mängder viruspartiklar i perifert blod och en markant sänkning av CD4+ T-celler inom 2-6 veckor. Samtidigt sker en ökning av CD8+ T-celler som dödar virusinfekterade celler och B-cellerna börjar producera antikroppar mot viruset. Tc-celler anses viktiga för att kontrollera virusnivåerna. Cellkoncentrationen når ett max inom några veckor och minskar sedan. De CD4+ T-cellerna ökar så småningom igen till en ungefärlig koncentration på 700-800 celler per µL (700-800 x 10⁶/L), mot normala 1,000 celler per µL (1,000 x 10⁶/L) för att sedan sakta sjunka, under i medeltal en period av 10 år. Under den här tiden när infektionen är latent, behöver sjukdomens progress monitoreras var tredje till sjätte månad [6]. Under denna period reproducerar viruset sig och CD4+ Th-cellerna minskar i antal. Tidiga symptom förekommer när CD4+ T-lymfocyter sjunker till 500 celler per µL (500 x 10⁶/L). Till slut, efter 2 till 15 år, har patienten en mycket låg koncentration av CD4+ T-celler och drabbas ofta av opportunistiska infektioner. När antalet CD4+ T- celler sjunker till 200 celler per µL (200 x 10⁶/L) utvecklas sjukdomen AIDS [6]. Undantaget utgörs av personer som verkligen är ”long -term nonprogressors”, d.v.s. personer som inte progredierar i sin hivinfektion. CD4cellsnivån ger ett mått på graden av immundefekt och är den viktigaste markören för risken att utveckla opportunistisk infektioner. CD4-cellsnivån avgör därför om antiretroviral terapi bör påbörjas. När antalet CD4 T-celler är 200-350 celler per µL, påbörjas antiviralbehandling 4 beroende på hastigheten med vilken CD4 nivån faller samt patientens beredskap och önskemål. När antalet CD4 T-celler sjunker till under 200 celler per µL samt för patienter som visar symtom tidigare och gravida kvinnor rekommenderas alltid antiviralbehandling [7]. CD4-cellsnivåer används som komplement till hiv-1 RNA kvantifieringen för att monitorera effekten av antiretroviral terapi [6]. Eftersom nivån av CD4-celler kan påverkas av tidpunkt på dygnet, fysisk och psykisk stress, etc. bör standardisering av provtagningsförhållanden eftersträvas. För att övervaka hur sjukdomsutvecklingen fortskrider använder man sig av olika prognostiska markörer. Celltypning sker generellt genom detektion och analys av ytcellsmarkörer d.v.s. CD-molekyler. Analysen sker normalt genom immunofluorescence eller immunocytokemi och flödescytometri. Immunocytokemiska och immunofluorescence metoder möjliggör visualisering av celler och dess morfologi, men ger litet antal analyserade celler och subjektiva tolkningar av preparatet, vilket ger ett större metodfel än vid flödescytometri, där ett stort antal celler kan räknas på kort tid. Flödescytometrisk teknik används idag för att göra en kvantitativ och kvalitativ mätning av lymfocyter. Rutinanalyserna för att övervaka HIV patienters sjukdomsförlopp är att bestämma koncentrationen av T-lymfocyter (CD3 positiva), T- hjälpar celler (CD4 positiva) och koncentrationen av cytotoxiska T-celler (CD8 positiva). Tekniken som traditionellt används vid flödescytometri är manuell preparation av prover vilket inkluderar pipettering, inkubering av prover med antikroppar, hemolys, tvättning och fixering av prover. Tiden som behövs för preparering är runt en timme. Metoden bygger på analys av celler i suspension. Dessa får passera förbi en laserstråle. När cellerna belyses kommer de att sprida ljuset i olika riktningar. Det ljus som sprids framåt kallas "forward scatter" och är ett mått på cellens storlek. Det ljus som sprids i 90 graders vinkel kallas "side scatter" och återspeglar cellens granularitet. För att studera de antigen och de antigenkombinationer som finns på cellytan hos olika celler används antikroppar mot respektive antigen. Dessa antikroppar har till sig kopplade en fluorokrom d.v.s. ett ämne som tar emot energi vid belysning med en viss våglängd och som avger denna genom att sända ut ljus av en annan våglängd än det infallande. Det utsända ljuset kan sedan mätas av flödescytometern. Genom att koppla olika fluorokromer till olika antikroppar kan förekomst av olika antigen på samma cell studeras. De nya flödescytometrarna kan analysera minst fyra färger samtidigt. Detta ger mer information vid varje analys och leder till mer rationell hantering och minskar behovet av provvolym. Det ger också utökade möjligheter att studera fler parametrar per cell och nya undergrupper av celler. Ett problem vid kliniska undersökningar med flödescytometer är att preparering av prover 5 innan flödescytometri kräver öppna blodrör vilket ökar risken för att sprida smittämnen. Nyligen presenterades en teknik för analys av T-celler som inte kräver någon kontakt med innehållet i röret. Företaget ”Abbot Laboratories” har utvecklat en snabbare och insluten teknik för att kvantifiera CD4+ och CD8+ T-lymfocyter. Celldyn Sapphire (CD Sapphire; Abbott Laboratories, CA, USA) är en helautomatisk cellräknare som kan användas för immunologisk mätning av T-lymfocyter och tillhörande subtyper av T-celler och är avsedd för diagnostisk användning i kliniska laboratorier på sjukhus, vårdcentraler, referens- och forskningslaboratorier. Tekniken bygger liksom flödescytometern på monoklonala antikroppar som är fästa till ett fluorescerande färgämne med kovalent bindning vilket avger färg vid belysningen med laserljus av specifik våglängd. T-cell analysen använder också ljusspridningsteknik. Mätningar av ljusförlusten vid 0˚ och ljusspridning vid 7˚ används vid beräkning tillsammans med fluorescensmätningar från tre fluorescenskanaler FL1, FL2 och FL3 (8). Resultaten används för att identifiera och räkna T-celler, T-hjälparceller och Tcytotoxiska celler bland andra celler och cellfragment i provet. Syftet med denna studie var att först sätta upp en metod för fenotypning av humana leukocyter med flödescytometer, EPICS XL-MCL från Beckman Coulter. Blod från friska blodgivare med normal leukocyt koncentration fenotypades för att bestämma referensvärden för analysen samt få en uppfattning om spridning i instrumenten och metodvariation baserade på instrumentet resp. manuella moment. Även ljuskänslighet och hållbarheten av blodproverna i rumstemperatur undersöktes. Sedan utfördes fenotypning av blod från patienter med varierande låg, hög och normal leukocytkoncentration med både flödescytometer och Celldyn Sapphire med syftet att jämföra immunfenotypnings- resultaten mellan de två instrumenten. Analysen går ut på att beräkna kvoten av CD4 positiva/CD8 positiva celler och koncentrationen av T-lymfocyter som är CD4- respektive CD8-positiva. MATERIAL OCH METODER Provmaterial Provmaterialet utgjordes av ocentrifugerat helblod i 5mL vakuumrör, med tillsats av EDTA (ethylendiamintetraaceticacid), som togs venöst från 45 blodgivare från blodcentralen på Akademiska sjukhuset. Dessa prover hade normala koncentrationer av leukocyter och lymfocyter. Dessutom analyserades 39 prover från patienter med normala, höga och låga koncentrationer av leukocyter som tidigare hade analyserats med avseende på cellantal vid 6 avdelningen för Klinisk Kemi på Akademiska sjukhuset. Provvolymen var minst 1mL och blodet förvarades max 24 timmar i rumstemperatur. Analytiska metoder Proverna från friska blodgivare analyserades i en flödescytometer, EPICS XL-MCL från Beckman Coulter Inc. (USA, CA), med hjälp av mjukvaran Expo 32 software (www.beckmancoulter.com) som styr instrumentet och lagrar erhållna data. Proverna från patienter analyserades både med flödescytometern och med en helautomatisk cellräknare vid avdelningen för klinisk kemi, Celldyn Sapphire, med hjälp av applikationen immuno T-cell (CD3/4/8) Assay. Analyserna utfördes på Akademiska sjukhuset. Reagens och kemikalier till flödescytometer Vid analys med flödescytometern, användes ett kit från Beckman Coulter Inc. som innehåller en antikroppslösning, Flow Count Flourospheres, Optilyse, Coulter Isoton II Diluent och Coulter Clenz (tvätt lösning). För tvättning av flödescytometern användes Hypoklorit 1% och avjoniserat vatten. Preparering av prover för flödescytometri Före prepareringen kontrollerades koncentrationer av leukocyter i varje prov. Koncentrationen skall inte vara mer än 10 x 10⁹/L. Prover med hög koncentration (>10 x 10⁹/L) av leukocyter späddes 1:2. För spädningen tillsattes 500µL Isoton II till 500µL blod i ett nytt provrör. Proverna preparerades enligt beskrivningen i kittet från Beckman Coulter Inc. i mörker för att fluorescensen inte skulle avta. Alla inkuberingar utfördes i rumstemperatur. Vid prepareringen av proverna pipetterades 10µL av antikroppslösningen i nya provrör. Sedan tillsattes 100µL blod till antikropparna och proverna blandades väl. Rören inkuberades mörkt i 15 min. För att lysera blodkropparna och fixera cellmembranen tillsattes 500µL Optilyse. Efter 15 min inkubering i mörker, tillsattes 500µL Isoton II och proverna fick stå mörkt i ytterligare 15 min. Slutligen tillsattes 100µL välblandad Flow Count, fluorescerande plastkulor. Eftersom koncentration av celler mäts, är det mycket viktigt att ta samma mängd blod och Flow Count. Därför användes en ny pipettspets inför varje pipettering och spetsen torkades av före tillsats. 7 Analys med flödescytometer Den aktuella flödescytometern kunde mäta fluorescens vid fyra olika våglängder, vilket medgav bestämningar av fyra olika markörer per cell. Kittet som användes vid analysen innehöll antikroppar med fyra olika fluorescenserande färger, anti CD45-FITC (fluoresceinisotiocyanat), anti CD4-RDI (phykoerytrin, PE ), anti CD8-ECD (PE-Texas Red) och anti CD3- PC5 (PE-Cyanin). När de exciteras vid 488 nm uppvisar de fyra färgämnena fluorescenstoppar vid våglängderna 520 nm för FITC, 575 nm för PE, 615 nm för ECD och 670 nm för PC5 i de fyra optiska kanalerna FL1, FL2, FL3 och FL4. Ljusspridningen och fluorescensparametrarna hos flödescytometern standardiserades med två kontroller, Flow-Check och Flow-Set, för att erhålla optimala instrumentprestanda. Flow-Check består av partiklar inmärkta med stabil fluorescensintensitet som används för kontroll av laserstrålens inställning och korrekt flöde i flödescellen. Med Flow Check Fluorospheres kontrolleras HPCV (Half Peak Coefficient of Variation) värdena för ”forward scatter” och fluorescens 1-4, vilka bör vara mindre än 2,0 (HPCV<2). Flow-Set är en lösning med fluorescerande partiklar som används för inställning av flödescytometern. Flow-Set har en stabil fluorescensintensitet. Reagensens stabilitet tillåter standardisering av ljusspridningen medan fluorescensintensiteten tillåter en inställning för kvantitativ och kvalitativ analys av leukocyter. Med Flow Set kontrolleras att medelfluorescensvärdena (mean fluorescense intensity) för alla 4 fyra fluorescensfärgerna, d.v.s. FL1, FL2, FL3 och FL4, är stabila över tiden. Om värdet inte stämmer överens med tidigare analyser justeras spänningen. Inställning av färgkompensationer utfördes med hjälp av Quick Comp 4 kit (Beckman Coulter) och programvaran EXPO 32 ADC. EPICS använder Forward och Side Scatter för att skilja på lymfocyter, monocyter och granulocyter. Vid analyser av CD4- och CD8-positiva lymfocyter utnyttjas CD45 för att skilja lymfocyterna från andra celler och partiklar och CD3 för att identifiera T-lymfocyter. Thjälparceller identifieras som CD3/CD4-positiva celler och T-suppressor /cytotoxiska celler som CD3/CD8 positiva celler (Figur 1). Koncentrationen av CD3/CD4 och CD3/CD8 positiva celler, lymfocyter och monocyter beräknas av programvaran EXPO 32 med hjälp av Flow Count partiklarna. 8 FL1 Log/SS Lin FL1 Log/SS Lin A SSC FSC granulocyter monocyter lymfocyter CD45 FITC SSC FL2 Log/FL4 Log FL3 Log/FL4 Log B C CD3+ CD3+ CD/4+ CD3+ CD8+ CD3 PC5 CD3 PC5 CD3+ neg neg CD4+ CD4 RD1 CD8+ CD8 ECD Figur 1: Analys av T-lymfocyter med flödescytometrn EPICS-XL. (A) Scatterbilden visar 90°scatter, side scatter, på x-axeln (cellens granularitet) och 0°scatter, forward scatter, på yaxeln (cellenstorlek). (B) Scatter bilden visar side scatter på x-axeln och CD45 FITC fluorescens på y-axeln. Lymfocyt populationen är inringade i figuren. (C) Scatterbilden visar CD4 RDI fluorescens på x-axeln och CD3 PC5 fluorescens på y-axeln. Alla celler i övre vänstra kvadraten är CD3 positiva T-lymfocyter. T-lymfocyter som är både CD3 och CD4 positiva ligger i övre högra kvadraten. Celler i nedre vänstra kvadraten är CD3 och CD4 negativa lymfocyter. Celler i nedre högra kvadraten är CD4 positiva CD3 negativa lymfocyter. (D) Scatterbilden visar CD8 ECD fluorescens på x-axeln och CD3 PC5 fluorescens på y-axeln. Alla celler i övre vänstra kvadraten är CD3 positiva T-lymfocyter. Tlymfocyter som är både CD3 och CD8 positiva ligger i övre högra kvadraten. Celler i nedre 9 vänstra kvadraten är CD3 och CD4 negativa lymfocyter. Celler i nedre högra kvadraten är CD8 positiva CD3 negativa lymfocyter. Celldyn Sapphire Ett antal blodprover från patienter med normala, höga och låga koncentrationer av lymfocyter analyserades både med flödescytometern EPICS XL och cellräknaren Celldyn Sapphire. Två reagenser används vid T-cellsanalysen i cellräknaren, CD 3/4 reagenset för att mäta koncentrationen av CD4 positiva lymfocyter och CD 3/8 reagenset för att mäta koncentrationen av CD8 positiva lymfocyter. Huvudkomponenterna i dessa reagenser är monoklonala antikroppar, som betecknas anti-CD3, anti CD4 och anti-CD8. Ett fluorescerande färgämne är bundet till varje monoklonal antikropp. Färgämnena i Tcellsanalysen är FITC och PE. I båda reagensen är FITC bundet till anti- CD3. I CD3/4 reagens är PE bundet till CD4 och i CD3/8 reagens är PE bundet till anti-CD8. När de exciteras vid 488 nm uppvisar de två färgämnena fluorescenstoppar vid våglängder 530 nm för FITC och 570 nm för PE. I celldyn används tre optiska system. Det första optiska systemet, FL1, används för att mäta FITC fluorescens och andra optiska systemet, FL2, används för mättning av PE fluorescens. Det tredje optiska systemet FL3 används för att mäta Propidium Iodid (PI) fluorescens för bedömning av lymfocyternas viabilitet. Lymfocyter med FL3- fluorescens under en viss nivå anses vara viabla. Detta beror på att PI inte kan passera ett viabelt cellmembran, och därför används för att skilja levande celler från döda eller döende celler. Om det finns för många döda celler i ett prov, flyttas cellpopulationen till höger i FL3bilden vilket kommenteras med att provet är för gammalt och inte godkänt för analys. De monoklonala antikropparna har frystorkats till en pellet och placerats i ett standardrör. En avgränsare av rostfritt stål håller pelleten på plats på provrörets botten. Rören med CD3/4 reagens har orange propp och rören med CD3/8 reagens har grön propp. Blodprov i rör med EDTA tillsats placerades i en rack. Bakom detta i samma rack sattes ett orange respektive ett grönproppat rör ur immuno T-cell förpackningen. Instrumentet aspirerade blod och spädningsvätska till varje rör och sedan injicerades spädningen till den optiska flödescellen för mätning av leukocyter. Resultatet gick ut på att räkna antal T-lymfocyter som är CD4 och CD8 positiva samt kvoten mellan CD4 och CD8 T-lymfocyter (Figur 2). 10 Figur 2: Analys av T-lymfocyter med Celldyn Sapphire. (A) Scatterbilden visar 7°scatter på x-axeln (cellens granularitet) och 0°scatter på y-axeln (cellstorlek). (B) Scatterbilden visar CD4 (FL2) fluorescens på x-axeln och CD3 (FL1) fluorescens på y-axeln. Alla celler som ligger över den horisontella linjen är T-lymfocyter. Den vertikala linjen är gränsen mellan CD4-positiva T-lymfocyter (övre höger kvadrant) och CD4-negativa T-lymfocyter (övre vänster kvadrant). Populationen i nedre vänstra kvadranten består av alla vita blod celler exklusive T-lymfocyterna. (C) Scatterbilden visar CD8 (FL 2) fluorescens på x-axeln och CD3 (FL1) fluorescens på y-axeln. Alla celler över den horisontella linjen är T- lymfocyter. Den vertikala linjen är gränsen mellan CD8-positiva T-lymfocyter (övre höger kvadrant) och CD8-negativa T-lymfocyter (övre vänster kvadrant) [11]. Referensvärden för CD3+, CD4+ och CD8+ T-lymfocyter från Abbott diagnostik visas i Tabell 1. 11 Tabell 1: Bakgrundsgränsvärden för T- celler Referensvärden Lymfocyter 0,7-3,9 x 10(9)/L CD3 5,6- 2 x 10(9)/L CD4 0,35-1,35 X 10(9)/L CD8 0,15- 0,83X 10(9)/L CD4/CD8 normalt ca 2, men stora variationer kan förekomma. Dataanalys och statistik För statistiska beräkningar användes programmet Microsoft Excel (Portland, Oregan, USA). För att beräkna spridning i referensgruppen, friska blodgivare (n=40) användes standardavvikelsen. Dessutom uträknades medelvärdet, median, maximum och minimum. Vid jämförelse av resultat från patientprover (n=39) som analyserades med både EPICS XL och Celldyn Sapphire, bestämdes korrelationskoefficienten, linjens lutning och skärningspunkten i x- axeln med hjälp av programmet Sigma Plot (SPSS Inc, Chicago, Illinois, USA). RESULTAT Referensmaterial- EPICS XL Koncentrationen av CD3+, CD4+ och CD8+ T-lymfocyter som analyserades i blod hos 40 friska vuxna blodgivare med normal leukocytkoncentration med hjälp av EPICS XL framgår av Tabell 2. Tabell 2: Koncentrationen av CD3+, CD4+, och CD8+ T-lymfocyter analyserade med EPICS XL [celler x 10⁹/L] hos 40 blodgivare. Medelvärdet ± SD (x 10(9)/L Lymfocyter CD3+ CD3/4 + CD3/8 + CD4 /CD8 Min-Max (x 10(9)/L) 1,6 ± 0,4 1,1±0,3 0,7± 0,2 0,4 ± 0,1 2,1 ± 0,8 0,8 – 3,9 0,6 – 2,5 0,4 – 1,7 0,1 – 0,7 1,0 – 6,6 12 Jämförelsen mellan Celldyn Saphhire och EPICS XL Koncentrationen av CD3+, CD4+ och CD8+ T-celler analyserades i 39 patientprover från Klinisk Kemi med cellräknaren Celldyn Sapphire och flödescytometern EPICS XL. Resultatet visas i Tabell 3. Tabell 3: Koncentrationen av CD3+, CD4+, och CD8+T-lymfocyter analyserade med EPICS XL och Celldyn Sapphire [celler x 10⁹/L] hos 39 patienter. Celldyn Sapphire Lymfocyter CD3+ CD3/4+ CD3/8+ CD4 /CD8 EPICS XL Medelvärde ± SD (x 10(9)/L) Min-Max (x 10(9)/L) 1,49 ± 0,79 0,99±0,64 0,60± 0,42 0,38 ±0,27 2,23 ± 1,21 0,08-3,76 0,03-2,78 0,02 -2,01 0,01-1,12 0,14-18,41 Medelvärde ± SD (x 10(9)/L) 1,50 ± 0,80 1,11± 0,65 0,68 ±0,44 0,40 ±0,27 2,54 ± 1,49 Min-Max (x 10(9)/L) 0,07 - 4,05 0,03 -3,05 0,02 - 2,30 0,01 -1,24 0,14 - 21,39 Korrelationskoefficient(r) beräknades mellan resultat från EPICS XL och Celldyn Sapphire vid analys av lymfocyter, CD3+, CD4+ och CD8+ T-lymfocyter hos de 39 patientproverna vilket framgår av Tabell 4. Denna korrelation beräknades även separat för prover med hög och låg koncentration av lymfocyter. Linjens lutning beräknades också vilken var högre än 0,9 vid nästan alla analyser (Figur 3,4). Tabell 4: Jämförelse av korrelationskoefficient (r) och linjens lutning vid analys av koncentrationen av lymfocyter, CD3+, CD4+ och CD8+ T-lymfocyter i 39 patientprover med EPICS XL och Celldyn Sapphire. n Korrelationskoefficient (r) Lutning Lymfocyter 39 0,985 0,925 Lymfocyter<0,8 x 10⁹/L CD3+ Lymfocyter 8 39 0,948 0,993 0,901 0,936 CD3+ Lymfocyter<0,7 x 10⁹/L CD3/4+ Lymfocyter 15 39 0,876 0,993 0,757 0,928 CD3/4+ Lymfocyter<0,5 x 10⁹/L CD3/8+ Lymfocyter 18 39 0,970 0,997 0,739 0,967 CD3/8+ Lymfocyter<0,25 x 10⁹/L 14 0,960 0,974 CD3/4+ Lymfocyter>0,4 x 10⁹/L 23 0,976 0,922 CD3/8+ Lymfocyter>0,15 x 10⁹/L 28 0,980 0,966 13 Jämförelse mellan flödescytometer och cellräknare + CD8 -T-lymfocyter CD3+CD8+-lymfocyter (Celldyn 4000) (x 109/L) Jämförelse mellan flödescytometer och cellräknare + 9 CD4 -T-Lymfocyter (<0,5 x 10 /L) 0,4 0,3 0,2 r=0,970 y=0,739x + 0,004 n=18 0,1 1,4 1,2 1,0 0,8 0,6 0,4 r= 0,997 y=0,967x -0,008 n=39 0,2 0,0 0,0 0,0 0,1 0,2 0,3 0,4 0,0 0,5 0,2 0,4 0,6 0,8 1,0 1,2 1,4 CD3+CD8+-lymfocyter (EPICS XL) (x109/L) CD3+CD4+-Lymfocyter (EPICS XL) Figur 3: Jämförelseanalys av koncentrationen av CD4+ T-lymfocyter (A) och CD8+ Tlymfocyter (B) i 39 patientprover mellan EPICS XL och Celldyn Sapphire (p<0,001). Jämförelse mellan flödescytometer och cellräknare + 9 CD4 -T-Lymfocyter (<0,5 x 10 /L) Jämförelse mellan flödescytometer och cellräknare CD8+-T-lymfocyter (<0,25 x 109/L) 0,5 0,25 CD3+CD8+-Lymfocyter (Celldyn) CD3+CD4+-Lymfocyter (Celldyn) CD3+CD4+-Lymfocyter (Celldyn) 0,5 0,4 0,3 0,2 r=0,970 y=0,739x + 0,004 n=18 0,1 0,1 0,2 0,3 0,4 0,15 0,10 0,5 r=0,960 y=0,974x + 0,007 n=14 0,05 0,00 0,00 0,0 0,0 0,20 0,05 0,10 0,15 0,20 0,25 CD3+CD8+-Lymfocyter (EPICS XL) CD3+CD4+-Lymfocyter (EPICS XL) Figur 4: (A) Jämförelseanalys av koncentrationer av CD4+ T-lymfocyter i 18 patientprover med mindre än 0,5 x 10⁹/L mellan EPICS XL och Celldyn Sapphire. (B) Jämförelseanalys av koncentrationer av CD8+ T-lymfocyter i 14 patientprover med mindre än 0,25 x 10⁹/L mellan EPICS XL och Celldyn Sapphire (p<0,001). Precision Spridningsmåttet vid analys i flödescytometern EPICS XL respektive Celldyn Sapphire beräknades genom att analysera tre olika blodprov 7 gånger vardera i flödescytometern samt 14 ett patientprov 10 gånger i Celldyn. Sedan beräknades medelvärdet, standardavvikelse och variationskoefficienten (CV%) vilket visas i Tabell 5. Tabell 5: Metodvariation beroende på instrumenten (CV%) vid analys av CD3+, CD4+, och CD8+ T-lymfocyter med EPICS XL [celler x 10⁹/L] i 3 blodprover från friska blodgivare samt ett blodprov från en patient med Celldyn Sapphire. EPICS XL CV%, mv – (min-max) Lymfocyter CD3+ CD3/4 + CD3/8 + Celldyn Sapphire CV%, mv– (max-min) 1,8 (1,3-2,4) 2,0 (1,8-2,1) 2,1 (0,9-2,8) 1,3 (0,4-1,9) 5,1 6,0 8,0 7,5 Spridning beroende på manuella moment och instrument beräknades genom att prov från fem olika blodgivare preparerades 10 gånger och analyserades med flödescytometern. Sedan beräknades variationskoefficienten vilket framgår av Tabell 6. Tabell 6: Metodvariation beroende på manuella moment och instrument (CV%), vid analys av CD3+, CD4+ och CD8+ T-lymfocyter med EPICS XL [celler x 10⁹/L] i 5 blodprover med normala leukocytkoncentrationer. EPICS XL CV% (mv) (min-max) Lymfocyter CD3+ CD3/4 + CD3/8 + CD4/CD8 3,8 (1,7-7,8) 3,9 (1,8-7,9) 4,1 (1,9-8,0) 5,0 (2,5-7,7) 3,6 (1,4-4,8) Linjaritet – EPICS XL För att studera hur spädning påverkar proverna, späddes ett prov till 1/1, 1/2, 1/4, 1/8, 1/16, 1/32, 1/64 och 1/128. Metoden visade en god linjaritet i intervallet ner till 0,01 x 10⁹/L för CD4 positiva T-lymfocyter respektive 0,003 x 10⁹/L för CD8 positiva T-lymfocyter. Korrelationskoefficienten (r) beräknades i bägge fallen (Figur 5). 15 Spädningskurva Spädningskurva 1 CD3+CD8+ (x109/L) A 0,1 + + 9 CD3 CD4 (x 10 /L) 1 B 0,1 0,01 0,009-0,96 x 10 9/L 0,003 - 0,46 x 10 9/L 0,01 0,001 1/128 1/128 1/64 1/32 1/16 1/8 1/4 1/2 1/64 1/32 1/1 1/16 1/8 1/4 1/2 1/1 spädning spädning Figur 5: (A)Analys av koncentrationen av CD4+ T-lymfocyter och (B) CD8+ T-lymfocyter i ett prov spätt 1/2 - 1/128. Hållbarhet i rumstemperatur (Celldyn 4000, EPICS XL) För att studera blodprovernas hållbarhet i rumstemperatur analyserades koncentrationen av CD4+ och CD8+ T-lymfocyter i prover från fem friska blodgivare efter tidsintervallet 0, 6, 24, 36 och 48 timmar med EPICS XL. Medelvärdet av variationskoefficient för CD4+ respektive CD8+ T- lymfocyter beräknades till 5,7% och 6,1% (Figur 6). 0,6 CD3+CD8+-Lymfocyter (x 109/L) CD3+CD4+-Lymfocyter (x 109/L) 1,0 0,8 0,6 0,4 0,2 0,0 0,5 0,4 0,3 0,2 0,1 0,0 0 7 24 31 48 0 Tid (timmar) 7 24 31 Tid (timmar) Figur6: Studie av hållbarheten i rumstemperatur av lymfocyter i 5 blodprov efter 0, 6, 24, 36 och 48 timmar. Koncentrationen av CD4+ och CD8+T-lymfocyter analyserades med EPICS XL. CD4+ T-lymfocyter CV% (mv): 5,7 (2,0-8,0), CD8+ T-lymfocyter CV% (mv): 6,1 (3,48,1). 16 48 Samma studie utfördes även med Celldyn Sapphire där koncentrationer av CD4+ och CD8+ T-lymfocyter analyserades i blodprover från tre friska blodgivare efter 0, 24, 48, 55 och 72 timmar. Denna analys utfördes med två olika instrument. Analysen efter 24 och 48 timmar utfördes med den ena instrumentet och övriga med det andra. De CD4 värden som saknades i figuren berodde på fel på provrören (Figur 7). 0,5 CD3 CD8 -lymfocyter (x 10 /L) 9 0,6 9 CD3 CD4 -lymfocyter (x 10 /L) 0,7 0,5 + 0,2 + + 0,3 + 0,4 0,4 0,3 0,2 0,1 0,1 0,0 0,0 0 24 Celldyn: 1 2 48 55 72 2 1 1 0 24 48 55 72 2 1 1 Tid (timmar) Tid (timmar) Celldyn: 1 2 Figur 7: Studie av hållbarheten i rumstemperatur av lymfocyter i 3 blod prov efter 0, 24, 48 och 72 timmar. Koncentrationen av CD4+ och CD8+ T-lymfocyter analyserades med Celldyn Sapphire. Förvaring av preparerade prover i mörker och dagsljus Tre prover från friska blodgivare analyserades med EPICS XL för att studera hur den beräknade koncentrationen av lymfocyter, CD3+, CD4+ och CD8+ T-lymfocyter förändras efter en, två respektive tre timmar förvaring i både mörker och dagsljus efter preparering. Resultatet framgår av Tabell 7. 17 Tabell 7: Studie av förvaring av preparerade prover i mörker och dagsljus efter 1, 2 och 3 timmar. Mörker början efter 1 tim efter 2 tim efter 3 tim Lymfocyter (%) 100 101 100 101 Normal rumsbelysning CD3 CD4 CD8 100 100 100 102 100 100 100 102 100 101 100 102 Lymfocyter (%) 100 97 101 97 CD3 CD4 CD8 100 97 101 97 100 94 97 93 100 97 102 99 Övriga faktorer Faktorer som är viktiga vid jämförelse av de två instrumenten bl.a. kostnad, provvolym och analystid redovisas i Tabell 8. Tabell 8: Sammanställning av övriga faktorer. EPICS XL-MCL Reagenskostnad Preparationstid Analystid Provvolym Provhantering Övrigt Celldyn Sapphire 204 kr ca 70 min 2 -4 min 100 µL Manuell pipettering --- 233 kr ---ca 10 min 225 µL Slutet system Varierande kvalitet på analysrören DISKUSSION Monitorering av CD4- cellnivån är väldigt viktig hos HIV patienter för att följa sjukdomsförloppet och avgöra när antiviralbehandling ska påbörjas [9]. Flödescytometri är en metod som idag används i många länder för att beräkna antal CD4 T-lymfocyter. Under den senaste tiden har helautomatiska cellräknare används vilket inte kräver att öppna blodrören. Många studier har utförts för att jämföra uträkning av CD4 T-celler mellan flödescytometern och cellräknaren Celldyn 4000 [10-12]. I dessa studier visade Cellräknaren bra korrelation med flödescytometer vid analys av CD4+ T-lymfocyter och en bra korrelation uppvisades även vid låga koncentrationer. I denna studie studerades koncentrationen av CD3+, CD4+ och CD8+ T-lymfocyter med flödescytometern EPICS XL. Analys av koncentrationer av CD3+, CD4+ och CD8+ Tlymfocyter i blod hos 40 friska vuxna blodgivare med hjälp av EPICS XL visade att 18 uppmätade värden stämmer bra med referensvärden som hade angivits tidigare av Abbott Diagnostik (Tabell 1, 2). När det gäller jämförelsen av resultat med flödescytometern och cellräknaren observerades god korrelation mellan EPICS XL och Celldyn Sapphire vid analys av lymfocyter, CD3+, CD4+ och CD8+ T-lymfocyter hos de 39 patientproverna (Tabell 4). Denna starka korrelation observerades även hos prover med hög och låg koncentration av lymfocyter. Linjens lutning var högre än 0,9 vid nästan alla analyser. Undantaget var låga koncentration av CD3respektive CD4+ T-lymfocyter där linjens lutning var mindre än 0,9. Detta innebär att cellräknaren ger något lägre värde (~ 30%), än flödescytometern vid analys av låg koncentration av CD4+ och CD3+ T-lymfocyter. Precision beroende på instrumenten som beräknades för bägge instrumenten, visade bra värde med CV% mindre än 10% (Tabell 5). Detta innebär att båda instrumenten är användbara vid analys av CD3+, CD4+ och CD8+ T-lymfocyter, men flödescytometern visade bättre precision (<2,4%) än cellräknaren (<10%). Även precision baserade på manuella moment som beräknades för flödescytometern visade ett bra värde på mindre än 5%. Vid spädning av prover ner till 1/128 visade metoden bra linjaritet med korrelationskoefficienten 0,99 vilket betyder att flödescytometer även kan analysera prover i väldigt låga koncentrationer och ändå visa tillförlitliga resultat. Korrekt förvaring av prover är viktig för att få ett korrekt svar vid analysen. Tidigare studier av analys av lymfocyter med Celldyn 4000 visade att förvaring av blodprover i rumstemperatur ökade antalet icke viabla celler jämfört med de prover som förvarades vid 4°C. Ökning av temperatur påskyndar celldödsprocessen [13]. Analys av koncentrationen av CD4+ och CD8+ T-lymfocyter med flödescytometern efter förvaring i rumstemperatur vid olika tidsintervall upp till 48 timmar visade ingen signifikant förändring i antalet Tlymfocyter i förhållande till variationskoefficienten. Metoden visade en låg variationskoefficient för CD4+ respektive CD8+ T- lymfocyter (5,7%, 6,1%) vilket betyder att lymfocyter har lång hållbarhet och kan analyseras även efter 48 timmar med flödescytometer. Däremot visade samma studie utförd med Celldyn Sapphire där koncentrationer av CD4+ och CD8+ T-lymfocyter analyserades i blodprover i tidsintervallet upp till 72 timmar, en sämre stabilitet. Koncentrationer av T-lymfocyter gick ner efter 24 timmar. Denna analys utfördes med två olika instrument (Celldyn Sapphire 25 och 26). Analysen som utfördes efter 24 och 48 timmar med Celldyn Sapphire 26 visade något lägre värde än Celldyn Sapphire 25 vilket betyder att de två instrumenten inte analyserade på 19 samma sätt. Saknade CD4 värden berodde på fel på provrören d.v.s. antikropparna satt inte fast i botten av rören. Förvaring av preparerade prover i mörker och dagljus, vanlig inomhusbelysning, studerades för att få en uppfattning om hur länge efter preparering man kan utföra analysen. I manualen från Beckman Coulter står att proverna skall analyseras högst två timmar efter preparering. Preparerade prover som stod i mörker upp till 3 timmar visade ingen förändring. Däremot visade preparerade prover som förvarades i inomhusbelysning något mindre stabilitet i den uppmätta koncentrationen av T-celler i jämfört med prover förvarade i mörker. Detta visar att preparerade prover är hållbara upp till tre timmar, men de håller sin stabilitet bättre om de förvaras i mörker. Denna studie visar att både flödescytometern EPICS XL och cellräknaren Celldyn Sapphire är tillförlitliga för att analysera koncentrationer av CD4 och CD8 positiva T-lymfocyter. Reagenskostnaden för celldyn är lite högre än för flödescytometern. Analysen med flödescytometer omfattar pipettering av prover vilket ökar risken för smittspridning. Prepareringen av prover för flödescytometri tar drygt en timme och själva analysen med instrumenten tar 2-4 minuter [l0]. Det är svårare att arbeta med flödescytometern. Den kräver vana vid hantering av dataprogram eftersom hanteringen av mjukvaran i flödescytometern inte är automatisk. Fördelen med flödescytometern är att medelvärdet för alla fyra fluorescensfärgerna kan kontrolleras med Flow Set vilket kan justeras om den inte stämmer överens med tidigare analyser. Analysen bygger på att mjukvaran genom ”gater” stegvis skiljer ut de celler som skall analyseras. Gaten kan justeras i efterhand så att man uppnår en korrekt lymfocytpopulation. I flödescytometern analyseras CD3, CD4 och CD8 lymfocyter samtidigt i samma rör. Celldyn Sapphire är ett helautomatisk och insluten system som inte ger någon kontakt med innehållet i blodröret. Det är lättare att arbeta med den och analystiden är knappt 10 minuter. Celldyn kan lättare användas för rutinanalys dygnet runt vilket ökar laboratoriets kapacitet att snabb analysera lymfocyterna vid behov [14]. Analysen bygger på att olika parametrar ställs mot varandra och mjukvaran har fasta gränser. Vid analys med Celldyn Sapphire är skillnaden mellan positiv och negativ fluorescensen liten vilket kan vara en nackdel i jämfört med flödescytometern där separationen är väldigt tydlig. Instrumentet analyserar CD4 och CD8 lymfocyter i två olika provrör, en med anti-CD4 och den andra med anti-CD8. Antikropparna skall sitta fast i botten av rören under analysen. Det visades sig att i vissa rör satt inte antikropparna fast i botten av röret vilket ledde till ett negativt svar. Detta kan skapa problem vid rutinanalys då det kräver ordentlig undersökning av rören innan analys. Dessutom är det 20 möjligt att antikropparna flyttar på sig när instrumenten vänder upp och ner rören för blandning av blodproverna. Denna studie visar att både EPICS XL och Celldyn Sapphire är användbara vid analys av koncentrationen av CD4+ och CD8+ T-lymfocyter. Det är dock något säkrare att använda flödescytometern vid analys av lägre koncentrationen av CD4+ T-lymfocyter (<200 celler/µL). Det behövs flera studier vid analys av låga koncentrationen av CD4+ Tlymfocyter med Celldyn Sapphire för att avgöra hur säkert den analyserar. ACKNOWLEDGEMENT En särskild tack vill jag ge till min handledare Lena Douhan Håkansson för hennes tålamod och engagemang och den tid hon har lagt för utformning av detta arbete både det praktiska utförandet och vid skrivandet av rapporten. Hon har alltid varit tillhands och svarat gärna på alla mina frågor. Ett stort tack till Anders Larsson som har hjälpt mig med skrivandet av rapporten med sina bra kommentarer och Agneta Trulson som gav mig möjligheten att utföra detta arbete på Klinisk Kemi. Jag vill också tacka Birgitta Wande och personalen på klinisk kemi och farmakologi både de som jobbar vid forskning och utvecklings labb och Celldyn Sapphire för att de låt mig ta del av deras aktivitet. Jag har alltid känt mig välkommen hos er. REFERENSER [1] Reichert T, et al. Lymphocyte subset reference ranges in adult Caucasians. Clin Immunol Immunopathol. 1991; 60(2): 190-208 [2] Bofil M, et al. Laboratory control values for CD4 and CD8 T lymphocytes. Implications for HIV-1 diagnosis. Clin Exp Immunol. 1992; 88(2): 243-252 [3] Uppal SS, et al. Normal values of CD4 and CD8 lymphocyte subsets in healthy Indian adults and effects of sex, age, ethnicity and smoking. Cytometry B Clin Cytom. 2003; 52(1): 32-36 [4] Pattanapanyasat K, et al. CD4+ T cell Count as a tool to monitor HIV progression & antiretroviral therapy. Indian J Med Res. 2005; 121(4): 539-549 [5] Paranjape RS. Immunopathogenesis of HIV infection. Indian J Med Res. 2005; 121(4) 240-255 21 [6] Khalsa AM. Preventive counselling, screening, and therapy for the patient with newly diagnosed HIV infection. Am Fam Physician. 2006; 73(2): 271-280 [7] Yeni PG, et al. Antiretroviral treatment for adult HIV infection in 2002. JAMA. 2002; 288(2): 222-235 [8] Johannessen B, et al. Implementation of monoclonal antibody fluorescence on the Abbott Celldyn Sapphire haematology analyser, evaluation of lymphoid, myeloid and platelet markers. Clinical Lab Haematol. 2006; 28(2): 84-96 [9] Kandathil A.J. et al. Comparison of Micro capillary cytometry technology and flowcytometry for CD4+ and CD8+ T-cell estimation. Clin Diagn Lab Immunol. 2005; 12(8): 1006-1009 [10] Marshall P, et al. Rapid, automated, closed- tube Quantitation of CD4+ and CD8+ T-cell populations on the Cell-dyn 4000. Clin Lab Haematol. 2000; 6(3): 137-143 [11] Yamane T, et al. T- lymphocyte subset analysis using the automated haematology analyser Cell-dyn 4000 for patients with haematological disorders. Leuk Lymphoma. 2006; 47(3): 503-506 [12] Hagihara K, Et al. Evaluation of an automated Haematology analyser (Cell-dyn 4000) for counting CD4+ T helper cells at low concentrations. Ann Clin Lab Sci. 2005; 35(1): 31-36 [13] Grimaldi E, et al. Evaluation of the Abbott Cell-Dyn 4000 haematology analyzer. Am J Clin Pathol. 2000; 113(4): 497-505 [14] Molero T, et al. Analysis and enumeration of T-cells, B-cells and NK cells using the monoclonal antibody fluorescence capability of a routine haematology analyser (cell-Dyn CD4000). Clin Lab Haematol. 2005; 27(4): 224-234 22