Förekomst av genuttryck för enzymer i biosyntesen av
advertisement

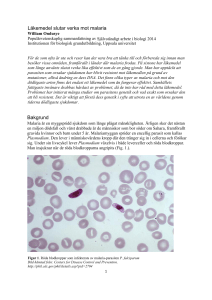
Examensarbete 15hp Förekomst av genuttryck för enzymer i biosyntesen av artemisinin hos Artemisia dracunculus Författare: Emil Kennedy Handledare: Anneli Lundgren Examinator: Kjell Edman Termin: VT14 Ämne: Biomedicinsk vetenskap 15 hp Nivå: Grundnivå Kurskod: 2BK01E Förekomst av genuttryck för enzymer i biosyntesen av artemisinin hos Artemisia dracunculus Emil Kennedy Examensarbete i Biomedicinsk vetenskap, 15 hp Filosofie Kandidatexamen Handledare: Anneli Lundgren Laboratorieingenjör Institutionen för kemi och biomedicin Linnéuniversitet 391 82 Kalmar Examinator: Kjell Edman, Ph.D. Institutionen för kemi och biomedicin Linnéuniversitetet 391 82 Kalmar Sammanfattning Malaria drabbar över 200 miljoner människor årligen och är främst utbredd i Afrika. Många som drabbas är fattiga och har svårt att ha råd med botemedel. Malaria överförs genom bett från Anopheles myggor som blivit infekterade av parasiter från Plasmodium släktet. Den vanligaste parasiten heter Plasmodium falciparum och ger upphov till obehagliga febercykler. År 1972 påvisades förekomst av artemisinin i växten Artemisia annua. Artemisinin är en aktiv substans i malarialäkemedel som ger effektiv avdödning av malariaparasiter. Avbrutna behandlingar har lett till att parasiten börjat bli resistent mot läkemedlet. Kombinerade behandlingar har därför tagits fram för fortsatt effektiv behandling. Artemisia annua har tack vare sin förmåga att bilda artemisinin börjat användas över hela världen som behandling mot malaria. Mängden artemisinin som kan framställas ur varje enskild växt är dock relativt liten och därför har intensiv forskning för att öka mängden artemisinin inletts, bl.a. genom att studera andra växter som ingår i Artemisia släktet. I denna studie undersöks förekomst av gener samt genuttryck för enzym som ingår i biosyntesen av artemisinin i växten Artemisia dracunculus genom RNA isolering, cDNA syntes, extraktion av genomiskt DNA och PCR. RNA för Farnesyl diphosphate synthase (FDS), 3-hydroxy-3methyl-glutaryl-CoA reductase (HMGR) och Amorpha-4, 11-diene 12-hydroxylase (CYP71AV1) kunde påvisas med PCR. Amorpha-4, 11-diene synthase (ADS) och Artemisinic aldehyde reductase (DBR2) som är nyckelenzym i biosyntesen av artemisinin uttrycks inte i Artemisia dracunculus. Förekomst av generna för ADS och DBR2 kunde heller inte påvisas. Ytterligare forskning krävs för att på längre sikt kunna öka utvinning av nyckelsubstansen artemisinin och på så sätt minska förekomst av malaria. Abstract Malaria affects over 200 million people annually and is mostly prevalent in Africa. Many victims are poor and unable to afford the cure. Malaria transmits usually through bites from the Anopheles mosquitos which are infected by parasites from the genus Plasmodium. The most common parasite is called Plasmodium falciparum which give rise to unpleasant fever cycles. Artemisinin was first found in Artemisia annua in 1972. Artemisinin is the active substance in malaria drugs and it is effectiv in eliminating malaria parasites. Interrupted treatment has led to recurrence of the disease. Combined treatments have therefore been developed for continued effective treatment. Artemisia annua is due to its ability to produce artemisinin, used worldwide as a treatment for malaria. The amount of artemisinin that can be extracted from each individual plant is relatively small and therefore intensive research has been initiated to increase the amount of artemisinin, which involves examining other plants in the Artemisia genus. This study examines the prevalence of genes and gene expression of the enzymes involved in the biosynthesis of artemisinin in Artemisia dracunculus by RNA isolation, cDNA synthesis, genomic DNA extraction and PCR . Farnesyl diphosphate synthase (FDS), 3-hydroxy-3-methyl-glutaryl-CoA reductase (HMGR) and Amorpha-4, 11-diene 12-hydroxylase (CYP71AV1) where amplified. Amorpha-4, 11-diene synthase (ADS) and Artemisinic aldehyde reductase (DBR2) which are key enzyme in the biosynthesis of artemisinin were not amplified and thus are not likely to be expressed in Artemisia dracunculus. The genes of ADS and DBR2 could not be detected in genomic DNA. Further research is required in the long term to provide increased extraction of the key substance artemisinin and to reduce the up come of malaria. Innehållsförteckning 1. Bakgrund ................................................................................................................................................................................ 1 1.1 Artemisinin och Artemisia annua .................................................................................................................................... 2 1.2 Artemisia dracunculus ..................................................................................................................................................... 4 1.3 RNA isolering.................................................................................................................................................................. 4 1.4 cDNA syntes.................................................................................................................................................................... 1 1.5 Extraktion av genomiskt DNA ........................................................................................................................................ 5 1.6 PCR och gelanalys ........................................................................................................................................................... 5 Syfte ...................................................................................................................................................................................... 5 Problemformulering .............................................................................................................................................................. 5 2. Material och metod................................................................................................................................................................. 6 2.1 Provmaterial .................................................................................................................................................................... 6 2.2 Förhindra kontaminering ................................................................................................................................................. 6 2.3 RNA isolering från A.dracunculus .................................................................................................................................. 6 2.4 Framställning av cDNA ................................................................................................................................................... 6 2.5 PCR med FDS, HMGR och ADS .................................................................................................................................... 7 2.5.1 PCR med primers för fullängds ADS....................................................................................................................... 9 2.5.2 PCR med framställt cDNA som templat .................................................................................................................. 9 2.6 Extraktion av genomiskt DNA (CTAB method) .......................................................................................................... 10 2.6.1 PCR med gDNA som templat ................................................................................................................................ 10 3. Resultat................................................................................................................................................................................. 11 3.1 PCR med FDS, HMGR och ADS .................................................................................................................................. 11 ............................................................................................................................................................................................. 11 3.2 PCR med fullängds ADS primers .................................................................................................................................. 11 3.3 PCR med ADS, FDS, DBR2, HMGR och CYP71AV1 primers ................................................................................... 12 3.4 PCR med genomiskt DNA som templat ........................................................................................................................ 13 4. Diskussion ............................................................................................................................................................................ 13 Slutsats ................................................................................................................................................................................ 15 Tack ..................................................................................................................................................................................... 16 5. Referenslista ......................................................................................................................................................................... 17 Förkortningar ACTs = Artemisinin-based combination therapies ADS = Amorpha-4, 11-diene synthase ALDH 1 = Aldehyde dehydrogenase 1 cDNA = komplementär Deoxiribonukleinsyra CTAB-METHOD = Cetyl trimethylammonium bromide CYP71AV1 = Amorpha-4, 11-diene 12-hydroxylase DBR2 = Artemisinic aldehyde reductase DEPC = Diethylpyrocarbonate DNA = Deoxiribonukleinsyra FDS = Farnesyl diphosphate synthase FDP = Farnesyl diphosphate GST = Glandular Secretion Trichomes HMGR = 3-hydroxy-3-methyl-glutaryl-CoA reductase HPLC = High Performance Liquid Chromatography mRNA = messenger Ribonukleinsyra RNA = Ribonukleinsyra PCR = ”Polymerase Chain Reaction” WHO = World Health Organization 1. Bakgrund Malaria är en sjukdom som främst finns i tropiska och subtropiska regioner runt ekvatorn (Figur 1). Afrika är svårt drabbat men även delar av Asien och Amerika är drabbade. ”The World Health Organization” (WHO) fastställde att det har förekommit 219 miljoner fall av malaria år 2012, men troligtvis finns det ett stort mörkertal som inte har dokumenterats (1, 2). Figur 1. Förekomst av malaria i varje land (per 100 000 invånare) där skalan går från ljusgul (mindre än 10 fall) till mörkröd (mer än 3500 fall) (3). Malaria överförs vanligtvis genom bett från Anopheles myggor som blivit infekterade av parasiter från Plasmodium släktet (Figur 2). Den mest spridda och dödliga arten är Plasmodium falciparum (P. falciparum). Infektionen uppstår då myggan suger blod och samtidigt sprutar in saliv innehållande sporozoit. Sporozoiter sprider sig sedan vidare till levern och ombildas till schizonter. Schizonterna innehåller tusentals merozoiter som i stora mängder bidrar till att schizonterna brister och merozoiterna faller ut i blodomloppet. Väl ute i blodet tar sig merozoiterna in i de röda blodkropparna och bildar trofozoiter. Trofozoiter tillgodogör sig näringsämnen genom att sönderdela hemoglobinet i våra blodkroppar. Gametocyter ligger kvar i blodkroppar och när nästa mygga suger blod från en malariasmittad människa får den med sig gametocyter. Gametocyterna tar sig till myggans tarmsystem där de utvecklas till mogna könsceller. Detta leder i sin tur till att nya sporozoiter kan ta sig till salivkörtlarna och en ny malariacykel uppstår. När malaria spridit sig i kroppen uppstår febercykler och patienten kan gå från att må relativt bra till att insjukna i kraftiga feberattacker. Detta beror på att P. falciparum tillväxer inuti de röda blodkropparna. Dessa går sönder, och antikroppar och toxiner frisätts ut i kroppen. Symptomen minskar sedan tills parasiten återigen förstör de röda blodkropparna med nya feberattacker som följd (4-6). 1 Figur 2. Livscykeln för Plasmodium spp, där tre olika cykler förekommer. Inuti Anophelesmyggan börjar ”sporogonic cycle” följt av två utvecklingscykler inuti människan, ”exo-erythrocytic cycle” och ”erythrocytic cycle”, som sker i levern respektive i erytrocyterna (7). 1.1 Artemisinin och Artemisia annua Artemisinin upptäcktes som ett fungerande botemedel mot malaria redan år 1596, men det var först år 1972 som Tu Youyou identifierade förekomsten av artemisinin i Artemisia annua (A. annua) eller Sommarmalört som den kallas på svenska. Forskning visade att artemisinin kan döda malariaparasiten i ett tidigt stadium utan några tecken på bieffekter (8). Den effektiva avdödningen har dock fått konsekvenser. Patienter som behandlats med artemisinin har känt sig bättre inom 24 timmar, vilket har lett till avbrutna behandlingar. En avbruten behandling kan leda till återkommande sjukdom. Forskare har därför börjat kombinera andra antimalarialäkemedel med artemisinin och skapat så kallade ”Artemisinin-based combination therapies” (ACTs). ACTs som ”artemether/lumefantrine” och ”artesunate/amodiaquine” har använts mot okomplicerad malaria i stora delar av Afrika med bättre resultat än enbart artemisinin. Till skillnad från artemisinin är ACTs betydligt dyrare, vilket har lett till förfalskningar på många apotek i världen där man inte har råd med äkta ACTs. Med anledning av detta är det nu viktigare än någonsin med ett prisvärt botemedel mot malaria (9). A. annua har tack vare sin förmåga att bilda artemisinin börjat användas över hela världen som behandling mot malaria. Mängden artemisinin som kan framställas ur varje enskild växt är dock relativt liten och forskare har därför inlett en intensiv forskning för att öka mängden 2 artemisinin i A. annua eller på annat sätt få fram mer artemisinin (10). För att biosyntesen av artemisinin ska kunna genomföras krävs det att ”3-hydroxy-3-methyl-glutaryl-CoA reductase” (HMGR) finns. Utan HMGR kan biosyntesen inte starta och därmed kan inte artemisinin bildas. Ett annat viktigt enzym för bildningen av artemisinin är ”Farnesyl Diphosphate Synthase” (FDS) som katalyserar bildningen av ”Farnesyl Diphosphate” (FDP), som i sin tur är en prekursor för steroler och terpener. En viktig seskviterpen i A. annua bildas av enzymet ”amorpha-4, 11-diene synthase” (ADS), som är det första viktiga steget i biosyntesen av artemisinin (11, 12). ADS hittas i de ”Glandular Secretion Trichomes” (GST) som sitter på ytan av växtens blad (Figur 3). I artikeln Olofsson et al. visar Figur 3. Ljus mikroskopbild av resultatet att förekomsten av de fyra enzymerna som ingår i GST från A.annua biosyntesen av artemisinin finns i betydligt större mängd i blomknoppar och i unga blad (ställen med hög mängd GST) jämfört med andra delar av växten (10). GSTs struktur består av tre sekretoriska celler; apikala celler, basala celler och stalkceller. De apikala cellerna är transparenta och innehåller proplastid eller leukoplast medan basala och stalk celler innehåller kloroplaster (12). Biosyntesen för artemisinin är nästan helt klarlagd. Enzymet ADS gör det inledande steget i ringslutningen av FDP och slutprodukten blir ”amorpha-4, 11-diene (amorphadiene) (Figur 4). Biosyntesen fortsätter sedan med att amorphadiene hydroxyleras för att erhålla ”artemisinic alcohol”. Detta sker genom att ”amorpha-4, 11-diene 12-hydroxylase” (CYP71AV1) katalyserar den kemiska reaktionen. CYP71AV1 kan även oxidera alkoholen till ”artemisinic aldehyde”. I fortsatt biosyntes till artemisinin krävs det att ”artemisinic aldehyde” reduceras till ”dihydroartemisinic aldehyde” som oxideras till ”dihydroartemisinic acid”, som sen ger upphov till slutprodukten genom påverkan av syre och ultraviolett ljus. De två enzymatiska stegen till uppkomsten av ”dihydroartemisinic acid” katalyseras av ”artemisinic aldehyde reductase” (DBR2) och ”aldehyde dehydrogenase 1” (ALDH1) (13, 14). Figur 4. En schematisk översikt av biosyntesen för artemisinin. 3 1.2 Artemisia dracunculus Artemisia dracunculus (A. dracunculus) är det latinska namnet för dragon, en växt främst är förknippad som krydda i mat men som även visat sig vara blodglukossänkande. A. dracunculus tillhör samma släkte som A. annua vilket möjliggör att även A. dracunculus kan innehålla artemisinin. Enligt artikeln Mannan et al. har förekomst av artemisinin hittats i A.dracunculus. Artikeln i fråga har dock använt sig av High Performance Liquid Chromatography (HPLC). Detta är en separationsmetod som bör kombineras med Masspektrometrisk (MS) analys för identifikation (15). Ribonukleinsyra (RNA) från A. dracunculus användes som utgångsmaterial för syntes av komplementär deoxiribonukleinsyra (cDNA) templat följt av PCR, för utvärdering om huruvida artemisinin kan produceras i andra arter av släktet Artemisia. Även genomiskt DNA användes som templat för att påvisa eventuell förekomst av generna för de viktiga enzymerna (16). 1.3 RNA isolering Isolering av total RNA (allt RNA i en cell) är ett viktigt steg för att få en hög kvalitet på RNA produkten. RNAt är väldigt känsligt och risken för kontaminering är hög. För att få hög avkastning av det genetiska materialet krävs en effektiv finfördelning av vävnaden. Det är även viktigt att hålla vävnaden så kall som möjligt under extraktionen för att undvika degradering. Det är alltså viktigt att sönderdela cellmembranet, minimera frisättning av RNaser och minimera risk för kontaminering. Risken för kontaminering ökar då cellerna lyserar. Detta beror på att den regulatoriska mekanismen störs vilket kan ge upphov till snabb degradering(17). 1.4 cDNA syntes Figur 5. Ett diagram av en PCR-reaktion cDNA syntes är en process som används för att på ett säkert som demonstrerar hur amplifiering leder sätt syntetisera cDNA från messenger RNA (mRNA). mRNA till exponentiell tillväxt av en produkt för över information från DNA till ribosomerna vilket leder till flankerad av primers. genuttryck (18). För att genomföra syntesenav cDNA från mRNAt används ett RNA-beroende DNA-polymeras som kallas Moloney Murine Leukemia Virus (M-MLV) reverse transkriptas (19). Till poly(A)-svansen på mRNAt binder Oligo(dT)18 Primer. När Oligo(dT)18 primer binder in fosforylerar den 5´ änden för att underlätta kloning av cDNAt (20). 4 1.5 Extraktion av genomiskt DNA Vid extraktion av genomiskt DNA är det viktigt att sönderdela växtens cellväggar. Vid lysering av cellens väggar uppstår ytterligare problem då lysatet innehåller bland annat tanniner, fenoler och polysackarider som kan påverka DNA-kvalitéten samt inhibera efterföljande reaktioner. För att undvika detta används ofta speciella kit som kan behandla dessa komponenter på ett effektivt sätt (21). 1.6 PCR och gelanalys Polymerase chain reaction (PCR) används för att framställa stora mängder av en vis DNAsekvens. Till PCR behövs nukleotider (dATP, dGTP, dTTP och dCTP), DNA-polymeras (enzym som bygger samman DNA-kopian genom att använda sekvenser från cDNAt som mall), primers (korta DNA-sekvenser som bidrar till en startpunkt för DNA-syntesen) och en buffertlösning (innehåller magnesiumjoner som behövs för att DNA-polymeraset ska fungera optimalt) (22, 23). Detta blandas sedan samman med cDNA i ett PCR-rör och sätts i en PCRmaskin. Proverna hettas upp till 95°C vilket gör att DNA strängarna separerar (denaturering). Temperaturen sänks sedan snabbt till 5°C under ”melting temperature”. Detta gör att primerna binder till sina specifika bindningsställen (annealing). Temperaturen höjs sedan igen till 72°C där DNA-polymeraset fungerar optimalt och börjar bygga en kopia av cDNA-templatet. Detta leder till att antalet DNA-templatet fördubblas. Sedan upprepas processen 25-30 gånger (Figur 5). För att undersöka vilken längd PCR-produkten har, utförs en gelelektrofores, för att separera molekyler efter storlek. Till gelelektrofores används en gel av agaros. En elektrisk spänning läggs över gelen och DNAt som är minusladdat kommer att vandra genom gelen mot pluspolen. PCR-fragment färgas in med GelRed och visualiseras i en geldokumenteringsutrustning vilken gör det möjligt att se DNA-kopiornas längd. Mindre och kortare fragment vandrar snabbare genom gelen medan större och längre DNA-fragment vandrar långsammare (22). Syfte Syftet med studien var att studera eventuell förekomst av genuttryck för enzymerna ADS, FDS, DBR2, HMGR och CYP71AV1 i växten Artemisia dracunculus (dragon). Problemformulering Förekommer ett eller flera av enzymerna som krävs för bildning av artemisinin även i andra arter av Artemisia-släktet? Om så är fallet, har dessa växter i så fall möjlighet att producera artemisinin? 5 2. Material och metod 2.1 Provmaterial I den här studien användes unga blad från växten dragon (Artemisia dracunculus) för extraktion av RNA och genomiskt DNA (gDNA).. 2.2 Förhindra kontaminering För att undvika kontaminering av RNAt användes Diethylpyrocarbonate (DEPC) behandlade rör och pipettspetsar, ribonuclease (RNase) fria reagenser, RNase inhibitor för att skydda RNA-templatet. Viktigt var också att rören var väl tillslutna. RNA-arbetet utfördes i dragskåp och under hela processen användes handskar som kontinuerligt byttes ut. 2.3 RNA isolering från A.dracunculus Innan bladen från dragon tillsattes, kyldes RNase-fria mikrorör. Växtvävnaden finfördelades i flytande kväve och maldes till ett pulver i en steril iskall mortel. Vid RNA isolering från växtcellerna tillsattes 0,5 ml kall ”PureLink™ plant RNA reagent” (Invitrogen) till 0,1 g frusen växtvävnad. Blandningen mixades och röret inkuberades under 5 minuter i rumstemperatur. För att få en klar lösning centrifugerades (Eppendorf Mini spin plus) röret vid 12000 rpm i rumstemperatur under 2 minuter. Efter centrifugering överfördes supernatanten till ett nytt RNase-fritt rör. Till supernatanten tillsattes 0,1 ml 5M NaCl och blandades genom att flicka på röret. Till provet tillsattes 0,3 ml kloroform och blandades noggrant genom att vända röret försiktigt. Provet centrifugerades vid 12000 rpm i 4°C under 10 minuter. Efter centrifugering överfördes den övre vattenbaserade fasen till ett RNase-fritt rör. Isopropylalkohol tillsattes i samma volym som vattenfasen för utfällning av RNA som föreligger i vattenhaltigt medium. Provet blandades och fick stå i rumstemperatur under 10 minuter. Provet centrifugerades vid 12000 rpm i 4°C under 10 minuter. Supernatanten avlägsnades. Till pelleten tillsattes 1 ml 75 % etanol och centrifugerades vid 12000 rpm i rumstemperatur under 1 minut. Supernatanten dekanterades och ytterligare en centrifugering utfördes för att spinna ner restvätskan och sedan pipettera upp den. När pelleten torkat tillsattes 30 µl DEPC behandlat H2O som pipetterades upp och ner över pelleten för att resuspendera RNA:t. 2.4 Framställning av cDNA Vid framställning av komplementärt DNA (cDNA) användes ”RevertAid™ H Minus Reverse Transcriptase”, ”RiboLock™ RNase Inhibitor”, dNTP Mix 10 mM av varje nukleotid, samt Oligo(dT)18 primer (Thermo Scientific United Kingdom). För att få bort eventuellt genomiskt DNA från RNA-preparationen utfördes en DNase behandling. Till ett RNase-fritt rör tillsattes 25,5 µl RNA, 3 µl 10X Reaction Buffer med MgCl2 och 1,5µl RNase-fri DNase 1. Provet inkuberades vid 37°C under 30 minuter. Därefter 6 tillsattes 3 µl 50 mM EDTA för att undvika att RNA hydrolyseras vid inaktiveringen av DNaset. Provet inkuberades sedan vid 65°C under 5 minuter. Till cDNA-syntesen användes 0,5µl RNA-templat (1µg), 1µl oligo(dT)18 primer och 9,5 µl nukleasfritt vatten (totalt 11 µl) som tillsattes till ett rör på is och inkuberades vid 65°C under 5 minuter. Provet placerades därefter på isen och 4 µl 5X Reaction Buffer, 1µl RiboLock RNase inhibitor, 2 µl dNTP mix samt 2 µl RevertAid™ H Minus Reverse Transcriptase tillsattes (totalt 20 µl). Provet mixades försiktigt och centrifugerades. Provet inkuberades sedan vid 37°C under 60 minuter, följt av 70°C under 5 minuter. För att undvika inhibering vid PCR-amplifieringen utfördes en RNase-behandling, där 35 µl cDNA, 4 µl 10X Buffer RNase samt 1 µl RNase H tillsattes till ett rör. Detta rör inkuberades sedan vid 37°C i 60 minuter, följt av 65°C i 10 minuter. 2.5 PCR med cDNA för FDS, HMGR och ADS Vid PCR med FDS, HMGR och ADS primers användes ”PuReTaq™ Ready-To-Go-™ PCR beads” (GE Healthcare United Kingdom) innehållande 2,5 U PuReTaq DNA polymeras, 200 µM dNTP mix, 50 mM KCL och 1,5 mM MgCl2 (24). Till rören tillsattes 22 µl dH2O, 1 µl forward primer, 1 µl reverse primer (Tabell I) och 1 µl cDNA. Två av rören användes som positiv kontroll respektive negativ kontroll. I den positiva kontrollen byttes cDNA:t ut mot pJETADS-plasmid innehållandes cDNA för ADS (Per Mercke) medan det i den negativa kontrollen tillsattes dH2O som templat. 7 Tabell I. Primersekvenser för respektive enzym som nyttjats i studien. Primer Sekvens ADSfw #634 5'-GGG AGA TCA GTT TCT CAT CTA TGA A-3' ADSrev #635 5'-CTT TTA GTA GTT GCC GCA CTT CTT-3' ADSfwRT #496 5'-GGG AGA TCA GTT TCT CAT CTA TGA A-3' ADSrevRT #504 5'-CTT TTA GTA GTT GCC GCA CTT CTT-3' FDSfwRT #509 5´-ATC TGC CCT TGG TTG GTG TAT TGA-3´ FDSrevRT #510 5´-GTT GCC CTC TGC GTG TAT GAG A-3´ DBR2QPCRfw3 #737 5'-GCG GTG GTT ACA CTA GAG AAC TT-3' DBR2QPCRrev3 #738 5'-ATA ATC AAA ACT AGA GGA GTG ACC C-3' HMGRfwRT #512 5´-GGG CGT GGA AAA TCT GTT GTG TTC-3´ HMGRrevRT #501 5´-GAA CCA GCA ATA GCA GAA CCA GTA A-´3 CYPfwRT #506 5'-CGA GAC TTT AAC TGG TGA GAT TGT-3' CYPrevRT #517 5'-CGA AGC GAC TGA AAT GAC TTT ACT-3' Fragmentlängd av PCR-produkt 1600 bp 95 pb 92 bp 228 bp 136 bp 144 bp För att amplifiera upp korta fragment av FDS, HMGR och ADS användes ett PCR-program med inledande denaturering, under 3 minuter vid 95°C. Detta följdes av 25 cykler innehållande 30 sekunder denaturering vid 95°C, annealing i 30 sekunder vid 60°C, samt extension i 30 sekunder vid 72°C. Programmet avslutades med en extension i 8 minuter vid 72°C, följt av kylning vid 4°C i ∞. När PCR-programmet avslutats tillverkades en 3 % agarosgel. Till en bägare tillsattes 0,75 g agarospulver samt 25 ml (25 g) 0,5x TBE buffert (5x lösning innehållande 450 mM TRIS-bas, 450 mM Borsyra, 10 mM EDTA). Lösningen hettades upp på 360 W i en mikrovågsugn tills alla partiklar var lösta. Lösningen blandades och varmt destillerat vatten tillsattes sedan för att återfå rätt vikt (25 g). Lösningen mixades ordentligt och tillsattes till en gelform. Sedan blandades 10 µl PCR-produkt med 2 µl 6x Loading Buffer (innehållande 30 % sukrose, 0,35 % Orange G (Sigma-Aldrich United Kingdom)) och tillsattes i brunnarna på gelen. I två av brunnarna tillsattes 5 µl DNA-markör (Thermo scientific) medan det i den sista brunnen tillsattes 3 µl cDNA, tillsammans med 2 µl 8 6x Loading Buffer (Figur 6). Gelen placerades i en elektroforesutrustning (Mupid-eXu) vid 100 V i 30 minuter och inkuberades i GelRed (Biotium USA) i 60 minuter, följt av en bildanalys i en geldokumenteringsutrustning (ChemiDoc MP). 2.5.1 PCR med primers för fullängds ADS cDNA Vid PCR med fullängds ADS primers, användes ”PuReTaq™ Ready-To-Go-™ PCR beads” . Till rören tillsattes 22 µl dH2O, 1 µl forward primer, 1 µl reverse primer (Tabell I) och 1 µl cDNA. En positiv kontroll gjordes där cDNA:t byttes ut mot pJETADS-plasmid, samt en negativ kontroll (FDS primer) där dH2O tillsattes som templat. För att amplifiera ADS användes ett PCR-program med inledande denatuering under 3 minuter vid 95°C, följt av 25 cykler innehållande 30 sekunder denatuering vid 95°C, annealing i 30 sekunder vid 67°C, samt extension i 2 minuter vid 72°C. Sedan följde en avslutande extension i 10 minuter vid 72°C, följt av kylning vid 4°C i ∞. När PCRprogrammet avslutats tillverkades en 0,8 % agarosgel. Till en bägare tillsattes 0,2 g agarospulver samt 25 ml (25 g) 0,5x TBE buffert. Lösningen hettades upp i en mikrovågsugn (360 W) tills alla partiklar var lösta. Lösningen blandades och destillerat vatten tillsattes för att återfå rätt vikt (25 g). Lösningen mixades ordentligt och tillsattes till en gelform. När gelen stelnat blandades 10 µl PCR-produkt och 2 µl 6x Loading Buffer, vilket tillsattes i fyra av brunnarna på gelen. I två av brunnarna tillsattes 5 µl DNA markör (Figur 7). Gelen placerades i en elektroforesutrustning vid 100 V i 30 minuter och inkuberades i GelRed i 60 minuter, följt av en bildanalys i en geldokumenteringsutrustning. 2.5.2 PCR med framställt cDNA som templat Vid PCR med ADS, FDS, DBR2, HMGR och CYP71AV1 primers, användes ”PuReTaq™ Ready-To-Go-™ PCR beads. Till rören tillsattes 22 µl dH2O, 1 µl forward primer, 1 µl reverse primer (Tabell I) och 1 µl cDNA. En positiv och en negativ kontroll utfördes. I de positiva kontrollerna byttes templatet ut mot cDNA från A.annua och i den negativa kontrollen tillsattes dH2O som templat (Figur 8) För att amplifiera fragment av ADS, FDS, DBR2, HMGR och CYP71AV1-sekvenserna användes ett PCR-program med inledande denaturering under 2 minuter vid 95°C, följt av 30 cykler innehållande 30 sekunder denaturering vid 95°C, annealing i 30 sekunder vid 60°C samt extension i 30 sekunder vid 72°C. En avslutande extension utfördes i 8 minuter vid 72°C, följt av kylning vid 4°C i ∞. När PCR-programmet avslutats tillverkades en 2,4 % agarosgel. Till en bägare tillsattes 50 ml (50 g) 0,5x TBE buffert tillsammans med 1,2 gram agaros. Lösningen hettades upp på 360W i en mikrovågsugn tills alla partiklar var lösta. Sedan blandades lösningen och varmt destillerat vatten tillsattes för att återfå rätt vikt (50 g). Lösningen mixades ordentligt och tillsattes till en gelform. När gelen stelnat blandades 10 µl PCR-produkt med 2µl 6x Loading Buffer och laddades i 11 av brunnarna på gelen. I tre av 9 brunnarna tillsattes 5 µl DNA-markör (Figur 8). Gelen placerades i en elektroforesutrustning vid 100 V i 30 minuter. Gelen inkuberades i 60 minuter i GelRed, följt av en bildanalys i en geldokumenteringsutrustning. 2.6 Extraktion av genomiskt DNA (CTAB method) Vid extraktion av genomiskt DNA (gDNA) finfördelades toppskott från A. dracunculus noggrant i flytande kväve i en mortel. Till ett 10 ml rör tillsattes 100 mg toppskott följt av 600 µl upphettad i Cetyl trimethylammonium bromide (CTAB) -buffer (innehållande 2 % mercaptoethanol). CTAB lyserar membranet och binder till DNAt. Rören inkuberades vid 65°C i 45 minuter och fick stå i rumstemperatur i 5 minuter, för att sedan centrifugeras vid 13000 rpm i rumstemperatur under 10 minuter. Till ett nytt rör innehållande 500 µl 24:1 kloroform: isoamylalkohol (proteiner övergår till kloroform-fasen) tillsattes 500 µl supernatant. Blandningen i röret mixades och fick stå i rumstemperatur i 5 minuter, följt av centrifugering vid 13000 rpm i rumstemperatur under 10 minuter. Till ett nytt rör tillsattes 400 µl av vattenfasen tillsammans med 400 µl isopropanol (DNA är mindre lösligt i isopropanol än i vatten). För att få ytterligare utfällning av DNAt tillsattes 1 droppe 3M natriumacetat-lösning. Blandningen mixades och fick stå i 30 minuter vid -20°C för att sedan centrifugeras vid 13000 rpm i rumstemperatur under 10 minuter. Supernatanten pipetterades bort och det kvarvarande innehållet tvättades med 75 % ethanol följt av centrifugering vid 13000 rpm i rumstemperatur under 10 minuter. Supernatanten pipetterades bort och pelleten torkades för att sedan lösas i 80 µl dH2O som slutligen förvarades vid -20°C. 2.6.1 PCR med gDNA som templat Vid PCR med gDNA användes gDNA från A.dracunculus samt A.annua som templat. Till ”PuReTaq™ Ready-To-Go-™ PCR beads”-rören tillsattes 22 µl dH2O, 1 µl forward primer, 1 µl reverse primer (Tabell I), samt 1 µl gDNA (1 µg). Den positiva kontrollen bestod av gDNA från A.annua och i den negativa kontrollen tillsattes dH2O som templat. För att amplifiera fragment av ADS, FDS, DBR2, HMGR och CYP71AV1 användes ett PCRprogram med inledande denaturering under 3 minuter vid 95°C, följt av 25 cykler innehållande 30 sekunder denaturering vid 95°C, annealing i 30 sekunder vid 60°C och extension i 30 sekunder vid 72°C. Detta följdes av en avslutande extension i 8 minuter vid 72°C, följt av kylning vid 4°C i ∞. När PCR-programmet avslutats tillverkades en 2,4 % agarosgel. Till en bägare tillsattes 1,2 g agarospulver samt 50 ml (50 g) 0,5x TBE-buffert. Lösningen hettades upp på 360W i en mikrovågsugn tills alla partiklar var lösta. Lösningen blandades sedan och varmt destillerat vatten tillsattes för att återfå rätt vikt (50 g). Lösningen mixades ordentligt och tillsattes till en gelform. När gelen stelnat blandades 10 µl PCRprodukt och 2 µl 6x Loading Buffer, vilket laddades i 11 av brunnarna på gelen. I tre av brunnarna tillsattes 5 µl DNA markör (Figur 9). 10 Gelen placerades i en elektroforesutrustning vid 100 V i 30 minuter. Sedan inkuberades gelen i 60 minuter i GelRed, följt av en bildanalys i en geldokumenteringsutrustning. 3. Resultat 3.1 PCR med FDS, HMGR och ADS primers PCR med cDNA från A. dracunculus som templat gav produkt för FDS (brunn 2) HMGR (brunn 3) samt den positiva kontrollen (brunn 5) vilken hade pJETADS-plasmid som templat. ADS amplifierades inte (figur 6, brunn 4). Möjligheten att starta biosyntesen av artemisinin är möjlig, men avsaknaden av ADS förhindrar processen. Figur 6. Agarosgel med 2 markörer, 5 PCR-produkter samt en cDNA från A. dracunculus (kontroll). Brunn 1: FastRulertm Ultra Low Range DNA Ladder. Brunn 2: FDS. Brunn 3: HMGR. Brunn 4: ADS. Brunn 5: Positiv kontroll. Brunn 6: Negativ kontroll. Brunn 7: Kontroll av cDNA och brunn 8: FastRulertm Ultra Low Range DNA Ladder. 3.2 PCR med fullängds ADS primers Amplifiering med fullängds primer visade ingen förekomst av ADS i de båda cDNApreparationerna (figur 7). Det fanns alltså inget ADS i cDNAt från A.dracunculus. Som positiv kontroll användes pJETADS-plasmid som kan ses i brunn 4 vid 1,6 kb. 11 Figur 7. Agarosgel med 2 markörer samt 4 olika PCR-produkter. Brunn 1: O´GeneRuler 1 kb DNA Ladder. Brunn 2: cDNA (amplifierat med fullängds ADS primers) från A.dracunculus. Brunn 3: cDNA2 (amplifierat med fullängds ADS primers) från A.dracunculus. Brunn 4: Positiv kontroll. Brunn 5: Negativ kontroll och brunn 6: O´GeneRuler 1 kb DNA Ladder. 3.3 PCR med ADS, FDS, DBR2, HMGR och CYP71AV1 primers I cDNAt för A.dracunculus amplifierades FDS (figur 8, brunn 3), HMGR (brunn 5) och CYP71AV1 (brunn 6) enligt förväntad storlek. cDNA för ¨övriga enzym (brunn 2 och brunn 4) amplifierades inte. I cDNAt från A.annua (som använts som positiv kontroll) amplifierades även ADS och DBR2 (alla enligt förväntad storlek) som krävs för biosyntesen av artemisinin. cDNAt från A.dracunculus saknar alltså ADS och DBR2 för att kunna genomföra biosyntesen av artemisinin. Figur 8. Agarosgel med 3 markörer samt 11 olika PCR-produkter. Brunn 2-6 innehåller cDNA från A.dracunculus och brunn 9-13 innehåller cDNA från A.annua som templat. Brunn 1: O´Generuler, 100 bp plus DNA. Brunn 2 och 9: ADS. Brunn 3 och 10: FDS. Brunn 4 och 11: DBR2. Brunn 5 och 12: HMGR. Brunn 6 och 13: CYP71AV1. Brunn 7: Negativ kontroll. Brunn 8 och 14: FastRulertm Ultra Low Range DNA Ladder. 12 3.4 PCR med genomiskt DNA som templat Med gDNA för A.dracunculus amplifierades FDS (figur 9, brunn 3), HMGR (brunn 5) och CYP71AV1 (brunn 6). Övriga enzym (ADS och DBR2) amplifierades inte. I gDNA för A.annua (som använts som positiv kontroll) amplifierades även ADS och DBR2 som krävs för biosyntesen av artemisinin. gDNA från A.dracunculus saknar alltså även generna för ADS och DBR2. FDS-fragmenten ampliferades som ett 200 bp fragment på både gDNA för A.dracunculus och gDNA för A.annua. I A.annua amplifierades även ADS runt 200 bp. Figur 9. Agarosgel med 3 markörer samt 11 PCR-produkter. Brunn 2-6, gDNA från A.dracunculus och brunn 9-13 gDNA från A.annua som templat). Brunn 1: GeneRuler 100 bp plus DNA Ladder. Brunn 2 och 9: ADS. Brunn 3 och 10: FDS. Brunn 4 och 11: DBR2. Brunn 5 och 12: HMGR. Brunn 6 och 13: CYP71AV1. Brunn 7 och 14: FastRulertm Ultra Low Range DNA Ladder. Brunn 8: Negativ kontroll. 4. Diskussion Syftet med studien var att med hjälp av biokemiska metoder undersöka eventuell förekomst av genuttryck hos enzymerna ADS, FDS, DBR2, HMGR och CYP71AV1 i A.dracunculus. Artemisinin är en aktiv substans i malariamedicin och utvinns främst ur växten A.annua. Mängden artemisinin som kan utvinnas ur A.annua är relativt liten, och är dessutom dyrt att framställa (9). Den här studien gick därför ut på att undersöka alternativa källor för utvinning av artemisinin, vilket skulle kunna bidra till att fler kan få tillgång till medicinen då prevalensen av malaria är hög bl.a. i fattiga delar av Afrika (1). 13 PCR är en effektiv men känslig metod som behöver optimeras för att fungera korrekt. Om inte rätt temperatur, tid och koncentration anpassats för preparaten som ska genomgå PCR kan önskade resultat utebli. För att få bästa möjliga resultat för de produkter som skulle erhållas i studien, justerades temperatur, tid och koncentration för att få fram optimala förhållanden (22). För att underlätta amplifiering användes främst primers för korta DNA-sekvenser. Ett undantag var figur 6 där primers för hela ADS cDNAt användes. Korta DNA-sekvenser minskar risken för att få med introner vid amplifiering av gDNA. För att biosyntesen av artemisinin ska kunna starta krävs enzymerna FDS och HMGR. Därför analyserades cDNA från A.dracunculus (Figur 5) där fragmenten av FDS och HMGR amplifierades. Båda fragmentbanden för enzymerna låg enligt förväntad längd på 92 bp, respektive 136 bp (Tabell I). Förekomst av FDS och HMGR gör det möjligt för biosyntesen av artemisinin att starta. FDS och HMGR förekommer naturligt i växter (10) och att enzymerna påträffats säkerställer därmed inte att artemisinin förekommer i växten. För att fastställa eventuell förekomst av ADS analyserades cDNA från A.dracunculus med fullängds primers (Figur 6). ADS amplifierades inte i cDNAt och med frånvaro av ADS kan biosyntesen av artemisinin inte genomföras och bildning av artemisinin kan därmed inte slutföras. Resultatet där ADS, FDS, DBR2, HMGR och CYP71AV1 undersöktes i cDNAt från A.dracunculus (Figur 7) amplifierades FDS, HMGR och CYP71AV1. Även CYP71AV1 är ofta naturligt förekommande i växter, vilket gör att detta enzym tillsammans med FDS och HMGR bör finnas även i A.dracunculus (10). Samtliga enzym som amplifierades från A.dracunculus låg enligt förväntad längd (Tabell I). ADS och DBR2 amplifierades inte. DBR2 är, liksom ADS, ett viktigt enzym i biosyntesen av artemisinin och frånvaro av dessa förhindrar bildning av artemisinin (13). De positiva kontroller som använts bestod antingen av cDNA från A.annua, där samtliga enzymerna amplifierades och återfanns vid rätt längd (Tabell I, Figur 7, 8) eller pJETADS som amplifierats enligt fragmentlängden på ADS (Figur 5, 6). De negativa kontrollerna amplifierades inte, vilket indikerar att kontaminering kan exkluderas. Enligt artikeln Mannan et al. har man hittat förekomst av artemisinin i A.dracunculus (0,27 ± 0 %) med separationsmetoden HPLC (15). I den här studien påvisades dock inte genuttrycket av enzymerna ADS och DBR2 i A.dracunculus, vilket motsäger resultatet i tidigare studier eftersom dessa enzymer krävs för bildning av artemisinin. Det positiva resultatet av artemisinin i tidigare studier kan bero på kontaminering som då påvisar felaktig förekomst av artemisinin. A.dracunculus genomet är ej sekvenserat och därmed ej känt. Detta faktum skulle kunna medföra att primersekvenserna för ADS och DBR2 är annorlunda vid targetsite och kommer därmed inte att amplifieras vid utförandet av PCR. Detta är dock högst osannolikt då övriga enzym i A.dracunculus återfinns med samma sekvens i targetsite i 14 generna som för enzymerna i A.annua (Figur 7). För att säkerställa att ADS och DBR2 inte förekommer i A.dracunculus, extraherades även genomiskt DNA eftersom möjligheten finns att ADS och DBR2 kan uttryckas i ett annat stadie av växtens utveckling. Extrahering av genomiskt DNA utfördes därför för att se om generna finns i A.dracunculus. Resultatet av amplifierat gDNA från A.dracunculus (Figur 8) visade fragment av FDS, HMGR och CYP71AV1. ADS och DBR2 amplifierades inte. Fragmentlängden för FDS var runt 200 bp i både A.dracunculus och A.annua. Då sekvensen för FDS ännu inte är fastställd finns möjligheten att genen för FDS innehåller ett intron. I FDS-provet hittades även extraband. Den positiva kontrollen bestod av gDNA från A.annua. PCR-produkten för ADS påvisade ett ca 200 bp fragment. Hela genen för ADS är nyligen sekvenserad (Genbank FJ432667) och vid target site finns ett intron på 114 bp som ger en slutlig fragmentlängd på 209 bp. Det finns därför en chans att även FDS-sekvensen innehåller intron. Övriga gensekvenser för de enzymer som ingick i den positiva kontrollen återfanns vid förväntad längd. Den negativa kontrollen amplifierades ej vilket indikerar att kontaminering kan exkluderas. I flera geler (Figur 5, 6, 7 och 8) uppstod primeröverskott. Detta beror troligtvis på att de primers som använts varit i för hög koncentration. Slutsats Målet med studien var att undersöka förekomst av genuttryck hos de enzymer som ger upphov till den aktiva substansen artemisinin i malarialäkemedel. Artemisinin syntetiseras och ackumuleras i A.annua i väldigt små mängder vilket gör det omöjligt att bota alla som drabbats av malaria. Att finna andra arter av Artemisia släktet som eventuellt kan producera mer artemisinin är därför av intresse. I denna studie undersöktes A.dracunculus för att finna gener samt genuttryck av de enzymer som är essenstiella för biosyntesen av artemisinin. Resultaten visar att nyckelenzym som ADS och DBR2 troligen inte existerar i A.dracunculus trots att tidigare studier påvisat förekomst av artemisinin. Ytterligare forskning och kunskap krävs för att på längre sikt få ökad utvinning av den viktiga substansen artemisinin och på så sätt kunna minska förekomsten av malaria. 15 Tack Först och främst vill jag tacka Peter Brodelius som gett mig möjligheten att utföra detta projekt. Till Anneli Lundgren vill jag säga tack för all hjälp, stöd, råd, inspiration och motivation du givit mig. Utan dig hade jag inte kunnat utföra detta projekt. Jag vill även tacka Ke Yang som ställt upp och svarat på mina frågor när Anneli inte kunnat närvara. 16 5. Referenslista 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. 18. 19. Nayyar GM, Breman JG, Newton PN, Herrington J. Poor-quality antimalarial drugs in southeast Asia and sub-Saharan Africa. Lancet Infect Dis. 2012 Jun;12(6):488-96. 10 facts on malaria [Internet]. World health organization2014 [cited 05/26]. Available from: http://www.who.int/features/factfiles/malaria/en/. Lokal_Profil [CC-BY-SA-2.5 (http://creativecommons.org/licenses/by-sa/2.5)], via Wikimedia Commons [Internet]. Bartoloni A, Zammarchi L. Clinical aspects of uncomplicated and severe malaria. Mediterr J Hematol Infect Dis. 2012;4(1):e2012026. Johnston GL, Smith DL, Fidock DA. Malaria's missing number: calculating the human component of R0 by a within-host mechanistic model of Plasmodium falciparum infection and transmission. PLoS Comput Biol. 2013 Apr;9(4):e1003025. Taylor WR, Hanson J, Turner GD, White NJ, Dondorp AM. Respiratory manifestations of malaria. Chest. 2012 Aug;142(2):492-505. CDC/Alexander J. da Silva, PhD/Melanie Moser [Public domain], via Wikimedia Commons [Internet]. Miller LH, Su X. Artemisinin: discovery from the Chinese herbal garden. Cell. 2011 Sep 16;146(6):855-8. Cook SP. The quest for affordable artemisinin. Future Med Chem. 2013 Mar;5(3):233-6. Olofsson L, Engstrom A, Lundgren A, Brodelius PE. Relative expression of genes of terpene metabolism in different tissues of Artemisia annua L. BMC Plant Biol. 2011;11:45. Brown GD, Sy L-K. In vivo transformations of dihydroartemisinic acid in Artemisia annua plants. Tetrahedron. 2004 1/26/;60(5):1139-59. Olsson ME, Olofsson LM, Lindahl A-L, Lundgren A, Brodelius M, Brodelius PE. Localization of enzymes of artemisinin biosynthesis to the apical cells of glandular secretory trichomes of Artemisia annua L. Phytochemistry. 2009 6//;70(9):1123-8. Wang H. Studies on the expression of enzymes related to the artemisinin biosynthesis in Artemisia annua L. Växjö: Linnaeus University Press; 2013. 65 s. p. Wang H, Han J, Kanagarajan S, Lundgren A, Brodelius PE. Trichome-specific expression of the amorpha-4,11-diene 12-hydroxylase (cyp71av1) gene, encoding a key enzyme of artemisinin biosynthesis in Artemisia annua, as reported by a promoter-GUS fusion. Plant Mol Biol. 2013 Jan;81(1-2):119-38. Mannan A, Ahmed I, Arshad W, Asim MF, Qureshi RA, Hussain I, et al. Survey of artemisinin production by diverse Artemisia species in northern Pakistan. Malar J. 2010;9:310. Ribnicky DM, Poulev A, Watford M, Cefalu WT, Raskin I. Antihyperglycemic activity of Tarralin™, an ethanolic extract of Artemisia dracunculus L. Phytomedicine. 2006 9/11/;13(8):550-7. A Method for Extracting High-Quality RNA from Diverse Plants for Next-Generation Sequencing and Gene Expression AnalysesRoxana Yockteng, Ana M. R. Almeida, Stephen Yee, Thiago Andre, Colin Hill, and Chelsea D. SpechtApplications in Plant Sciences 2013 1 (12), 1300070. Gene Expression [Internet]. NCBI: The National Center for Biotechnology Information; 2014 [cited 05/27]. Available from: https://www.ncbi.nlm.nih.gov/projects/genome/probe/doc/ApplExpression.shtml. cDNA synthesis system [Internet]. invitrogen.com: Invitrogen life technologies; [cited 5/8]. Available from: http://tools.lifetechnologies.com/content/sfs/manuals/18267.pdf. 17 20. 21. 22. 23. 24. Oligo(dT)12-18 primer [Internet]. Invitrogen.com: Invitrogen; [cited 05/20]. Available from: http://www.lifetechnologies.com. Plant DNA extraction [Internet]. invitrogen.com: Invitrogen life technologies; [cited 5/8]. Available from: http://www.lifetechnologies.com/se/en/home/life-science/dna-rnapurification-analysis/dna-extraction/genomic-dna-extraction/plant-dna-extraction.html. McPherson MJ, Møller SG. Pcr. 2. ed. Abingdon: Taylor & Francis; 2006. 292 s. p. Polymerase chain reaction / PCR [Internet]. 2013 [cited 03-20]. Available from: http://www.nature.com/scitable/definition/polymerase-chain-reaction-pcr-110. Sciences GHL. PuReTaq™ Ready-To-Go-™ PCR beads [Internet]. 2014. Available from: http://www.gelifesciences.com/webapp/wcs/stores/servlet/productById/en/GELifeSciences/ 27955701. 18