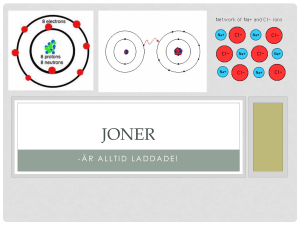
Periodiska systemet
advertisement

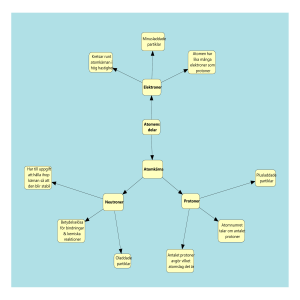
Periodiska systemet • Grupp 1 Alkalimetallerna. Har 1 valenselektron. Reagerar häftigt med vatten. T.ex. natrium och väte. • Grupp 2 Alkaliska jordartsmetaller. Har 2 valenselektroner. Reagerar häftigt med syror. T.ex. kalcium och magnesium. • Grupp 7(17) Halogenerna. De har 7 valenselektroner. Reagerar mycket lätt med andra ämnen och bildar ofta salter. Har en stickande lukt. Har färg i gasform. T.ex. Fluor och klor. • Grupp 8 (18) Ädelgaserna. Har fullt yttre skal. Reagerar ogärna. T.ex. helium och neon. Atomnummer • • • • I periodiska systemet En karta över alla kända grundämnen Alla atomer har ett atomnummer Atomnumret talar om hur många protoner det finns i atomkärnan Masstal • Antalet neutroner och protoner sammanlagt. Det ökar med stigande atomnummer eftersom ju större atom desto fler neutroner finns det i kärnan. Grupper De lodräta raderna i periodiska systemet anger antalet valenselektroner Atomen • Är neutral d.v.s. det finns alltid lika många protoner som elektroner i en atom • Elektroner är negativt laddade • Protoner är positivt laddade • Neutroner är neutrala Period De vågräta raderna talar om antalet skal , K,L,M,N,O,PQ Atom • I mitten av atomen finns en atomkärna. • Atomkärnan består av protoner (positivt laddade) och neutroner (ingen laddning, neutral). • Runt om kärnan kretsar elektroner (negativt laddade) • Det finns lika många protoner (positiva laddningar) som elektroner (negativa laddningar) i en atom. • Laddningarna tar alltså ut varandra och gör så att atomen i sin helhet är elektriskt neutral. Väteatom, H + Zinkatom molekyler • Två eller flera atomer som sitter ihop • Vanliga molekyler: H2O, CO2 O2, N2 • Siffran talar om hur många av atomslaget som sitter i hop Molekyl • När ett grundämne är bundet till ett annat grundämne kallas gruppen (den kemiska föreningen) för en molekyl. + + - + De gemensamma elektronerna kretsar då runt båda atomkärnorna Vatten, H2O Syre (O) Väte (H) Väte (H) Vatten, H2O + - -- + - 2 väteatomer, 2H -- -- --- ---- Syreatom, O -- Vattenmolekyl, H2O + - ---- - ---- - -- -- + - Metanmolekyl, CH4 + - - 4st Väteatomer, H - -- --+ - -- -- - Kolatom, C -+ - -- + - Syrgas, O2 -- -- ---- -- -- ----- -- - -- -- Dubbelbindning två elektroner kretsar runt båda atomkärno Kemiska beteckningar för molekyler • Varje atom betecknas med sitt kemiska tecken • Antal atomer betecknas efter atomens kemiska tecknet – CO2 (koldioxid) – CH4 (metan) • Antal molekyler betecknas innan molekyl beteckningen – 2 CO2 – 3 CH4 VAD ÄR DET FÖR SKILLNAD PÅ 2O OCH O2? • 2 O betyder att det finns två syreatomer. • O2 betyder att syreatomerna sitter ihop i en kemisk förening, molekyl. VAD ÄR DET FÖR SKILLNAD PÅ 2O OCH O2? • 2 O betyder att det finns två syreatomer. • O2 betyder att syreatomerna sitter ihop i en kemisk förening, molekyl. Kemisk reaktion • Nya ämnen bildas genom att molekylerna sätts ihop eller tas isär. • Atomerna försvinner aldrig! Lika många atomer finns innan och efter reaktionen. • En kemisk reaktion kan beskrivas med en reaktionsformel Ämne + Ämne Nytt Ämne Kemisk reaktion Knallgas + värme bildar vatten O2 + 2H2 2H2O Kemisk reaktion mellan magnesium och syre Kemisk reaktion mellan järn och svavel REAKTIONSFORMEL När man skriver en reaktionsformel använder man ämnenas kemiska tecken. Fe + S FeS • Det ska alltid finna lika många atomer av varje grundämne på båda sidor om pilen! • En järnatom + en svavelatom en järnsulfidmolekyl • FeS Fe + S Om vi vill skriva reaktionsformeln för järn (Fe) och svavel (S) går vi tillväga på följande sätt: • Steg 1: Fe + S – Skriv de ämnen du har från början (Fe och S) – Sätt ett plustecken mellan ämnena. • Steg 2: Fe + S – Rita en pil efter ämnena • Steg 3: Fe + S FeS – Till höger om pilen skriver du det eller de ämnen som bildats. • Reaktionsformeln för när magnesium brinner i syre: • 2Mg + O2 2MgO • Varför ser formeln ut så? • 2Mg + O2 2MgO • Syre förkommer i luft som en gas, syrgas, vilket betyder att syret är bundet till ett annat syre. • Syrgas består av syremolekyler och ska därför skrivas O2. • Vid reaktionen delar syremolekylen upp sig till två syreatomer 2Mg + O2 2MgO • Syreatomerna förenar sig sedan med varsin magnesiumatom. • Nytt ämne som har bildats kallas magnesiumoxid (MgO). • 2 Mg + O2 2 MgO • Eftersom syret har två stycken syreatomer som sitter ihop i en molekyl på vänster sida om pilen så måste det finnas med två syreatomer även på höger sida om pilen. • För att det ska vara jämvikt och reaktionen kunna äga rum måste det finnas lika många magnesiumatomer som syreatomer, eftersom att det är syret och magnesiumet som reagerar. • Därför sätter man dit en 2:a framför Mg. En annan kemisk reaktion Joner- hur bildas de? • Om atomer krockar så flyttar elektroner över från en atom till en annan och elektriskt laddade joner bildas. Vad är Joner • Joner är partiklar med en elektrisk laddning. • Skapas genom att en atom antingen tar upp eller avger elektroner (e-). • En positiv jon bildas genom att en atom avger en eller flera elektroner. • En negativ jon bildas genom att en atom tar upp en eller flera elektroner. • Exempel på joner är: – Li+ Litiumjon – laddning 1+ – Mg2+ Magnesiumjon – laddning 2+ – ClKloridjon – laddning 1– O2Oxidjon – laddning 2- Positiva joner • Atomer med få valenselektroner (elektroner i sitt yttersta skal) kan släppa iväg de elektronerna och få en ädelgasstruktur. • Då bildas positiva joner eftersom de har fler positiva protoner i kärnan än negativt laddade elektroner i skalen. M L K L K 11p+ Natriumatom 11p+ Natriumjon, Na+ + 1 elektron Negativa joner • Atomer med många valenselektroner (elektroner i det yttersta skalet) kan ta upp elektroner och få ädelgasstruktur. • Då bildas negativa joner eftersom de har fler negativt laddade elektroner i skalen än positivt laddade protoner i kärnan. L L K K 11p+ Syreatom + 11p+ 2 elektroner Oxidjon, O2- Sammansatta joner • Det är inte bara atomer som kan släppa iväg eller ta upp elektroner. Det kan även hela molekyler – sådana kallas för sammansatta joner. • En av de vanligaste är hydroxidjonen, OH-. Den består av en syreatom och en väteatom som tillsammans har en extra elektron och därmed laddningen 1-. Jonbindning • Joner med motsatt laddning kan bilda ämnen med väldigt starka bindningar – jonbindningar. • Salter är exempel på ämnen som hålls ihop med hjälp av jonbindningar. • Salter är därför ofta hårda kristaller med höga smältpunkter. • Vanligt koksalt (natriumkklorid) måste värmas till 801 ºC innan det smälter. Vanliga joner i salter… Vanliga positiva joner i salter • • • • Natriumjon, Na+ Kaliumjon, K+ Kalciumjon, Ca2+ Järnjon, Fe2+eller Fe3+ Vanliga negativa joner i salter • • • • Kloridjon, ClNitratjon, NO3Sulfatjon, SO42Karbonatjon, CO32-