File
advertisement

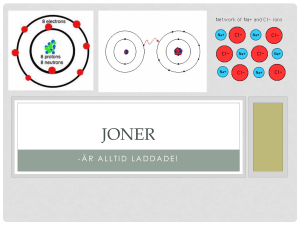
Periodiska systemet • Varje grundämne har en kemisk beteckning, t.ex. H=väte eller O=syre • Atomnummer – antalet protoner och även antalet elektroner • Atommassan – massan hos en atom av grundämnet • Man skiljer på metaller och icke metaller • http://www.ptable.com/?lang=sv Ädelgaserna • Finner vi i grupp 18 längst till höger i det periodiska systemet. • Är de ämnen där atomen har fullt yttersta skal. • Alla ämnen vill uppnå ”ädelgasstruktur”, det får de genom att fylla sitt yttersta skal på olika sätt. • Ädelgaserna varken reagerar med andra ämnen eller bildar molekyler med varandra, de är redan nöjda. • Ädelgaserna är: - Helium (He), universums näst vanligaste grundämne. - Neon (Ne), främst i lysrör och vissa lampor. - Argon (Ar), t.ex. skyddsgas vid svetsning. - Krypton (Kr), används i vissa glödlampor. - Xenon (Xe), används i blixtlampor. - Radon (Rn), har ingen praktisk användning. Är farlig och kan ge lungcancer, finns i marken och kan ta sig upp i hus. Elektronparbindning – kovalent bindning • Innebär att två atomer delar på två elektroner – ett elektronpar • Genom elektronparbindning uppnår de ädelgasstruktur eftersom de delar på elektroner som då kan fylla deras yttersta skal. • Atomer som håller ihop med elektronparbindning bildar molekylföreningar - T.ex. vätgas, klorgas och vatten. Joner • Ännu ett sätt att uppnå ädelgasstruktur! • Elektriskt laddade atomer kallas joner • Protonerna i kärnan håller kvar elektronerna, men e- är lättrörliga och en eller flera e- kan lämna en atom helt. Den som avlämnar e- får fler p+ och blir positivt laddad Den som får/tar upp e- får fler e- och blir negativt laddad - De har blivit elektriskt laddade! De får nu andra egenskaper, kan bl.a. leda ström. • Atomerna väljer alltid det lättaste alternativet, om de bara har en valenselektron släpper de hellre den än att ta till sig 7, det går åt mindre energi! Väteatom Vätejon