Atomen, periodiska systemet och kemiska reaktioner
advertisement

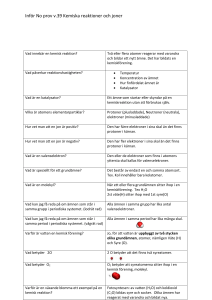
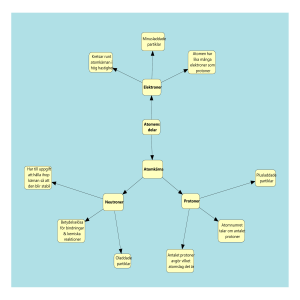
GRUNDLÄGGANDE kemi Att kunna till provet Atomer Grundämne = Pyttesmå byggstenar som allting är uppbyggt av. Atomer kan se olika ut. = Ett ämne som bara består av en sorts atomer. Molekyler Kemisk förening = Två eller flera atomer som sitter ihop. = Ämnen som innehåller olika sorters atomer. Jon H2O = en atom eller molekyl som har ett överskott eller underskott av elektrisk laddning. Den har alltså inte lika många elektroner som protoner. = Kemisk beteckning för en vattenmolekyl H står för väte (Hydrogen) och O står för syre (Oxygen) H H O Atomer, joner, grundämnen Atomer: Atomer är de ofattbart små byggstenar som allting är uppbyggt av. Atom betyder ”odelbar”. I atomkärnan hittar vi positiva protoner och neutrala neutroner. Utanför atomkärnan sitter elektronskalen. I dessa skal kretsar elektronerna. Elektron: negativ laddning (–) Proton: positiv laddning (+) Neutron: ingen laddning I en kemisk reaktion är det bara elektronerna som deltar. Antingen hoppar en eller flera elektroner iväg till en annan atom eller så tillkommer elektroner. Bilden visar en heliumatom. En atom har alltid lika många protoner som elektroner. Om antalet är olika har vi en jon. En positiv jon har fler protoner än elektroner. En negativ jon har fler elektroner än protoner. Grundämnen: Grundämnen består av en enda sorts atomer. Det finns strax över 100 grundämnen. Dessa kombineras på olika sätt för att bilda allting omkring oss. Antalet protoner i atomkärnan bestämmer vilket grundämne det är! Varje grundämne har ett eget namn. De har också en egen kemisk beteckning. Till exempel: grundämnet som har 1 proton heter väte. Den kemiska beteckningen för väte är H. En molekyl består av två eller flera atomer som sitter ihop. Vätemolekylen består av 2 stycken väteatomer. På kemispråket skriver man detta H2 OBS! De grundämnen ni ska kunna den kemiska beteckningen på är inringade i periodiska systemet nedan. Kemiska föreningar: Kemiska föreningar består av olika sorts atomer. Ett exempel är vatten, vars molekyl skrivs H2O. Joner: En positiv jon har fler protoner än elektroner. Den har lämnat ifrån sig elektroner och därför blivit positivt laddad. Exempel: En kopparjon skriver man Cu2+ Plustecknet berättar att jonen är positiv och 2:an visar att den har 2 protoner fler än elektroner. En negativ jon har fler elektroner än protoner. Den har tagit upp elektroner och blivit negativt laddad. Exempel: En kloridjon skriver man ClMinustecknet visar att den är negativ och eftersom det inte står någon siffra framför så betyder det att den har 1 elektron mer än antalet protoner. ATOM – lika många protoner som elektroner NEGATIV JON – fler elektroner än protoner POSITIV JON – fler protoner än elektroner Kemiska reaktioner: En kemisk reaktion är när atomer eller joner reagerar med varandra och bildar nya ämnen med nya egenskaper. När man skriver en reaktionsformel måste det finnas lika många atomer på båda sidor om pilen. Exempel på en kemisk reaktion: natriumjon + kloridjon bildar natriumklorid Reaktionsformel: Na+ + Cl- NaCl Fysikalisk förändring: Vid en fysikalisk förändring bildas inget nytt ämne utan det ämnet man hade från början byter bara aggregationstillstånd (fas). Exempel är när vatten kokar eller is smälter. Att sammanföra ämnen: Blandning: När två ämnen blandas utan att reagera kemiskt med varandra. Till exempel sand blandas med socker. Lösning: En lösning är en klar vätska. Den bildas när ett ämne löses upp i en vätska, oftast vatten. Exempel på lösning: socker i vatten. Omättad lösning: det går fortfarande att lösa upp mer av ett ämne i vattnet. Mättad lösning: man har löst upp så mycket av ett ämne att det inte går att lösa upp mer, det blir kvar lite av ämnet på botten. För att kunna lösa upp mer av ämnet kan man värma vätskan. Slamning: En slamning är grumlig. Man kan se det uppslammade ämnet flyta runt i vätskan innan det samlas på botten eller ytan. Detta kallas sedimentering. Emulsion : är en blandning av två vätskor som inte löser sig i varandra. Ett exempel är när man har hällt olja i vatten. Legering: är en blandning av två eller flera metaller där den nya blandningen får andra egenskaper än usprungsmetallerna. Exempel: brons som är en blandning av koppar och tenn. Aggregationstillstånd: Aggregationstillstånd är namnet på de olika faser ett ämne kan befinna sig i. Värme är egentligen rörelse hos atomerna. Ju varmare det är, desto mer rör atomerna sig. När ett ämne är i fast form rör sig atomerna långsamt. Exempel på ämnen i fast form är järn och is. När ett ämne är flytande rör de sig snabbare Exempel på vätskor är vatten och bensin. När ett ämne är i gasform rör de sig jättefort och är långt ifrån varandra. Exempel på gaser är neon och koldioxid. Värme tillförs Värme avges Smältpunkt: Den temperatur där ett ämne övergår från fast till flytande form, det smälter Kokpunkt: Den temperatur där ett ämne övergår från flytande form till gasform, det förångas. Kondensation: Är när en gas övergår till flytande form. Exempelvis när vattenånga träffar en kallare yta och återgår till flytande. Stelning: När ett flytande ämne övergår till fast form, till exempel vatten fryser till is.