MALMÖ HÖGSKOLA 1(4) Teknik och samhälle Basåret Kemi III
advertisement

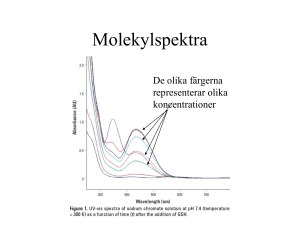
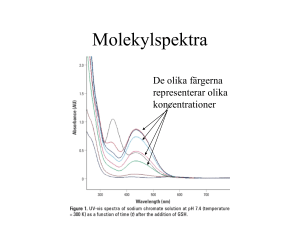
MALMÖ HÖGSKOLA Teknik och samhälle Basåret Kemi III 1(4) Laboration 3 BESTÄMNING AV PROTEINKONCENTRATION I OKÄNT PROV Bakgrund Biuretmetoden bygger på att kopparjoner i alkalisk lösning ger ett blåviolett komplex med kväveatomerna i proteinernas peptidbindningar. Genom att mäta absorbansen av peptidkomplexet kan man bestämma proteinkoncentrationen. Princip för absorbansmätning Ett metallkomplex absorberar ljus vid specifika våglängder. Detta kan utnyttjas vid koncentrationsbestämningar. Om våglängden för mätningen inte är angiven tas först ett spektrum upp för att bestämma våglängden för komplexets absorbansmaximum. Därefter mäts absorbansen för lösningar med kända proteinkoncentrationer vid denna våglängd och sedan ritas en kalibreringskurva. Genom att mäta absorbansen för prov med okänd koncentration kan koncentrationen bestämmas ur kalibreringskurvan. Se appendix. Lösningsberedning Biuretreagens: 0,15 g CuSO4.5H2O (Finns färdig) 0,6 g natriumkaliumtartrat löses i 50 ml destillerat vatten 30 ml nyberedd 10 % NaOH tillsätts späd till 100 ml med destillerat vatten. Proteinstamlösning: Proteinlösning med koncentrationen 80 mg protein/cm3 (finns färdig). Utförande Bered med hjälp av proteinstamlösningen och 0,10 % NaCl-lösning fyra kalibreringslösningar som innehåller 2,0 - 4,0 - 6,0 och 8,0 mg protein/ml. Använd 20 eller 25 cm3 mätkolvar vid spädningen. Samtliga lösningar späds från stamlösningen, 80 mg/ml. Dessa 4 lösningar tillsammans med ett 0-prov (se nedan) används för att ta upp en kalibreringskurva. Provberedning för kalibreringslösningarna och okänt prov utföres samtidigt enligt beskrivning nedan: 0,5 cm3 av vardera proteinlösningen (4 st.), 0-provet (= 0,5 cm3 0,10 % NaCl) och 0,5 cm3 lösning av okänt prov, som beretts på samma sätt som kalibreringslösningarna sätts till vardera två märkta provrör (dubbelprov). Tillsätt 3 cm3 Biuretreagens till varje provrör (totalt 12 st. provrör). Blanda väl. Låt färdigblandad lösning stå i minst 15 min före absorbansmätningen. För att nollställa spektrofotometern används destillerat vatten. Detta kallas för blank. Labhandledaren demonstrerar handhavandet av spektrofotometern. Mät absorbansen för samtliga lösningar vid 540 nm, även det okända provet. Beräkningar Subtrahera 0-provets absorbans från var och en av proteinlösningarnas absorbanser. Rita upp en kalibreringskurva genom att i ett diagram avsätta de på detta sätt beräknade absorbanserna för kalibreringslösningarna mot dess halter. Avläs det okända provets halt ur kalibreringskurvan. 1 MALMÖ HÖGSKOLA Teknik och samhälle Basåret Kemi III 2(4) Laboration 3 APPENDIX Spektrofotometrisk mätning En lösnings färgintensitet beror på arten och koncentrationen av det färgade partikelslaget samt på tjockleken av lösningsskiktet. Med ögats hjälp kan man göra en uppskattning av en färgad lösnings koncentration genom att jämföra den med en lösning vars koncentration är känd. Om man i stället for ögat använder en fotocell som objektivt registrerar färgintensiteter, får man ett mycket noggrannare resultat. Metoden grundar sig på mätning av lösningars absorption av ljus. Instrumentet som används kallas en spektrofotometer. Spektrofotometern kan konstrueras så att den kan användas utanför det synliga våglängdsområdet. Man får då möjlighet att analysera ofärgade ämnen som absorberar strålning i det ultravioletta eller infraröda våglängdsområdet. Våglängden anges vanligen i nanometer (1 nm = 10-9 m). Synligt ljus har våglängder mellan 400 nm och 750 nm. Man arbetar ofta inom ett smalt våglängdsområde, monokromatiskt ljus. När monokromatiskt ljus passerar en lösning absorberas en del av strålningen. Om intensiteten for det infallande ljuset är I0 och intensiteten för det utträdande ljuset är I gäller Lambert-Beers lag: A = log(I0/I) = .c.l (se härledning nedan) Formler Beteckningar: I0 I l c T A E intensitet hos det infallande ljuset intensitet hos det utgående ljuset den sträcka ljusstrålen går genom lösningen (cm) lösningens koncentration (M) transmittans (ev. %) absorbans (absorbansenheter, Abs.) molara absorptiviteten (M-lcm-l) ljusets våglängd (nm) Figur 1. Transmittans. Transmittansen, T, är förhållandet mellan det utgående och det infallande ljusets intensitet: T = (I/I0) (Vill man uttrycka transmittansen i procent får man multiplicera kvoten (I/I0) med 100.) Absorbans är den mest använda storheten vid spektrofotometriska mätningar. Anledningen är att absorbansen är direkt proportionell mot koncentrationen, vilket leder till en rät linje när man ritar absorbansen som funktion av koncentrationen. För att få absorbansen skall man logaritmera det inverterade värdet av transmittansen: A = log(1/T) = log(I0/I) För absorbansen gäller Lambert-Beers lag: A = .C.l, där konstanten = molära absorptiviteten och C ges i mil/dm3. Används annan enhet på koncentrationen anges konstanten a som den specifika absorptiviteten. (A = a·C·l) 2 MALMÖ HÖGSKOLA Teknik och samhälle Basåret Kemi III 3(4) Laboration 3 Ljusets sträcka, l, genom lösningen är oftast lika med 1 cm i en vanlig kyvett. , den molara absorptiviteten är konstant förutsatt att ljusets våglängd, lösningsmedlets art eller lösningens temperatur inte ändras. Absorbansen är ett relativt tal och saknar enhet. Spektrofotometern kan ge mätresultat både i absorbans- och transmittansenheter. Vid höga absorbanser (> 1 ungefär) absorberas nästan allt ljus. Endast en liten del når fram till detektorn och mätningarna blir osäkra dvs. Lambert-Beers lag slutar att gälla. Absorptionsspektrum I metodbeskrivningar är oftast den våglängd man skall mäta vid angiven. Skulle det inte vara så kan man bestämma en lämplig våglängd genom att variera våglängden och mäta absorbansen för den lösning man är intresserad av att analysera. Rita sedan absorbansen som funktion av våglängden i ett diagram. Figur 2. Absorptionsspektrum. Lämplig våglängd for mätningarna är den våglängd som motsvarar absorptionsmaximum på kurvan. Kalibreringskurva Man kan bestämma lösningens koncentration genom att jämföra lösningens absorbans med absorbansen hos några lösningar med kända koncentrationer, standardlösningar. Standardlösningar med kända koncentrationer bereds och absorbansen mäts vid en bestämd våglängd. Absorbansen för standardlösningarna avsätts mot koncentrationen för respektive lösning i ett diagram. Detta diagram kallas standardkurva eller kalibreringskurva. Nedan finns en schematisk kalibreringskurva där punkterna för standardlösningarna inte är utsatta. 3 MALMÖ HÖGSKOLA Teknik och samhälle Basåret Kemi III 4(4) Laboration 3 Figur 3. Kalibreringskurva. Punkterna bör ligga på en rät linje genom origo vars riktningskoefficient är den molara absorptiviteten, . Att linjen går igenom origo beror på att 0-provets absorbans subtraheras från samtliga prov inklusive det med koncentrationen 0 dvs. 0-provet. För ett okänt prov ger kalibreringskurvan koncentrationen genom att man avläser koncentrationen för den absorbans provet har visat vid analysen. Kyvetter Kyvetter används som behållare för vätskan när denna ska analyseras i spektrofotometern. De är precisionstillverkade och därför relativt dyra. De är känsliga för repor och fett. Rör aldrig vid de polerade ytorna utan ta alltid i övre delen av kyvetten. Kyvetter kan vara tillverkade i olika material t.ex. glas, kvarts eller plats. Olika material krävs vid mätningar vid olika våglängder p.g.a. materialet i kyvetterna absorberar ljus vid olika våglängder. För mätningar med UV-ljus användes kvartskyvetter vilka är cirka 5 gånger dyrare än glaskyvetter. Vis betyder visible (synligt) och står på glaskyvetter. Kyvetter med tjockare glas eller mindre volym användes om man endast har tillgång till en mindre provvolym. Strålens väg genom lösningen blir lika lång eftersom det är sidoväggarna som är tjockare eller mindre breda. Diskning sker normalt med destillerat vatten. Krävs noggrannare diskning kan man koka kyvetterna (glas och kvarts) i koncentrerad salpetersyra varefter de sköljs i destillerat vatten och etanol. Diskningen är speciellt viktig vid UV-mätningar. Matchning av kyvetter kan man göra om man behöver använda flera olika kyvetter i samma mätserie och vill arbeta mycket noggrant. Man nollställer spektrofotometern med en kyvett i strålgången. Sedan byter man ut denna och kontrollerar att apparaten visar noll även med de andra kyvetterna. På så sätt kan man välja ut kyvetter som stämmer överens, matchar varandra. 4