Sammanfattning, Inger Andersson
advertisement

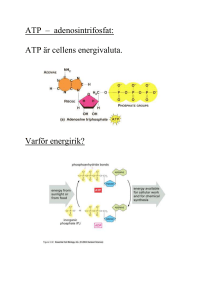
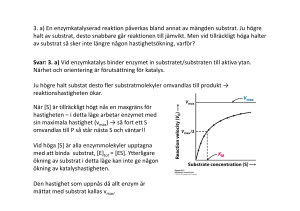
Tentamen Mi11/biokemi 23 november 2000, 08:15 - 1200. Med kortfattade svar. Detaljer mellan [] ej nödvändiga för full poäng. Max poäng = 32p. Gräns för godkänd = 17p (53%) 1. a) Glycin är den minsta aminosyran, dess sidokedja består endast av en väteatom. Vilken effekt har detta på huvudkedjans rotationsmöjligheter i en polypeptidkedja, jämfört med andra aminosyror? Med ledning av detta, vilka slutsatser kan man dra om var glycin oftast förekommer, i -helix, i strängar eller i böjar (loopar)? b) Glycins summaformel är C2H5O2N. Vad är summaformeln för en peptid som bildats av 10 glycinmolekyler? (3p) 2. a) Rita en Michaelis-Menten plot för ett hypotetiskt enzym (glöm inte att märka ut axlarna), och visa i skissen hur du bestämmer Michaelis-konstanten (Km) och maximala hastigheten (Vmax) för enzymet. b) Varför uppnås en maximal hastighet vid hög substratkoncentration? c) I ett experiment mäter du Km på 100 mM och Vmax enzymkoncentration på 20 nM. Beräkna kcat. d) En mutant av enzymet har samma kcat, men ett Km på 300 mM. Har mutanten högre eller lägre affinitet för sitt substrat? Förklara hur du kommer fram till ditt svar! (4p) 3. a) Förklara termerna ‘feedback’- och ‘feedforward’-reglering i samband med reglering av metaboliskt flöde. Använd gärna en enkel skiss för att förklara begreppen. b) Det glykolytiska enzymet fosfofruktokinas-1 (PFK-1) regleras av ATP, ADP och citrat. Redogör för var och en av dessa vilken sorts effektor det rör det sej om och om effektorn ökar eller minskar aktiviteten av PFK-1? (4p) 4. Hur kontrolleras glykolysen av citronsyracykeln? (2p) 5. Vad sker kemiskt under varje ‘runda’ av citronsyracykeln (vad produceras)? (2p) 6. ATP produceras i glykolysen, och till ännu högre grad i den process som kallas oxidativ fosforylering. Även om dessa processer båda resulterar i produktion av ATP, skiljer sej processerna åt principiellt. Vad är den principiella skillnaden i hur ATP produceras i glykolysen, och hur den produceras i oxidativ fosforylering? (4p) 7. Hur mäts kvantitativt reaktioner som använder NAD+/NADH som coenzym? (2p) 8. Vissa bakterier kan leva vid olika temperatur genom att förändra sammansättningen av lipider i sina membran. Varför är detta viktigt och vad är det som ändras? ß(3p) 9. Du har en blandning av två proteiner X och Y med följande egenskaper: Protein Molekylvikt (Dalton) Isoelektrisk punkt X 50,000 5.4 Y 53,000 9.5 Uppgiften är att separera X från Y för att vidare kunna använda X i ditt forskningsarbete. Du studerar X och Y:s egenskaper i tabellen och bestämmer dig för att använda en jonbytare. a)Varför är jonbyteskromatografi en lämplig metod i detta fall? (2 p) b)Beskriv kortfattat hur du kan gå tillväga för att utföra försöket. Du har fri tillgång till separationsgeler, buffertsubstanser, tomma kolonner m.m. (2 p) 10. a) Var i växten sker fotosyntesens ljus- respektive mörker-reaktion? b) Vad kallas den primära ljusreceptorn (ljusmottagaren) i växter? c) Den primära ljusreceptorn i fotosystem I (PSI) skiljer sej inte kemiskt från den i fotosystem II (PSII). Trots detta har de dessa två fotoreceptorer något skilda egenskaper, t.ex. absorberar de ljus vid något skilda våglängder. Hur kan detta förklaras? d) Ett enzym i Calvincykeln är unikt för fotosyntetiserande organismer. Vilket enzym? Vilken/vilka reaktion(er) katalyserar enzymet? (4p) SVAR 1. a) Glycins minimala sidokedja ger aminosyran större rotationsfrihet än alla andra aminosyror. Glycin återfinns därför oftast i böjar (loopar). b) 10 * C2H5O2N - 9 * H2O = C20H32O11N10 2. a).Vmax är värdet av v0 som nås asymptotiskt vid höga substratkoncentrationer. Km är den substratkoncentration för vilken initiala hastigheten är lika med 1/2 Vmax. b) Vid mycket höga substratkoncentrationer är enzymet fullständigt mättat med substrat (alla aktiva ytor binder substrat), så att ingen ytterligare ökning av initialhastigheten (v0) är möjlig vid tillsats av mer substrat. Se skiss sid 127 i Horton. c) kcat = Vmax/[E] = 50 * 10-6 /20 * 10-9= 2 500 /min. d) Ett högre Km betyder att en högre substratkoncentration krävs för att uppnå halva maximala hastigheten. Det betyder i sin tur att enzymets affinitet för substratet är lägre. 3. a) En regulator (effektor) är en metabolit, som påverkar aktiviteten av ett metaboliskt enzym positivt eller negativt. [Effektorn kan vara en metabolit, som produceras i den metaboliska vägen, eller i en relaterad väg, eller en förening som är relaterad till cellens energiladdning, t.ex. ATP eller ADP]. En inhibitor (hämmare) hämmar aktiviteten av enzymet, medan en aktivator ökar enzymets aktivitet. Effektorer binder till ett regleringssäte, som är skilt från enzymets aktiva yta och kallas även allosteriska effektorer. En metabolit som kontrollerar ett enzym i en reaktion längre fram i reaktionsvägen utövar feedback kontroll, medan en metabolit som kontrollerar en reaktion längre fram i en metabolisk väg utövar feedforward kontroll. Se skiss sid 314 i Horton. b) ATP och citrat är negativa effektorer, ADP är en positiv effektor. Citrat (metabolit i citronsyracykeln) utövar feedback inhibering på fosfofruktokinas-1 medan ATP kan anses som antingen feedback eller feedforward inhibitor, beroende på om man betraktar endast PFKreaktionen eller ser till hela glykolysen. 4. När koncentrationen av ATP är hög i cellen (hög energiladdning) ackumuleras citrat i mitokondrien. Citrat, Som kan transporteras ut ur mitokondrien) inhiberar [två] enzymer i glykolysen [fosfofruktokinas and pyruvate kinas]. 5. Totalt oxideras en molekyl acetyl-CoA, produceras (spjälkas) två (eller 3 om man beaktar dekarboxyleringen av pyruvat) molekyler koldioxid (CO2), reduceras tre (eller fyra, om man beaktar dekarboxyleringen av pyruvat) molekyler NAD+ till NADH, samt en molekyl FAD till FADH2, samt fosforyleras en molekyl GDP till GTP. 6. ATP-produktion i glykolysen sker genom fosforylering på substratnivå, d.v.s. genom enzymatisk överföring av en fosfatgrupp från ett vattenlösligt substrat (sker i cytosolen) till ADP. Föreningar som på detta sätt kan avge sin fosfatgrupp kallas ibland superenergirika föreningar, I oxidativ fosforylering (som sker i mitokondriemembranet) kopplas i stället syntesen av ATP från ADP till oxidation av reducerade coenzymer (som i sin tur produceras genom oxidation av kolhydrater) till elektrontransporten i mitokondriernas membran. Elektrontransport från reducerat coenzym till O2 ger upphov till en elektrisk potential och pH-gradient över membranet, och energin från denna process används av enzymet ATP-syntas för att syntetisera ATP från ADP och oorganiskt fosfat (Pi). (2p) 7. NADH har ett absorptionsmaximum vid 340 nm, medan i NAD+ inte absorberar vid den våglängden. Enzymaktivitet kopplad till NAD+/NADH kan därför mätas genom att spektrfotometriskt mäta ändringen i absorbans (1.5p) vid 340 nm (0.5p). Se laboration 4. Alternativa svar som också givits poäng är mätning av redoxpotential (1p) eller pH-mätning (1p). Observera dock att i det senare fallet bör mätningen göras i obuffrad lösning. 8. Det är viktigt att membranet behåller rätt fluiditet för att bland annat membranproteiner skall kunna fungera på rätt sätt (1p). Detta kan främst åstadkommas genom att variera fettsyrornas längd och halt av omättnad i membranlipiderna. (2p). 9. a) Proteinerna X och Y har stor skillnad i isoelektrisk punkt (1p) vilket i detta fall innebär att de bör ha olika laddning vid neutralt pH. Proteinerna bör därför kunna separeras med hjälp av jonbyteskromatografi. (En annan möjlig metod är preparativ elektrofores men den kan vara svårare att utföra i praktiken särskilt om större utbyten önskas.) Metoder baserade på storleksseparation som t.ex. gelfiltrering är mindre lämpligt (1p) då X och Y:s molekylvikter ligger mycket nära varandra. b) Tillverka en kolonn innehållande en separationsgel med en positivt laddad ligand t.ex. DEAE (0.5p). Jämvikta gelen med en lämplig buffert vilken bör ha ett pH mellan 7 och 8 (0.5p) samt låg jonstyrka (0.5p). Tillsätt provet i nästa steg. Vid detta pH bör X vara negativt laddad och Y positivt laddad. X som ska renas fram binder alltså till liganden medan Y bör gå rakt igenom. X kan elueras i nästa steg genom att jonstyrkan höjs (0.5p)antingen stegvis eller med hjälp av en saltgradient. 10. a) Ljusreaktionen i kloroplasternas tylakoidmembran (0.5p) och mörkerreaktionen i kloroplasternas stroma (0.5p). b) Klorofyll (1p). c) De binder till olika proteiner. Den nära protein-omgivningen modulerar klorofyllets absorptionsspektrum (1p). d) Enzymet Rubisco (0.5p): (ribulos-1,5-bisfosfat karboxylas/oxygenas) katalyserar fixering av atmosfärisk koldioxid till ribulos-1,5-bisfosfat (RuBP) (0.25p). Enzymet katalyserar dessutom oxygenering (0.25p) av RuBP i en reaktion som tävlar med karboxyleringsreaktionen.