Analys_av_kolhydrater_och_proteiner
advertisement

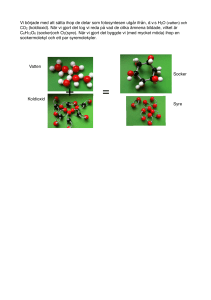
Analys av olika kolhydrater Teori: Ordet ”socker” kan ha olika betydelser. Socker i kaffet eller te heter sackaros. Mjölk innehåller socker som kallas mjölksocker eller laktos. Potatis, ris och pasta innehåller sockerarten stärkelse. Diabetessjuka testar sitt blod för ”socker” som egentligen är glukos. Du kommer lära dig hur man kan skilja på ”socker” men det kommer även i denna laboration att finnas ett protein. Material: 0,01% lösningar av stärkelse, protein, laktos, sackaros och glukos. Testa även fruktjuicer, mjölk och mjölkprodukter. Fehlings lösning I: 7 g CuSO4?. 5H2O i 100cm3 avjon.vatten Fehlings lösning II: 35 g C4H4KNaO6.4H2O (K,Na-tartrat) och 10 g NaOH i 100cm3 avjon.vatten. Vid användning blanda lika mängder av Fehlings lösningarna I och II. Lugol´s lösning: 1 g jod( I2) och 2 g KI i 50 cm3 avjon.vatten. Coomassie Brilliant Blue från Biorad. (färdig lösning innehåller fosforsyra och metanol) EnzyPlus EZS 962+ laktos/D-glukos från Biocontroll eller sockermätare som diabetiker använder. Vattenbad, provrör, pipetter Risker vid experimentet: Kopparjoner är miljöfarligt, natriumhydroxid är frätande, jod färgar huden. För Coomassie Brilliant Blue gäller att fara kan inte uteslutas - tillämpa försiktighetsprincipen. En fullständig riskbedömning ges av undervisande lärare. Utförande: Bestämning av socker, stärkelse och protein med Fehlings lösningar 1. Du får (eller hämtar) 5 provrör med olika sockerlösningar och ett med protein märka med A till E. 2. Märk upp 5 nya rör och pipettera ca 1 cm3 från varje rör A – E.. Tillsätt 5 drp av en blandning av Fehlings I och II. 3. Värm rören på ett vattenbad i ca 5 minuter eller tills en färgreaktion har skett. Röd färg av koppar(I)oxid indikerat på reducerande sockerart tex. fruktos, glukos eller laktos. Svagt violett lösning tyder på protein (Biuretreaktionen) Bestämning av stärkelse med Lugols lösning 4. Pipettera ca 0,5 cm3 5 rör A-E i nya provrör. Tillsätt 50 μl Lugols lösning till varje rör. Lugols lösning är en indikator på stärkelse. Jod ger med stärkelse en blå färg med stärkelemolekylen då den dras till stärkelsens inre hydrofoba spiralform. Monosackarider såsom glukos och fruktos eller disackarider som sackaros och laktos påverkas ej jod. Proteinbestämning med Coomassi blue. 5. Pipettera 50 μl av rör A-E i nya provrör. Tillsätt 800 μl vatten och 200 μl Coomassi blue. Proteiner bildar en blå färg som bestämmas i en spektrofotometer vid 595 nm. Enzymatisk bestämning av socker Teori: Innehåller i de provrör som visat sig vara reducerande socker arter går nu vidare för att avgöra vilket som är glukos och laktos. Laktos hydrolyseras av enzymet β-galaktosidas till D-galaktos och D-glukos. I närvaro av ATP(adenosin-5-trifosfat); sätts en fosforgrupp på D-glukosen till glukos6-fosfat. Samtidigt bildas ADP ((adenosin-5-difosfat). Glukos-6-fosfat oxideras av glukos-6-NADP till NADPH. Mängden NADPH som bildas är stökiometriskt mot den mängd laktos som fanns i provet. Halten bildad NADPH mäts spektrofotometriskt med en ökad absorbans vid 340 nm. 6. Utförande: Du har två rör med socker som visat sig vara reducerande sockerarter. Dessa kallas 1 och 2. 7. Märk 4 rör 1+, 1-, 2+ och 2-. Tillsätt 100 μl fosfatbuffert pH 6,6 (R4b) i alla 4 rören. Tillsätt sedan 5 μl β-galaktosidas i rören märkt med (+) alltså 1+ och 2+. Men inte i 1och 2-. 8. Tillsätt 100 μl av socker 1 i rören märkta 1+ och 1-. Samt socker 2 i 2+ och 2-. Ställ rören i vattenbad på 370C i 30 minuter. Lakotsen hydrolyseras 9. Efter inkubationen tillsätt 1 cm3 avjon.vatten, 200 μl reaktionsbuffert (R1) och 50 μl reagens R2 (ATP och NADP) i alla 4 rören. 10. Överför 1 cm3 av lösningarna till kuvetter. Efter två minuter mäts absorbansen vid 340 nm. 11. Till varje kuvett tillsätt 7 μl enzymmix (R3) med hexokinas och glukos-6fosfatdehydrogenas. Inkubera i ytterligare 5 minuter och mät absorbansen en gång till vid 340nm. Tolkning av resultat. Den första mätningen bör vara låg. Till Läraren: Riskbedömningsunderlag: ”Risker vid experimentet” gäller endast de kemikalier som nämnts, under förutsättning att beskrivna koncentrationer, mängder och metod används. Som lärare förväntas du göra en fullständig riskbedömning för dig själv och din elevgrupp. Fehlings lösning Lugols lösning Proteinbestämning Ämne A( Röd fällning brun brun Red. sockerart B Blå lösning blå brun stärkelse C Röd fällning brun brun Red. sockerart D Violet lösning brun blå Protein E Blå lösning brun brun Sackaros Prov nr Första mätningen Anra mätningen 1+ 12+ 2Laborationen kommer från “Science in school” Issue 8 sid 22-27 8 Resultat