Atomfysik ht 2011
advertisement

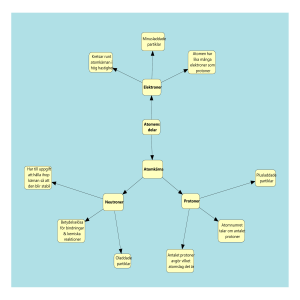
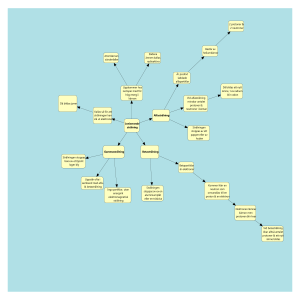
Atomfysik ht 2011 Atomens historia Atom = grekiskans a´tomos som betyder odelbar Filosofen Demokritos, atomer. Stort motstånd, främst från Aristoteles Trodde på läran om de fyra elementen Alla ämnen bildas utav en blandning av luft, eld, vatten och jord Atomens historia Slutet av 1800-talet trodde man att man hade en fullständig bild av alla fysikaliska fenomen. Detta var innan röntgenstrålningen, radioaktiviteten, elektronen och Einsteins relativitetsteori var upptäckta Thomsons atommodell (1897) Upptäckte elektronen och att dessa gick att frigöra från atomen, den var alltså inte odelbar. Hans modell bestod av att elektronerna var inbäddade i en positivt laddad sfär. Rutherfords atommodell (1911) Upptäckte protonen (atomkärnan). Bohrs atommodell (1913) Elektronerna finns som ett moln kring kärnan. De olika skalen (banorna) är lägen där chansen är störst att det finns elektroner. Elektroner som befinner sig i olika skal har olika energier. Bohrs modell kan liknas med vårt planetsystem där planeterna (elektronerna) kretsar kring solen (protonerna) i olika banor. Kvantmekaniska atommodellen (ca 1925): Elektronerna finns runt kärnan men rör sig inte runt den i banor utan med vågrörelser mot eller ifrån kärnan. de Broglie, Louis Atomens uppbyggnad En atom består av 2 delar Kärnan: atomkärnan består av positivt laddade protoner och neutrala (ingen laddning) neutroner. Runt kärnan kretsar negativt laddade elektroner. Atomens uppbyggnad Protoner, neutroner och elektroner = Elementarpartiklar Protoner och Neutroner = Nukleoner En atom består av lika många protoner (+) som elektroner (-). Därför blir alla atomen neutrala. Atomens uppbyggnad Protonerna och neutronerna har ungefär lika stora massor. Dessa har ungefär 2000 gånger så stor massa som elektronen. Därför återfinns större delen av en atoms massa i kärnan. Atomens uppbyggnad Elektronerna finns i olika skal kring kärnan, dessa betecknas K, L, M, N … I det innersta K-skalet får det plats 2 elektroner, i nästa (L-skalet) får det plats 8 elektroner o.s.v. Grundämne Ett grundämne består av ett slags atomer ex. guld (Au), Järn (Fe), Syre (O). Det finns idag ett hundratal kända grundämnen. Sammansatt ämnen Ett sammansatt ämne består av molekyler, vilket innebär att flera atomer, av ett eller flera olika sorter, sitter ihop med bindningar. Ex. är Syrgas (O2), vatten, (H2O), m.m. Atomnummer och masstal Atomnumret anger hur många protoner det finns i kärnan. Väte har 1 proton i kärnan, järn har 26 stycken medan guld har 79 stycken. O 16 8 Masstalen anger hur många protoner + neutroner det finns i kärnan. Isotop Isotoper är atomer av ett grundämne som har olika antal neutroner, men samma antal protoner. Atomkärnan i väte består endast av en enda proton En atom med en neutron och en proton kallas tungt väte (deuterium). Är det två neutroner och en proton i kärnan kallas det tritium. Dessa är alltså isotoper av väte. Diskutera Vilka påståenden är sanna? - Idag vet vi exakt hur en atom ser ut. - Atomkärnan består av lika många neutroner som protoner. 14 - C innebär att atomkärnan består av 6 protoner och 8 neutroner. 6 - I L-skalet får det plats 8 elektroner. Diskutera Vad är det som bestämmer vad det är för ett grundämne: protonerna, neutronerna eller elektronerna? Vad innebär sammansatt ämne? Vad är det för skillnad på två olika isotoper av en atom? Vad består en atom av mest? Vad är ljus? Partikel eller vågor? Ljus är en vågrörelse (transversella vågor) Ljusets hastighet är 300 000 km/s. Det som sänds ut är fotoner (energipaket). Det ljus (spektrum) som vi kan se kallar vi för elektromagnetisk strålning. Foton Mycket mindre än en atom. Forskarna tror att den är utan massa Att den kan färdas i ljusets hastighet. Kvant partikel. Både partikel och en våg. Hur uppstår ljusets färger? (del 1) Tillför man energi till en atom kan elektronerna lämna sitt skal för att hoppa till ett skal längre ut (exitererat tillstånd). När elektronen sen hoppar tillbaks sänds strålning ut, ibland som synligt ljus. + K L M + Hur uppstår ljusets färger? (del 2) Ju mer energi som matas in i elektronen ju längre bort från kärnan kommer den och ju mer energi får den. Energi fattigt Korta hopp Energi rikt Långa hopp Förklara för grannen! Använd orden: Energi, exitererat tillstånd, energi nivå, foton, strålning, synligt spektra Diskutera Vad är ljus? Bildas alla färger när det är lite ljus? Vi ser ju bara svart/vitt i mörker. Kan man se på en låga vad det är varmast? Elektromagnetiskt spektra Strålning Vilken sorts strålning atomen sänder ut beror på hur stort hopp elektronen gjort. Olika färger motsvarar olika långa hopp. Röntgenstrålning skapas när en elektron hoppar från ett yttre skal till ett av de innersta, alltså ett långt hopp, vilket innebär att röntgenstrålning är väldigt energirik. Röntgen Wilhelm Röntgen Elektron som gör långa hopp mellan skalen Atomen avger då röntgenstrålar Energirik och tränger lätt in i kroppens vävnader Skelettet fångar upp strålningen bäst Tandläkare, läkare Radioaktiva ämnen • • • • • • Upptäcktes av en slump 1896 Henri Becquerel Marie och Pierre Curie Radium och Polonium Nobelpriset i fysik 1903 med Becquerel Radioaktivitet Ett radioaktivt ämne har en instabil kärna som genom att släppa ut energi blir stabilare. Radioaktiv strålning sänds alltså ut från atomkärnan. Många ämnen har isotoper med instabila kärnor, dessa är radioaktiva, t.ex. kol-14 Många av de naturligt radioaktiva ämnena har stora kärnor (många protoner och neutroner) t.ex. uran, radon, radium. När kärnan sönderfaller sänds radioaktiv strålning ut, denna kan vara av tre slag: Sönderfall Sönderfall är när ett nytt ämne bildas eftersom antalet protoner och neutroner ändras. Kärnan avger radioaktiv strålning när sönderfall sker. Alfastrålning (α) • Alfastrålning består av positivt laddade partiklar. En alfapartikel består av två protoner och två neutroner. Det är alltså samma sak som en atomkärna av helium. • Om en atomkärna sänder ut en alfapartikel sänder den alltså ut protoner, på grund av det bildas ett nytt grundämne med två färre protoner i kärnan. Betastrålning (β) Betastrålning är negativt laddade elektroner. Elektronerna sänds ut från kärnan där det inte finns några elektroner. Dessa bildas när en neutron sönderfaller i en proton och en elektron. • Betastrålning innebär då att atomkärnan förlorar en neutron och får en proton, vilket leder till att atomen nu är ett annat grundämne. Gammastrålning (γ) • Gammastrålning består inte av partiklar. Det är istället elektromagnetisk strålning. • Gammastrålning är samma sorts strålning som ljus och röntgenstrålning. Den är dock energirikare och har därför kortare våglängd. Strålningens genomtränglighet Alfastrålningen har kort räckvidd och stoppas lätt av ett papper eller av huden. Betastrålningen har längre räckvidd (några meter i luft) och stoppas av några mm tjock aluminium- eller träskiva, stoppas även av ett lager kläder. Gammastrålningen tränger igenom det mesta, den kräver ett tjockt lager bly för att stoppas. Sönderfallsserie Att mäta radioaktivitet Mängden strålning ett radioaktivt ämne sänder ut kallas aktivitet. Aktiviteten mäts i becquerel (Bq) och innebär antal sönderfall per sekund. 1Bq innebär alltså ett sönderfall på en sekund. Radioaktiv strålning kallas också joniserande strålning. Detta eftersom strålningen har energi nog att slå bort elektroner från atomer och på så sätt bilda joner. Att mäta radioaktivitet Geiger-Müller räknare (GM-rör) är ett sätt att mäta aktiviteten hos ett radioaktivt ämne. Dosimeter är en liten dosa som registrerar radioaktivitet. Alla som arbetar med radioaktiva material ska bära en dosimeter så att man kan kontrollera att de inte blir utsatta för farliga mängder strålning. Att mäta radioaktivitet I en dimkammare utnyttjar man att den radioaktiva strålningen är joniserande. Den radioaktiva strålningen går genom vattenånga eller ånga av alkohol och skapar där joner som binder vattenångan och detta kan man se som dimspår. En bubbelkammare är ett annat exempel där man utnyttjar att det bildas joner där den radioaktiva strålningen har varit. I en bubbelkammare bildas små vätgasbubblor kring jonerna och på så sätt kan man se vart den radioaktiva strålningen har varit. Halveringstid • • • • • Atomkärnor faller inte sönder samtidigt i ett radioaktivt ämne Halveringstid = ett mått på hur fort sönderfallet går Tid för hälften av alla atomkärnor att sönderfalla När Radium omvandlas till Radon är halveringstiden 1620 år Kan variera kraftigt, från en sekund till flera miljoner år. Halveringstiden på Cesium efter Tjernobyl olyckan 1980 Åldersbestämning Kol 14 metoden. Man jämför sönderfallet av isotopen kol-14, genom att se hur många procent av den radioaktiva isotopen som finns kvar. Halveringstiden för kol-14 är ca 5500 år. Kärnenergi Tillverkning av grundämnen Grundämnen kan omvandlas till ett annat grundämne Radioaktivt sönderfall Konstgjord väg Ernest Rutherford 1919 Sköt alfapartiklar (heliumkärnor) mot kväve Alfakärnan tränger in i kvävekärnan ny instabil kärna av syre Atomklyvning (Fission) Första atomklyvningen gjordes 1939 Fission Sköt neutroner på atomkärnor Kedjereaktion Kärnenergi + Energi Atombomben Nyfunnen kunskap spelade stor roll i andra världskriget Atombomben Miljarders miljarder atomkärnor frigörs Okontrollerad kedjereaktion Mängder av energi frigörs Explosion Atombomben Hiroshima 6 augusti, 1945 Nagasaki 9 augusti, 1945 Ny energikälla Inte bara negativa effekter Ny energikälla kärnenergi Använda energin som frigörs till att värma upp vattnet i reaktorn. Fusion Kärnenergi skapas inte bara på jorden Enorma mängder energi frigörs i alla universums stjärnor Fusion lättare atomkärnor slås ihop Einstein Materia kan omvandlas till energi Lite mängd materia = stor mängd energi Formel: E = m • c2 W = energi och mäts i joule m = massan i kilogram c = ljusets hastighet m/s