Luft och vatten - År 8 Mälarhöjdens skola
advertisement

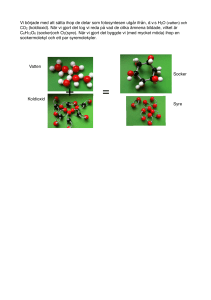
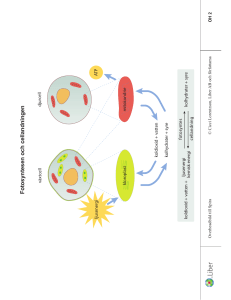
LUFT OCH VATTEN KE år 7 Mälarhöjdens skola KEMI – luft och vatten LUFT KE år 7 Mälarhöjdens skola KEMI – luft och vatten LUFT 1 m3 luft väger ca 1,3 kg. Kan man bära luften i NO-salen om man ”packar ihop” den till en boll? Svar: Luften i NO-salen väger ca 250-300 kg. GASER • Ingen bestämd volym • Expanderar (utvidgar sig) tills det fyllt tillgängligt utrymme. • Var och en av molekylerna eller atomerna rör sig helt oberoende av de övriga. • Gasformiga ämnen har egenskaper som gör att man kan skilja dem åt. LUFTEN Luftens sammansättning Koldioxid; 0,04% Ädelgaser; 0,93% Övriga gaser; 0,03% Syre; 21% Kväve Syre Ädelgaser Koldioxid Övriga gaser Kväve; 78% NÅGRA GASER KE år 7 Mälarhöjdens skola KEMI – luft och vatten SYRE • Heter även oxygen. • Alla syremolekyler kommer från de gröna växterna. • Syremolekyler förbrukas vid förbränning. • Syre är nödvändigt för vår andning och för att eld ska kunna brinna. • Utvinns ur luften eller framställs genom sönderdelning av vattenmolekyler. • Används till andningsgas, tillverkning av stål, blekning av pappersmassa, svetsning. Syremolekyl O2 KVÄVE • Heter även nitrogen. • Ogiftigt ämne (luft består till 78% av kväve) • Endast enstaka bakterier och alger kan använda sig av luftens kväve. • Allt liv innehåller kväveatomer. • Används till tillverkning av gödningsmedel, färgämnen, läkemedel. Flytande kväve används som kylmedel. Kvävemolekyl N2 VÄTE • Det lättaste av alla ämnen • Vanligaste atomslaget i universum • Brinner mycket intensivt i luft eller syre – ibland sker förbränningen med en knall • Knallgas - en blandning av väte och syre. Vid reaktionen bildas vatten • Fås frams genom att sönderdela vattenmolekyler med hjälp av elektricitet • Används vid tillverkning av margarin, ammoniak och saltsyra, bränsle i rymdraketer Vätemolekyl H2 KNALLGAS Knallgas En blandning av väte och syre. Vid reaktionen bildas vatten OZON Reagerar lätt med andra ämnen • Livsviktig högt upp i atmosfären - skyddar mot solens UV-strålar. Skadas av freoner. • Giftig på marknivå • Används bl.a. för att döda mögel i fuktskadade hus, blekmedel för pappersmassa. Syremolekyl, O2 Ozonmolekyl, O3 BILDNING OZON • Bildas högt upp i atmosfären → energirik solstrålning slår sönder syremolekyler till fria atomer → de fria atomerna sätter sig omedelbart på en ny syremolekyl • 3 O2 + energi → 2 O3 • Kan även bildas på annat sätt: FÖRSTÖRA OZON (Exempel) ÄDELGASER KE år 7 Mälarhöjdens skola KEMI – luft och vatten ÄDELGASER • Mycket stabila • Helium – lättast av alla ämnen efter väte. Används i bl.a. ballonger och luftskepp. Radon – farlig gas. Radonatomer faller sönder och avger då en strålning som kan framkalla cancer. • Neon - rött sken i neonskyltar • Argon – blått sken i lysrör. Glödlampor. Skyddsgas vid svetsning för att förhindra att metalloxider bildas. • Xenon och krypton → speciella belysningsanläggningar K: max 2 eL: max 8 eM: max 8 e- om det ligger ytterst ATOMENS UPPBYGGNAD - - M - - - L + + + ++ + ++ + + + +++ + + + + - 2He 10Ne 18Ar 36Kr - - - - - Helium Neon Argon Krypton - K - Om det finns skal utanför kan man dock få plats med 18 elektroner i M-skalet. - - OXIDER KE år 7 Mälarhöjdens skola KEMI – luft och vatten OXIDER • Oxider är kemiska föreningar där syreatomer sitter ihop med ett annat atomslag. • När någonting brinner bildas det alltid oxider. En sådan reaktion kallas förbränning. • I luften finns oxider med kolatomer, kväveatomer och svavelatomer. De kallas koloxider, kväveoxider och svaveloxider. KOLDIOXID • När ämnen med kolatomer brinner i luft bildas koldioxid. • Vid ofullständig förbränning (syrebrist) bildas i stället kolmonoxid som är giftigt. • När vår kropp förbränner maten bildas också koldioxid. KOLDIOXID • Mycket god löslighet i vatten → stora mängder i haven. • Används vid algernas fotosyntes eller för skaluppbyggnad hos många havslevande djur. • När koldioxid bubblas genom vatten stannar en del koldioxidmolekyler kvar i vattnet. Gasen löser sig och lösningen kallas kolsyra. • Tung gas som tränger undan luft → bra vid brandsläckning. • Läskedrycksframställning, gödningsämne i växthus m.m. VATTEN KE år 7 Mälarhöjdens skola KEMI – luft och vatten Drygt 70 % av jordytan är täckt av vatten 97 % av allt vatten finns i haven Kroppen består av ca 70 % vatten • H2O - Vattenmolekylen består av en syreatom och två väteatomer • Hög ytspänning – molekylerna håller ihop hårt. Gör att stora droppar kan bildas och att insekter kan gå på vatten. • Ytspänningen ger stark kapillärkraft → vatten kan sugas upp från marken genom växternas tunna kärl - ”klättrar uppför” väggarna • Lättare i fast form än som vätska (motsatsen gäller för de flesta andra ämnen) → flytande vatten under isen förhindrar bottenfrysning av sjöar. KONDENSATION NEDERBÖRD AVRINNING GRUNDVATTENAVRINNING Vattenförråd i snö och is SMÄLTVATTENAVRINNING AVDUNSTNING RENING AV DRICKSVATTEN Grundvatten har ”silats” genom jord och sand och behöver inte renas så mycket. Ytvatten behöver renas. • Rening sker ofta med grovsilning, flockning, filtrering och bakteriedödande medel. • Flockning → tillsätter ämnen som tar med sig föroreningar när de faller till botten RENING AV AVLOPPSVATTEN Avloppsvatten renas i tre steg: mekanisk rening, biologisk rening och kemisk rening: – Mekanisk rening → vattnet silar och uppslammade ämnen faller till botten. – Biologisk rening → mikroorganismer äter upp föroreningar som innehåller kolatomer. Sedan blir mikroorganismerna till bottenslam. – Kemisk rening → tar bl.a. bort fosfat from tvättmedel med hjälp av flockning.