Prostatacancer
advertisement

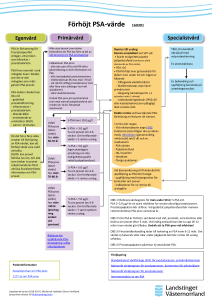
Prostatacancer Andreas Nilsson P Prostatacancer t t – mångfacetterad symtomatologi y g och behandling Riskfaktorer för prostatacancer • Hög Hö åld ålder • Ärftlighet • Geografisk och etnisk tillhörighet • Västerländskt levnadssätt • Rökning ? 1400 Incidens Mortalitet 1300 1200 1100 1000 /1 100 000 900 800 700 600 500 400 300 200 100 0 0 5-9 5 29 15 15-19 419 25 25-29 6 29 35 35-39 839 45 45-49 1049 55 55-59 1259 65 65-69 1469 75 75-79 16 79 85+ 18 Åldersgrupp Figur 2. Åldersspecifik incidens (1995-2004) och mortalitet (19932002) av prostatacancer t t i St Stockholm-Gotlandregionen. kh l G tl d i Relativ 55-årsöverlevnad prostatacancer Survival for eight major cancers and all cancers combined for European adults diagnosed in 1995– 1995–99: results of the EUROCARE EUROCARE--4 study, Lancet Oncol 2007: 8: 773 773– –783 Sverige Europa • 1995 1995--1999 77.3 % • 1995 1995--1999 73.9 % Periodanalys • 2000 2000--2002 82.5 82 5 % Periodanalys • 2000 2000--2002 77 77.5 5% Vägarna till doktorn 1. Symtom 2. PSAPSAscreening 5 Sena 5. S symtom t på å spridd cancer 3. Palpationsfynd 4. PAD PAD--svar efter transuretral kirurgi i området 1. Symtom a) Vattenkastningsbesvär - vanligast • Trängningar g g till vattenkastning g • Försämrat flöde • Pollakisuri • Känsla av ofullständig tömning • Nattlig vattenkastning • U Upprepade d Uvier U i b) Impotens 2. PSA PSA--screening a) Som led i allmän hälsokontroll b) På patientens begäran Så k ll d kallad ”Op O portun screening” screening” c)) Som led i malignitetsutredning g g d) Som del av planerad vetenskaplig screeningscreening-studie Kort om PSA Fritt och bundet PSA strömmar ut från epitelepitelcellerna i prostatan till blodbanan Mätbart som S-PSA - Diagnostik - Stadieindelning - Monitorering Skäl för PSAPSA-stegring • Prostatacancer • BPH - benign prostatahyperplasi • Prostatit, UVI • Instrumentering (TUR-ingrepp, Cystoskopi, TRUL, KAD(TURKAD-sättning, TRUL och biopsi – dock ej palpation) • 5-alfa alfa--reduktashämmare, provtagning, metodfel interindividuell variation metodfel, Hur ska ickeicke-urologer agera vid bed av PSA ? Män < 50 år med PSA > 2 μg/l remitteras till urolog Män 50– 50–60 år med PSA > 3 μg/l remitteras till urolog För män > 60 år med PSA 33-10 μg/l tas kvoten f/t PSA med i bedömningen: • PSA > 3 μg/l vid normalstor prostatakörtel och/eller prostatacancer hos far eller bror:Remiss till urolog • PSA 3– 3–10 μg/l och palpationsfynd som vid benign hyperplasi hos män utan hereditet för prostatacancer: - Kvot f/tPSA < 0 0,18: 18: Remiss till urolog - Kvot f/tPSA > 0,18: PSA följs halvårsvis. PSA > 10 μg/l: Remiss till urolog www.ocsyd.se 3 Palpationsfynd 3. I samband b d med d allmän ll ä undersökning d ök i eller ll annan undersökning kan… • Assymetri och/eller • Förhårdnad och/eller • ”Knöl Knöl”” …palperas. Ett sådant palpationsfynd kan föranleda vidare utredning 4 PAD 4. PAD--svar efter transuretral kirurgi g i området Patienter som opereras för BPH (benign prostatahyperplasi) t t h l i) med d TUR TUR--P eller ll öppen ö adenomenukleation I PADPAD-svaret kan återfinnas tidigare okänd prostatacancer 5 Sena symtom på spridd 5. cancer Skelettmetastaser Patienten uppsöker sjukvården primärt med tecken på -Spinal påverkan från kotmetastaser -Uttalad smärtproblematik p från kotpelare, p , bäcken,, långa g rörben -Patologiska frakturer Lymfkörtelmetastaser Patienten uppsöker sjukvården primärt med tecken på -Förstorade lymfkörtlar -Svullnad i extremitet, extremitet underlivet Prostatacancer-Prostatacancer en kontroversiell tumörsjukdom! j • Naturalförlopp – varierande • Äldre Äld män ä med d andra d sjukdomar j kd • Cancerceller hos 1/3 män > 50 år • Få kontrollerade studier Histologisk gradering: enligt Gleason Gleason grad 1 2 3 4 5 ”Elak Elak”” Gleasonsumman=det vanligaste + näst vanligaste tumörutseendet grad 11-5 Prognosticering Val av behandling • Gleasonsumma Gl (Gleasonsumma <7 = låg risk) • PSA värde (<10 = låg risk) • Tumörstorlek (T-stadium, (Tstadium antal biopsier med cancer cancer, mängd cancer i biopsin) • Förekomst av metastaser inför beslut om strålbehandling görs metastasutredning om: PSA>20, eller T3, eller Gleason ≥4+3=7 TNM T1-tumörer: T1Icke--palpabla Icke T3-4: T3Lokalt avancerade T1 och T2--tumörer: T2 Lokaliserade TNM Lymfkörtelspridning y p g - utreds med lymfkörtelop, y p någon gång MR. Dock inga säkra metoder! Fjä Fjärrmetastaser t t - utreds t d med d skelettscintigrafi k l tt i ti fi Kurativ u at behandlingsindikation be a d gs d at o generella indikationer • T1 T1--3, N0, M0 • Förväntad överlevnad 10 år • Symptomgivande sjukdom • Egen begäran Prognosgrupper PC • Lågrisk: T1 T1– –T2a, Gleasonsumma ≤ 6 och PSA < 10 μg/l • Intermediärrisk: T2b och/eller Gleasonsumma 7 och/eller PSA 10– 10–20 μg/l • Högrisk: T2c T2c– –T3 och/eller Gleasonsumma 8 8– –10 och/eller PSA 20– 20–50 μg/l Radical Prostatectomy • Diminishes the risk of prostate cancer death SPCG 4 trial NEJM 2002, NEJM 2007 • Extensive overtreatment. SPCG 4 trial NEJM 2002 Radical Prostatectomy • The patient has to accept a considerable risk of treatment induced side affects. • Quality Qua ty of o life e not ot worse o se co compared pa ed to watchful waiting. Stieneck et al NEJM 2002 Kurativt syftande behandling: Prostatectomi • Öppen • Robotassisterad laparoskopisk • Laparoskopisk Kurationsgrad 70 70--95% - riskfaktorberoende Hur fungerar den? Da Vinci är ingen robot... Hjälpmedel styrd av kirurgen g EndoWrist Tre-dimensionell bild och 10-gångers förstoring Utväxlade rörelser 5 cm 1 cm 2:1 till 5:1 Tremor filter En avslappnad icke-sterilklädd barfota operatör. Antalet Radikala Prostatektomier/år på Karolinska Solna 500 450 400 350 Open Robotic 300 250 200 150 100 50 0 2007 7 6 200 5 150 4 100 3 2 50 1 0 0 2000 2001 2002 Year 2003 2004 L en g th o f h o sp ital stay R ad ical p ro statecto m y 250 Open operation Robotic operation Komplikationer till kirurgi • impotens • inkontinens • biokemiskt recidiv 50 - 80% 20 - 35% 30 – 60% • SEER-data (ca 10 år gamla) SPGC 4; Quality of life SPGC-4; n= 695 inkontinens impotens miktionsmiktions svårigheter kirurgi n=347 49% 80% 28% expektans n=348 n 348 21% 45% 44% Steineck et al. NEJM 2002 Continence Co t e ce Overview Ove v ew Surgeon 3 mo 6 mo 12 mo Walsh (Open) 54 % 80% 93% Abbou (Laparoscopic) 58% 69% 78 4% 78.4% Guillonneau (Laparoscopic) N/A N/A 85.5 % Rassweiler (Laparoscopic) 54% 74% 97% M Menon (R b ti ) (Robotic) N/A 96% N/A Ahlering (Robotic) 76% 91% 94% Lee (Robotic) 60% 82% N/A Source: Published Clinical Data Review by David II. Lee Lee, M M.D., D UANT Continence data after 3, 6 and 12 months, all surgeons from case 1 to 595 på Karolinska Solna No pads 1 pad /day preop 98,3 % 0,8 % ≥ 2 pads /day 0,3 % 3 Months postop. 6 Months postop. 12 Months postop. 63 7 % 63,7 21 4 % 21,4 14 9% 14,9% 79,1 % 14,5 % 6,4 % 86,6 , % 8,9 , % 4,4 , % Potency data 12 months after surgery for all patients operated at Karolinska Solna with DvP Potency defined as having successful sexual penetration in at least half of attempts with or without the use of PDE-inhibitors. - 57.5 % after bilateral nerve sparing - 52.1 % after unilateral nerve sparing g Wide variation between surgeons concerning potency results 87% able to perform sexual penetration after either bi or unilateral nerve sparing for one of the surgeons Compared to 37 % able to perform sexual penetration after bilateral nerve sparing for an other surgeon Variable Bilaterally nerve spared Unilaterally nerve spared Semisparing of NVB Age (range) 59.8 (46-71) 60.4 (53-74) 63.5 (59-72) PSA ng/ml (range) 6.6 (2.7-21) 6.6 (1.1-14) 8.5 (3.2-17) T1c Tumours (%) 30/36 (83.3 %) 11/24 (45.8 %) 10/23 (43.5 %) T2 Tumours (%) 6/36 (16.6 %) 13/24 (54.2 %) 11/23 (47.8 %) T3 Tumours ((%)) 0/36 0/24 2/23 ((8.7 %)) Gleason score (preoperatively) ≤ 6 32/36 (88.9 %) 19/24 (79.2 %) 16/23 (69.6 %) =7 4/36 (11.1) 3/24 (12.5 %) 6/23 (26.1 %) ≥8 0/36 2/24 (8.3 %) 1/23 (4.4 %) pT3 tumours (%) 7/36 (24.1 %) 5/24 (20.8 %) 13/23 (56.5 %) Positive margins (%) 7/36 (24.1 %) 4/24 (16.7 %) 4/23 (15.7 %) O Oncological l i ld data t ffor th the diff differentt approches h off nervesparing Complications in Radical Prostatectomy • Retrospectively reviewed 1738 men • January 2002 to August 2007 485 open retropubic radical prostatectomies 1253 robot-assisted radical prostatecties Variable RRP (n= 485) Median age (range) 63 (47-77) 62 (35-78) 7.4 (0.1-135) 6.3 (0.4-50) Median PSA ng/ml (range) Median preop. Gleason score RARP (n= 1253) 6.0 (4-10) 6.0 (4-9) 38 0 (16 38.0 (16-130) 130) 38 0 (16-206) 38.0 (16 206) (range) Median prostate volume ml (range) RRP RARP T1c T2 T3 T1c T2 T3 r e ct a l in j u r y 1,6 1,4 1,2 1,6 1 08 % 0,8 0,6 0,4 , 0,15 0,2 0 RRP 1 RARP 2 W ou n d in fe ct ion s 6 5 4 5,9 % 3 2 1 0 0,4 RRP 1 RARP 2 Blood t r a n sfusions 25 20 23,0 15 % 10 5 0 46 4,6 RRP 1 RARP 2 Ur e t h r a l st r ict u r e s 4,5 4 3,5 3 4,5 2,5 % 2 1,5 1 0,2 0,5 0 RRP 1 RARP 2 MAJOR COMLICATIONS Deaths Rectal injury Small bowel injury U t l injury Ureteral i j Femoral nerve injury, Ob Obturator nerve iinjury j Pulmonary embolism Myocardial infarction M a j or com plica t ion s 4 3,5 3 2,5 % 3,7 2 1,5 1 0,7 0,5 0 RRP 1 RARP 2 Robotic in the future ? Clinical Training Livskvalitéfrågor å • Viktigt vid val av behandling • Biverkningar av behandling måste reduceras!! OM SJUKDOMEN ÄR SPRIDD SPRIDD…… • 65 65--80% • Skelettmetastaser y • 50% • Lymfkörtelmetastaser • Överväxt blåsa • 35% • • • • Levermetastaser Lungmetastaser Hjärnmetastaser Hudmetastaser • • • • 5-10% 3-4% 1-2% 1-2% När behandlingen inte hjälper mer TACK