Informationsbrev 10
Januari 2002
Innehåll
Litteratur
Undervisningsidéer
Par-bingo
Fasta ämnen – vätskor - gaser
Diverse: Kungsvatten
Laborationer
Kopparcykel i mikroskala
Identifiering av PVC-plast
Gummiband och värme
Kristallbildning i en gel
Opolära och polära vätskor
Från Internet
Sida
2
6
6
8
11
12
12
14
15
17
17
18
Vasa den 21 januari 2002
Hej!
Det börjar vara länge sedan ni hört av mig; en del har tom. hunnit börja fråga efter mina brev
och undrat om jag tappat bort deras skola från adresslistan. Så är dock inte fallet! Det är roligt
att märka att breven är välkomna! Själv har jag helt enkelt varit upptagen med andra
uppgifter, så att jag helt enkelt inte hunnit jobba med ett nytt brev. Jag vill samtidigt passa på
att påminna er om att jag tacksamt tar emot av era idéer och sprider dem till andra lärare via
dessa brev. Ju mera ni själva bidrar, desto mångsidigare material får alla ta del av!
Jag kan glädja er med att vi detta läsår faktiskt har 8 ämneslärarauskultanter inom vår
ämnesgrupp (lite varierande ämneskombinationer) här i Vasa. Detta är betydligt fler än de
senaste åren. Däremot ser inte framtiden speciellt ljus ut när det gäller antalet lärare i
matematik, kemi och fysik i Svenskfinland. MNF i Åbo har få studerande med lärarinriktning
i matematik, kemi och fysik och ett stort antal lärare går i pension inom de närmaste åren. Den
nya timplanen för grundskolan innebär ju för våra ämnen en klar förstärkning; en
matematiktimme till inplacerad i någon av årskurserna 6-9, en kemi/fysik-timme i högstadiet
samt kemi/fysik som eget ämne i årskurs 5-6. Detta är ju en glädjande förstärkning av våra
ämnen, men det behöver samtidigt finnas kompetenta och behöriga lärare som kan undervisa!
Vi har således alla en viktig uppgift i att skapa intresse för matematik och naturvetenskap å
ena sidan och för läraryrket å andra sidan!
Kemi och fysik har hittills, i princip, varit en del av helheten miljö- och naturkunskap i
lågstadiet. Många lärare och skolor har dock valt att lämna bort dessa ämnen ur sin
undervisning, kanske pga. att de ansett att kemi och fysik är för svåra ämnen att tas upp i
lågstadiet, eller för att de själva upplevt att de inte klarar av att undervisa dessa ämnen. Jag ser
i alla fall den nya timplanen som en möjlighet att verkligen kunna starta på mycket elementär
och vardagsnära nivå med kemi- och fysikundervisningen. Kemi och fysik i lågstadiet borde
få vara ett forum där eleverna får utveckla sin förmåga att studera och undersöka fenomen
som de stöter på i sin vardagsvärld. Jag antar att en del lågstadieskolor kommer att lösa
problemet med fysik-kemi-lärare genom att ta in någon av er som jobbar på högstadiet. Det är
då oerhört viktigt att hitta rätt nivå för denna undervisning (inte starta med ”atomens
byggnad” i årskurs 5 i stället för årskurs 7!). Jag kommer senare i detta brev att tipsa om några
böcker som kan vara till stor nytta och glädje för den som skall undervisa i lågstadiet.
För min del är det tänkt att jag under den närmaste framtiden skall försöka avdela mera tid till
forskning inom kemididaktik. Detta hoppas jag att på sikt kan gagna kemiundervisningen i
skolorna. Men det betyder samtidigt att jag kommer att vara mera ”sparsam” med
fortbildningsverksamheten – min tid vill inte räcka till allt jag tycker att jag borde hinna med!
Jag hoppas att ni skall hitta något i detta brev som ni har användning för. Kom ihåg att ni kan
kontakta mig om ni har problem, frågor och tankar som gäller kemiundervisningen, som ni
1
funderar över. Jag är också tacksam för tips på användbara Internetsidor, och mottaglig för
olika undervisningsidéer, laborationer mm.
Ha det så gott!
Berit
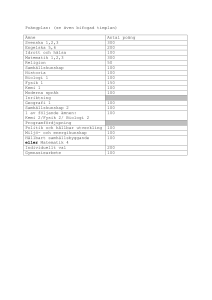
Litteratur
Kemi & biologi i maten
Bo Furugren
Natur och Kultur, 2001
ISBN 91 27 75245 3
Pris: € 27 (www.bol.com)
En bra bredvidläsningsbok med såväl experiment och teori, relativt enkelt framlagd. I boken
hittar man material såväl till specialkurser kring matens kemi, samarbetsprojekt med biologin
eller huslig ekonomi men även material för att göra den vanliga kemiundervisningen mera
verklighetsnära via kopplingar till matens kemi.
Från raff till rengöring
- ett material om petrokemisk industri på Sveriges västkust
Magnus Gustafsson
Kemilärarnas Resurscentrum
Enligt bokens titel handlar materialet om den petrokemiska industrin på Sveriges västkust,
men detta är nog rätt missvisande. Innehållet är långt mera allmängiltigt och användbart.
Syftet med materialet är bl.a. att eleverna (och lärarna) skall upptäcka petrokemins betydelse i
vardagen. ”Från raff till rengöring” består dels av en bok, som innehåller en del artiklar om
olika petrokemiska produkter i vår vardag, material om olika bränslen och oljor mm. dels av
en CD-skiva som bl.a. innehåller ett rikligt antal användbara laborationer.
Materialet kan beställas från Kemilärarnas Resurscentrum, men materialet kan också laddas
ner från Internet i pdf-format. Hittas under adressen: www.krc.su.se
Kjemi i skolen – undervisning og læring
Vivi Ringnes & Merete Hannisdal
2
HøyskoleForlaget, 2000
ISBN 82 7634 326 0
www.hoyskoleforlaget.no
Pris: 369 NKr
Detta torde vara den första skandinaviska kemididaktikboken! De båda författarna arbetar
med skolutveckling och lärarutbildning i Oslo. Boken är norsk och skriven med tanke på
kemiundervisningen i Norge, men är till stora delar tillämpbar även hos oss. Det är trevligt att
för en gångs skull få en bok i sin hand som direkt inriktar sig på undervisning av kemi. I
allmänhet är ju didaktikböcker mera inriktade på fysik, kemin kommer vid sidan om. I boken
diskuteras några grundläggande kemiska begrepp, såsom kemiska bindning, fällningar, syror
och baser kemiska reaktioner mm., vilka elevuppfattningar som finns gällande dessa begrepp
och hur man kan undervisa dem. I boken behandlas undervisning med sikta på förståelse av
kemi, kemins tre olika dimensioner (makro-, mikro- och symbolisk nivå), hur man kan
använda modeller i kemiundervisningen för att öka förståelsen osv.
Rekommenderas.
Kemiska mellanslag
Stig Olsson
Ekelunds förlag AB, 2002
ISBN 91 646 1469 7
Pris: €44 (www.bol.com)
Detta är ingen lärobok i kemi, däremot en intressant bredvidläsningsbok. En bok med
anekdoter, skrönor, historiska berättelser som berör kemin och dess uppkomst och utveckling.
I boken berättas om upptäckten av ett flertal grundämnen, hur det gick till då flogistonteorin
omkullkastades, hur blåsröret användes för att utvinna metaller ur metalloxider mm. Texten är
enkelt och begripligt skriven. Boken kan vara en källa att plocka ur då man vill krydda sin
undervisning med lite kemihistoria, här kanske man kan hitta uppslag till någon
morgonsamling med kemisk anknytning eller en bok som man kan ge som premie åt någon
speciellt intresserad elev. I boken finns dessutom en mängd serieteckningar med anknytning
till kemi; även dessa kan vara användbara i den egna undervisningen.
Modell och verklighet A
Kemi för gymnasieskolan
Pilström Helen m.fl.
Natur och kultur, 2001
ISBN 91 27 61215 5
Pris: €56 (www.bol.com)
3
Modell och verklighet B
Kemi för gymnasieskolan
Pilström Helen m.fl.
Natur och kultur, 2001
ISBN 91 27 61218 X
Pris: €57 (www.bol.com)
I Sverige har man nu reviderat läroplanerna i gymnasiet, vilket medfört färre kemitimmar.
Detta har gjort att åtminstone en del av deras läroböcker nu utkommit i nya reviderade
upplagor. Detta gör samtidigt att mängden stoff i böckerna närmar sig det vi kan ta upp i våra
gymnasier. Innehållet har dock en lite annan uppläggning, och böckerna kan därför vara svåra
att använda som läroböcker i våra gymnasier. Däremot tycker jag att jag själv hade stor nytta
och glädje av den första boken då jag undervisade en gymnasiekemikurs senaste år. I
uppläggningen finns en strävan efter att skapa förståelse, vilket jag kanske saknar i våra
läroböcker. Kan rekommenderas, åtminstone för den egna bokhyllan.
Making sense of secondary science
- research into children’s ideas
Driver Rosalind m.fl.
Routledge, 1997
ISBN 0 415 097657
Pris: € 37 (bol.com)
När våra elever kommer till högstadiet har de redan en mängd egna uppfattningar och
förklaringar till naturvetenskapliga fenomen som de kommit i kontakt med i sin vardag. Dessa
uppfattningar påverkar deras inlärning, och borde därför beaktas i undervisningen. Mycket
forskning har gjorts under de senaste decennierna för att ta reda på mera om elevers egna
uppfattningar. En del av dessa forskningsresultat finns sammanfattade i denna bok och den
ger därför en bra startpunkt för att ta reda på mera om dessa uppfattningar. I boken behandlas
teman ur såväl kemins, fysikens som biologins område. Detta är en bok som jag varmt
rekommenderar och hoppas att ni alla skall ha möjlighet att skaffa!
Iloa tutkimisesta
Kirsi-Maria Vakkilainen
Opetushallitus / Taloudellinen Tutkimustoimisto
2001
ISBN 952 9876 52 1
Idag inser man mer och mer behovet av att eleverna redan i lågstadiet borde komma i kontakt
med kemi och fysik. Denna bok innehåller en hel del idéer, material och didaktiska tips, som
lämpar sig för undervisning av kemi i lågstadiet, och kan därför vara ett bra hjälpmedel för
4
den som skall undervisa kemi i lågstadiet. Boken kan beställas från Taloudellinen
Tutkimuslaitos gratis (tills vidare bara på finska), men kan också laddas ner i pdf-format från
deras hemsidor. Adressen är:
http://www.tat.fi/fi/index2.htm
Genom att klicka på ”Aineistot” i menyn och vidare på ”Luonnontiede” hittar ni deras
undervisningsmaterial som gäller naturvetenskap (där finns också annat matnyttigt).
LUMO Tutkimuksia 1-3, opettajan opas
Kärnä P m.fl.
WSOY
En del skolor har övergått till den nya TOP-boken i högstadiets kemi- och fysikundervisning.
På svenska har det ju inte utkommit någon lärarhandledning (förstås), däremot finns det rätt
goda handledningar på finska. Om ni använder TOP-böckerna rekommenderar jag att ni
skaffar de finska lärarhandledningarna; de innehåller en hel del goda undervisningstips och
-idéer, en del forskningsresultat gällande barns förhandsuppfattningar, pedagogiska tankar
bakom materialet mm.
Kan beställas från:
WSOY/TILAUSKONTTORI
Tel: 019 - 548 01
Fax: 019 – 548 0339
www.wsoy.fi/koulu
Försök med kemi
Hans Persson
Almqvist & Wiksell, 1997
ISBN 21-14781-7
Försök med fysik
Hans Persson
Almqvist & Wiksell, 1996
ISBN 21-14764-7
Jag har presenterat böckerna i ett tidigare brev, men tycker att de nu igen är speciellt aktuella i
och med den nya timplanen i grundskolan. Böckerna är dyra men är definitivt värda att satsa
på då man skall undervisa kemi och fysik i lågstadiet. Laborationsbeskrivningarna utgör
kopieringsunderlag så tanken är nog att man skaffar ett exemplar av böckerna till en skola och
sedan är det fritt fram att kopiera det material som eleverna behöver då de skall jobba.
5
Böckerna innehåller en mängd laborationer med enkelt förklarad teori. De kan vara till stor
hjälp dels för att man skall hitta lämpligt material, dels för att hitta ”rätt nivå”.
Böckerna kan man skaffa via Schildts förlag; pris i mk är 580 mk resp. 690 mk. Beställer man
via bol.com är priset nästan det samma: ca. 570 mk resp 680 mk. Beställer man däremot
böckerna från förlaget i Sverige: www.liber.se är priset ungefär det samma, men i kronor; 580
SKr resp. 690 SKr. Postkostnaderna från Sverige är dock orimligt höga så det kan ju hända att
man inte sparar så många mark med att beställa därifrån.
Undervisningsidéer
Par-bingo
En grupp av årets ämneslärarauskultanter har utvecklat en ”bingo-övning” som jag tycker är
så bra att jag gärna delar den med er (med auskultanternas tillstånd). Övningen kan man
använda i olika sammanhang (läxförhör, repetition inför prov mm.). För uppgiften behöver
man 2 olika frågekort (t.ex. 5 x 5 rutor, med en fråga per ruta). Till frågorna bör dessutom
göras likadana svarskort, som limmas fast på baksidan av kortet. Utöver detta bör varje
deltagare ha ett tomt rutsystem, där hon/han lägger ett kryss i den ruta hon själv svarat rätt på
och ritar en boll för ett orätt svar.
Eleverna sätter sig så att de sitter mitt emot varandra, i en lång rad.
Frågekort 1
Svarskort 1
Frågekort 2
Svarskort 2
Eleverna som sitter mitt emot varandra får nu ställa varsin fråga till varandra. Man väljer
fråga genom att välja någon ruta, t.ex. ruta N3.
Då ett elevpar ställt varsin fråga till varandra, flyttar den ena raden elever ett steg så att alla nu
har ett nytt par att ställa en fråga till, och få en fråga av. På detta sätt fortsätter man tills någon
fått BINGO, dvs. fem i rad.
Ett frågekort kan t.ex. se ut enligt följande:
6
B
1
2
3
4
5
Vilken är den
kemiska
beteckningen för
järn?
Vilken halogenid
finns det mest av i
tandemaljen?
I
Vad anger pHvärdet?
N
G
Vilken är den
Vilket
kemiska
grundämne finns
beteckningen för
det mest av i
saltsyra?
människan?
O
Vad innebär en
indunstning?
Av vilka två
ämnen kan man
tillverka
salmiak?
Vilken färg har en
Vilken är den
Vilken gas kan
Vilken är den
Vilka pH-värden
basisk lösning som
kemiska
man påvisa med
kemiska
har basiska
innehållet
beteckningen för
hjälp av
beteckningen för
ämnen?
indikatorn BTB?
en hydroxidjon?
kalkvatten?
kväve?
Vilken är den
Vad bildas då
Vilken bas
Hur neutraliserar
kemiska
Vad menas med
man förbränner
kallas även för
man sur jord?
beteckningen för
en jon?
stearin?
lut?
syre?
Vilken är
Är tvättmedel
Vilken är den
likheten mellan
Vilken syra
Vad menas med
som används för
kemiska
järn som rostar
används som
en mättad
klädtvätt sura,
beteckningen för
och mat som
ackumulatorvätska?
lösning?
neutrala eller
bordssalt?
förmultnar i en
basiska?
kompost?
Hur släcker man Vad bildas då en
brinnande
syra
bensin?
neutraliseras?
Nämn en syrabas indikator
som vi kan äta.
Svarskortet:
B
I
N
G
O
Fe
Surhetsgrad.
HCl
Syre
Ett fast löst ämne
tas till vara då
vätskan
avdunstar.
Fluorid
Kväver elden, så
att syre ej finns
tillgängligt.
Salt + vatten
Rödkål, blåbär,
te.
Saltsyra +
ammoniak.
3
Blå
OH-
8-14
Koldioxid, CO2
4
Man kalkar jorden.
Koldioxid och
vatten.
O
En laddad
partikel.
Natriumhydroxid,
NaOH.
NaCl
En lösning som
inte kan lösa
upp mera av det
lösta ämnet.
Reaktion med
syre.
Basiska
1
2
5
Svavelsyra, H2SO4
N
För att spela bingo bör halva gruppen ha frågekort med andra frågor. Eftersom frågorna ju är
beroende av sammanhanget är det svårt för mig att göra färdiga frågekort; ni vet bäst själva
vilka frågor ni kan ha med. (Därför exempel på endast ett frågekort.)
Det egna kortet där man kryssar i sin bingorad:
7
B
I
N
G
O
1
2
3
4
5
Fasta ämnen – vätskor - gaser
Den didaktiska forskningen inom naturvetenskap har under de gångna ca 20 år sysslat med
frågor som gäller barns, ungas men även vuxnas uppfattningar som berör naturvetenskapliga
fenomen och begrepp. Forskningen visar tydligt att en mängd uppfattningar är djupt
förankrade hos människan, uppfattningar som kan ligga rätt långt ifrån eller stå i strid med de
naturvetenskapligt vedertagna förklaringarna.
Man vet idag att elevernas egna förhandsuppfattningar har stor betydelse för deras inlärning.
Dessa uppfattningar har också visat sig vara rätt resistenta gentemot undervisning; eleverna
kanske lär sig vad som är rätt svar till provet, men vidhåller sin egen uppfattning utanför
skolan. Det är väsentligt att vi som lärare är medvetna, dels om att elever har egna
uppfattningar (de är inte oskrivna blad, som vi bara behöver skriva in ny kunskap i), dels vilka
dessa uppfattningar är. Det är viktigt att vi i vår undervisning beaktar detta, dvs. tar reda på
vad eleverna egentligen tror och tänker, och bygger upp vår undervisning så att vi kan utmana
elevernas tänkande, få dem att se att deras egen modell kanske måste kompletteras, utvecklas
eller helt bytas ut för att de skall förstå ett fenomen.
8
Som mål för vår undervisning bör vi väl ha att eleverna skall uppnå en viss förståelse av
naturvetenskapliga fenomen och begrepp, inte att de kan ge ”mekaniska svar” på våra
provfrågor. I våra läroböcker behandlas begreppen fast ämne, vätska och gas förhållandevis
förenklat. Som exempel på ett fast ämne finns vanligen en bild av en träbit eller en metall.
Men uppnår eleverna en djup förståelse via dessa enkla exempel? Hur är det med pulver,
mjuka föremål såsom tyg eller bomull; hur förklara vi att de är fasta? För att eleverna skall
uppnå en djupare förståelse bör vi också kunna ta upp mera problematiska exempel.
Här kommer ett förslag till en övning som man kan använda då man i årskurs 7 behandlar
aggregationstillstånden (kan även fungera bra i gymnasiets första klass, som en fördjupning
av temat).
Låt eleverna jobba i grupper på 2-4 (helst 3).
Högstadiet
Lägg olika typer av fasta ämnen i genomskinliga burkar (t.ex. metallbitar, stenar, sand, mjöl,
tyg, plast, modellera, gummiband).
Berätta att alla burkarna innehåller fasta ämnen. Låt eleverna undersöka innehållet i burkarna
genom att iaktta, känna, studera med förstoringsglas, skaka burkarna osv. Låt eleverna
fundera på hur de skulle beskriva ett fast ämne.
Hjälp eleverna att tänka och formulera sig med lämpliga frågor, t.ex.
vad händer med burkens innehåll då man skakar burken?
vad händer om du lägger burken på sidan?
hur känns ämnet i burken om du tar i det?
vad har alla ämnena gemensamt med varandra?
Fortsätt med att låta eleverna ge exempel på andra fasta ämnen. Låt eleverna försöka skriva en
beskrivning av vad som menas med ett fast ämne.
Låt de olika grupperna berätta vad de kommit fram till. Diskutera er fram till en eventuell
gemensam definition.
Gymnasiet
Låt eleverna jobba i grupper på 2-4 (helst 3).
Ge varje grupp 4 burkar med olika typer av fasta ämnen:
Burk 1: metallbit, träbit eller sten; ett fast hårt ämne
Burk 2: sand, gryn, mjöl
Burk 3: bomull; fast ämne som är mjukt, böjligt, kan pressas ihop
Burk 4: modellera
Låt eleverna studera materialet i burk 1 och utgående från detta material skriva en definition
av ett fast ämne är.
Efter detta får de ta burk 2, testa sin definition, och modifiera den så att den stämmer in även
på innehållet i denna burk, och därefter fortsätta med de andra burkarna.
9
Diskutera tillsammans i klassen gruppernas definitioner och försök få eleverna att hitta en
gemensam korrekt definition.
Högstadiet
På ett liknande sätt kan vi behandla vätskor.
Vad har alla vätskor gemensamt med varandra, vad skiljer dem från varandra?
I detta fall kan ni ha burkar med t.ex. vatten, matolja, sirap, mjölk.
Några frågor som kan användas som vägledning:
Hur känns de olika ämnena?
Hur ser de ut?
Hur rör de sig om du vrider på burken?
Vad händer om du lägger burken på sida?
Vilka egenskaper är gemensamma för dessa vätskor?
Ge exempel på andra vätskor.
För många barn är begreppet ”gas” problematiskt. Forskning visar att ”gas” av många
uppfattas som något giftigt och farligt, gas är inte materia och saknar därför massa.
Ge eleverna i uppgift att hämta en gas åt dig. Låt plastpåsar, ballonger, askar ligga framme
utan att du desto mera nämner om det.
Fundera på hur man vet att det finns en gas, när kan man se en gas, kan man känna en gas?
Doft – en gas
Låt eleverna sluta ögonen. Sätt på stilla musik. Uppmana eleverna att tänka sig till en viss
tidpunkt, årstid, plats. Be dem känna efter någon doft som de förknippar med denna tidpunkt.
Låt eleverna beskriva sin doft.
Placera kärl med hett vatten på olika ställen i klassen. Be eleverna sluta sina ögon. Droppa i
något doftämne (t.ex. citron, apelsin, pepparmint, parfym). Be eleverna berätta vad de känner
och upplever.
Fundera tillsammans över vad doft egentligen är.
Vad sker med ett ämne som avger doft?
Vad består doft av?
Du behöver
sinol el motsv.
träribba (30-40 cm)
snöre, gummiband
2 tygbitar (ca 10 x 10 cm2)
2 häftstift
Häll upp lite alkohol (t.ex. sinol) i en bägare (OBS! giftigt!). Har ämnet någon doft eller
lukt?
10
Gör en ”balansvåg”. Se fig.
Häng upp en torr tygbit i ena ändan
av den lodräta staven, en tygbit
fuktad med alkohol eller aceton i de
andra. Ställ in ”vågen” så att den
väger jämnt, dvs. att staven, som
tygbitarna är fästade vid, är vågrät.
Följ med vad som händer.
Förklara, med hjälp av materiens
partikelnatur, vad som händer.
Skillnaden mellan fasta ämnen, vätskor och gaser
Undersök en gas (luft), vätska (vatten) och ett fast ämne (sand) i en injektionsspruta. Kan de
olika formerna komprimeras (sammanpressas)? Försök förklara resultatet utgående från
materiens partikeluppbyggnad.
Dramatisering
För att skapa en första förståelse av att materia är uppbyggt av partiklar och av att dessa
partiklars rörlighet förändras, då ett fast ämne smälter och vidare övergår i gasform, är
dramatiseringen ett utmärkts sätt att konkretisera detta på.
Fundera tillsammans på hur man i klassen kunde dramatisera detta.
Diverse
Kungsvatten
Vi vet alla att vi för att lösa upp guld måste använda en blandning av salpetersyra och
saltsyra. Däremot är det inte säkert att alla vet den kemisk förklaring till detta. I boken
”Kemiska mellanslag” av Stig Olsson stötte jag på följande förklaring.
Upplösningen av guld i salpetersyra bygger på följande två jämviktsreaktioner:
Au + NO3- + 4 H3O+
Au3+ + NO + 6 H2O
(1) (jämvikten förskjuten åt vänster)
I en blandning med saltsyra kommer guldjonerna att bilda ett komplex med klorid
11
Au3+ + 4 Cl-
AuCl4- (tetrakloroaurat(III)-jon)
(2) (jämvikten förskjuten åt höger)
Guldjonerna som bildas i reaktion 1 reagera således vidare med kloridjoner och påverkar
därmed reaktion 1, där nya guldjoner bildas för att jämvikten skall återupprättas.
Laborationer
Kopparcykel i mikroskala
I kompendiet ”Kemiskt kylskåp och förgasad tavelkrita” som utkom 1998 (PF:s serie med
undervisningsmaterial) ingår en laboration kallad kopparcykeln. Det har visat sig att denna
laboration inte alltid vill lyckas. Jag har därför nu jobbat lite med den, och tror mig ha kommit
underfund med var problemet ligger. Jag skall i detta brev ge en ny beskrivning över
experimentet, denna gång i mikroskala, och samtidigt visa på var jag tror att felet tidigare
uppstått. I försöket utgår man från en kopparbit, som löses upp i salpetersyra. Efter att
kopparn genomgått ett antal reaktioner bör man i slutet av försöket återfå den ”rena kopparn”.
Kemikalier
100 mg koppar
6 M HNO3
6 M NaOH
3 M H2SO4
6 M H2SO4
Zink-pulver
Tillbehör
10 ml e-kolv
kokplatta
magnetomrörare
”sandbad”
pH-papper
filtrerpapper + tratt
Säkerhet
Salpetersyra och natriumhydroxid är frätande. Reaktionen mellan koppar och salpetersyra ger
giftiga kväveoxider.
Utförande
1. Väg upp 100 mg koppar (anteckna exakta mängden om ni gör försöket kvantitativt) i en
10 ml e-kolv.
Tillsätt 2 ml 6 M HNO3. Obs gör detta i ett dragskåp! Värm på en kokplatta. Fortsätt
uppvärmningen tills all koppar löst upp sig och inga bruna gasångor mera avges från
kolven. Kyl av kolven och tillsätt därefter 2 ml destillerat vatten.
Vilka iakttagelser kan ni göra (hur har innehållet i lösningen förändrats, hur ser man att en
kemisk reaktion skett?)? Vad har bildats i lösningen?
12
2. Placera e-kolven i ett ”sandbad” ovanpå en magnetomrörare (lägg i en magnet i kolven).
Droppa 6 M natriumhydroxid till lösningen tills lösningen blir svagt basiskt (obs! sluta
direkt då lösningen blivit basisk – här gör man lätt fel).
På vilket sett har innehållet i kolven förändrat utseende?
Vilken kopparförening har bildats?
3. Värm upp e-kolven genom att vrida upp värmen på
magnetomröraren (temp. på ”sandbadet” ca 110-115 C).
Vilka iakttagelser kan ni göra gällande innehållet i kolven?
Vad har bildats?
4. Låt blandningen svalna. Ta bort magnetomröraren. Filtrera
lösningen (eller låt fällningen sjunka till botten eller
pipettera bort vätskan). Skölj fällningen med 2 ml
dest.vatten.
5. Lös upp fällningen i ca 6 ml 3 M H2SO4. Se till att all
fällning löser sig.
6. Tillsätt ca 800 mg zinkpulver till lösningen (gör detta i
dragskåp). Rör om lösningen med en glasstav. Hur kan du
iaktta att en reaktion sker?
Koppar
Upplösning
i HNO3
Kopparnitrat
Reaktion
med NaOH
Kopparhydroxid
Uppvärmning
Kopparoxid
Reaktion med H2SO4
7. Då all kopparoxid reagerat kan eventuell överskott av
zinkmetall lösas upp genom att du tillsätter 5 ml 6 M
svavelsyra. Rör om.
Kopparsulfat
Reaktion med
8. Låt kopparfällningen sjunka till bottnen och dekantera
därefter bort vätskan. Skölj några gånger med lite dest. vatten och dekantera bort vätskan
mellan sköljningarna.
9. Väg upp ett filtrerpapper och placera i en liten tratt. Häll lösningen genom filtrerpappret.
Se till att du får med all fällning (skölj med dest. vatten). Låt fällningen torka till nästa
gång. Väg fällningen.
10. Beräkna hur många procent av den ursprungliga kopparn du återfått. Analysera eventuella
felkällor.
Om laborationen görs exempelvis i kurs 3 i gymnasiet kan eleverna gärna även få i uppgift att
skriva reaktionslikheter.
Cu + 4 HNO3 Cu(NO3)2 + 2 H2O + 2 NO2 (bildas rödbrun NO2-gas, blå lösning, värme)
13
zink
Cu(NO3)2 + 2 NaOH Cu(OH)2 + 2 NaNO3 (blå fällning)
Cu(OH)2 CuO + H2O (svart fällning)
CuO + H2SO4 CuSO4 + H2O (blå lösning)
CuSO4 + Zn Cu + Zn SO4 (rödbrun fällning, värme + överskott zink kan reagera med
svavelsyra och ge vätgas)
Identifiering av PVC-plast
Var vi än bor i landet uppmanas vi idag att sortera vårt avfall. Hur denna sortering skall göras
är ju delvis beroende av var vi bor. Vi som bor här i Vasa-trakten skall bl.a. dela upp vårt
avfall i köksavfall och grovavfall. I köksavfallet uppmanas vi sätta det mesta av vårt
plastavfall, dock inte PVC-plast (eftersom en del av detta avfall skall brännas, och
förbränningen ger upphov till bl.a. sur väteklorid). För gemene man är det inte alltid helt lätt
att veta hur man skall känna igen PVC-plast. En utmärkt metod, som man gärna kan lära ut i
klassen och samtidigt koppla metoden till miljövård, är användningen av Beilsteins prov för
att påvisa klor (metoden kan användas även på andra klorföreningar, t.ex. för att testa om
pesticider innehåller klorid).
Till försöket behöver man
koppartråd
bunsenlåga (eller stearinljus, med tilläckligt het låga, värmeljus räcker antagligen inte)
Hetta upp en koppartråd i en bunsenlåga en stund så att det på tråden hinner bildas ett skikt av
svart kopparoxid, CuO.
Placera den heta tråden mot plastföremålet som du vill undersöka. Om plasten innehåller
klorid kommer kopparoxid att reagera med denna och kopparklorid, CuCl2 bildas.
Placera nu koppartråden i lågan på nytt. Om lågan färgas grön (vanlig låg-test) innebär detta
att plasten innehåller klorid, dvs. är PVC-plast, som inte får brännas.
Enkelt att utföra även därhemma!
Gummiband och värme
Försök 1
Dela ut ett gummiband åt alla elever.
14
Tag i vardera ändan av gummibandet, placera gummibandet löst mot dina läppar, drag ut det
(behåll kontakten med läpparna). Kan du känna någon förändring hos gummibandet (varmt
eller kallt)? Vänta ½ min. släpp därefter ihop gummibandet igen, fortfarande mot dina läppar.
Hur känns det?
Gummi hör till en grupp av ämnen som kallas elastomerer, dvs. ämnen med utpräglat
elastiska egenskaper. Naturgummi, polyisopren, är en elastomer. Vulkaniserat naturgummi
kan tom. töjas till 1500 % av sin ursprungliga längd.
I en elastisk polymer är molekylkedjorna i fullständig oordning, intrasslade i varandra ungefär
som en garnhärva (entropin är hög).
Då man töjer ut gummit kommer molekylkedjorna att orientera sig i töjningens riktning,
ordningen ökar.
Då man släpper av gummit söker sig kedjorna tillbaka till sina oordnade platser.
Att ordna upp molekylkedjorna i ett gummiband är en exoterm process; gummibandet känns
varmt mot våra läppar då vi drar ut det. Då vi släpper av bandet, och det återgår till sin
ursprungliga form, minskar temperaturen.
Försök 2a (demonstration)
Häng upp en tyngd i ett gummiband, som i sin tur får hänga t.ex. i ett stativ. Placera en linjal
bakom gummibandet. Låt eleverna gissa vad dom kommer att hända då du värmer upp
gummibandet (blir bandet, längre eller kortare?).
Värm upp bandet med en hårtork (inte bunsenlåga!) eller en värmelampa. Iakttag vad som
händer.
Försök 2b
Vad är det som händer?
Använd ett långt rep. Låt exempelvis 7 elever hålla i repet och placera sig enligt bilden.
15
Eleverna och repet föreställer nu en polymerkedja.
Vad händer om vardera ändan ”dras ut” dvs. går åt motsatt håll? Kedjar rätar ut sig.
Då vi värmer upp kedjan tillför vi energi vilket gör att atomerna börjar röra på sig mera. Vad
händer med kedjans längd om atomerna börjar röra på sig mera? Kedjan drar ihop sig och blir
kortare.
Detta är således vad som i princip händer då vi värmer upp gummibandet.
Källor:
Fun with Chemistry. Vol. 1
Institute for Chemical Education 1991
The Chemistry of polymers
2nd Ed.
John W Nicholson
RSC Paperbacks 1997
Macrogalleria
http://www.psrc.usm.edu/macrog/index.htm
16
Kristallbildning i en gel
I informationsbrev nr. 5 skrev jag om hur man gör en kemisk trädgård. Denna gång skall jag
beskriva hur man kan studera bildningen av ”metallkristaller” vid kemiska reaktioner i en gel.
Reaktionerna blir på detta sätt långsammare än i vanlig lösning och man bör därför helst ha
möjlighet att studera reaktionerna flera dagar i följd.
Kemikalier
Tillbehör
Utspädd natriumsilikatlösning (1 del
provrör
natriumsilikatlösning + 4 delar
stålull
dest.vatten)
1 M ättikssyra
1 M CuSO4
10 % NaCl
Metallbitar (gärna ganska stora) t.ex.
järn, zink, aluminiumfolie, magnesium
Säkerhet
Natriumsilikat är frätande.
Utförande
Häll 5 ml ättikssyra i 4 provrör (lika många som du har olika metallbitar).
Tillsätt 12 droppar kopparsulfatlösning. Rör om.
Tillsätt 5 ml natriumsilikatlösning. Rör om. Obs! natriumsilikat är frätande.
Värm provrören på vattenbad så påskyndar du gel-bildningen.
Då lösningen stelnat sätter du i en metallbit i varje provrör (putsa vid behov metallen med
stålull så att du får bort oxid-skiktet). Skuffa ner biten så att den är nerdoppad i gelen. Tillsätt
ett per droppar natriumkloridlösning. Stäng provrören med en gummikork eller parafilm. Låt
provrören stå några dagar och följ med vad som händer.
Kopparjonerna i lösningen kommer att reagera med metaller. Förklara varför. Hur kan man se
detta? Beskriv dina iakttagelser. Vilken metall reagerar snabbast, långsammast? Gör en
hypotes. Följ med och se om din hypotes stämmer.
Polära och opolära vätskor
Alla har vi väl i något skede demonstrerat vattnets polaritet med hjälp av en elektriskt
uppladdad ebonitstav, kam eller motsvarande. Samma metod kan ju användas för att
undersöka olika vätskors polaritet, t.ex. metanol, etanol, propanol, hexan, cyklohexan.
17
Fyll vätskan i en byrett (i mikroskala i en pipett). Låt vätskan sakta rinna ut och studera om
vätskestrålen påverkas av det laddade föremålet (ebonitstaven, kammen el. motsv.) genom att
föra föremålet i närheten av strålen.
Använd rena kärl så kan vätskorna återanvändas.
Från Internet
Att skriva kemiska formler i Word
Filen normal.dot är en fil som läses in av Word när man startar programmet. Den
innehåller inställningar av verktygsfälten. På nätet finns nu en variant av filen som ger
dig färdiga knappar för kemiska formler. Du kan alltså byta ut din vanliga normal.dot
till den som finns här. (Spara först originalfilen normal.dot på diskett eller i en annan
katalog på hårddisken, för att du skall kunna gå tillbaka till den om du så önskar.)
Filen hittar du om du går via Skolkemis sidor i Umeå och där väljer i menyn
”verktyg”:
http://school.chem.umu.se/
I samma verktygsmeny kan du också hitta recept till en del vanliga indikatorer. Kan vara bra
att veta!
Nordlab
Inom de nordiska länderna pågår för tillfället ett samarbetsprojekt vars syfte är att ge ”framför
allt lärarna i naturvetenskapliga ämnen redskap att förbättra och förnya sin undervisning”.
Projektet omfattar även matematikundervisningen. Väsentligt i projektet har varit att aktuell
ämnesdidaktisk forskning skall komma fram, men också att intressant och användbart
underviningsmaterial skall produceras, material som skall kunna användas av lärarna ute på
fältet. Projektet finansieras av Nordiska ministerrådet. Inom ramen för Nordlab svarar varje
nordiskt land för ett eget delprojekt. Dessa är följande:
Danmark: Experimentellt arbete i naturvetenskap
Finland: IT i naturvetenskaplig undervisning
Island: Samhällets energiförsörjning
Norge: Elevers självvärdering i matematik
Sverige: Elevtänkande och undervisning i naturvetenskap.
18
Via hemsidorna vid Göteborgs Universitet kommer man åt projektets sidor i de olika nordiska
länderna. De olika länderna har i varierande grad lagt ut sitt material på nätet, t.ex. Sverige
har ett utmärkt material som är tillgängligt för alla. Adressen till Nordlab är:
http://na-serv.did.gu.se/nordlab/nadid.html
Det svenska materialet kräver tills vidare ett lösenord för att man skall komma åt materialet,
men lösenordet får man genom att sända ett e-postmeddelande till den adress som finns given.
Mera material om plaster
I senaste brev skrev jag om Platform-materialet som numera kan laddas ner från nätet på det
språk man själv önskar (se brev nr. 9). En bra svensk sida, med undervisningsmaterial,
kopierbara färgfolier och en hel del information om plaster hittar man under ”Plast- och
kemibranschen”:
http://www.plast-kemi.se/
Några sidor om återvinning och miljö:
Pappersåtervinning
En sida med mycket informativt material om papper, återvinning av papper, länkar till
skogsindustri mm. Tyvärr är materialet på finska (finns länkar till en del svenska sidor). Här
kan man också hitta en del användbara folier
http://www.paperinkerays.fi/
Ozonkartor
http://lap.physics.auth.gr/ozonemaps/
Naturvårdsverkets hemsida
http://www.environ.se/
19
Miljöförvaltning i Finland
Huvudsidan finns på svenska, däremot märker man att en hel del av materialet enbart finns på
finska
http://www.vyh.fi/sve/
World Chemistry
Engelsk innehållsrik kemisida. Innehåller bl.a. interaktiva undervisningsmaterial (t.ex.
titreringar, gasdiffusion, periodiska systemet och periodicitet), ordlista över vanliga kemiska
begrepp, tredimensionella bilder av molekyler mm.
För att komma åt materialet måsta man skriva in sig som medlem, men detta är gratis.
http://209.213.125.106/wldchem/home/index.htm
Humor; länksamling i naturvetenskap, teknik och matematik
http://dbhs.wvusd.k12.ca.us/Humor/HumorIndex.html
Har ni t.ex. tänkt på att 1012 mikrofoner = 1 megafon eller att
10 monologer = 5 dialoger eller att
10¯2 mental = 1 centimental (eng.)
Och visst är det ju så här då det gäller datorer:
Murphy's Computer Laws (inte precis kemi men ändå relevant i vårt arbete.)
1. No matter how many resources you have, it is never enough.
2. Any cool program always requires more memory than you have.
3. When you finally buy enough memory, you will not have enough disk
space.
4. Disks are always full. It is futile to try to get more disk space. Data expands
to fill any void.
5. If a program actually fits in memory and has enough disk space, it is
guaranteed to crash.
6. If such a program has not crashed yet, it is waiting for a critical moment
before it crashes.
7. No matter how good of a deal you get on computer components, the price
will always drop immediately after the purchase.
8. All components become obsolete.
20
9. The speed with which components become obsolete is directly proportional
to the price of the component.
10. Software bugs are impossible to detect by anybody except the end user.
Science cartoons
En stor samling med serieteckningar som har anknytning till bl.a. naturvetenskap:
http://www.strange-matter.com/index.html
Här ett litet exempel
Några rikssvenska läromedelsförlag
Vi får ju inte alltid de rikssvenska läromedelskatalogerna sända till oss i Svenskfinland. Idag
är detta inte så stort problem i och med att man ju själv kan se vilka böcker som finns, genom
att gå till förlagens hemsidor. Här är adressen till några:
Natur och kultur
http://www.nok.se/
21
Libers förlag
http://www.liber.se/
Ekelunds förlag
http://www.ekelunds.se/
Gleerups förlag
http://www.gleerups.se/
Bonniers utbildning
http://www.bonnierutbildning.se/
22