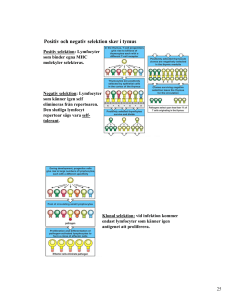
t.ex. virus och celler, inkluderande bakterier
advertisement

Artificiella antikroppar mot biopolymerer (t.ex. proteiner) och biopartiklar (t.ex. virus och celler, inkluderande bakterier) Stellan Hjertén Institutionen för naturvetenskaplig biokemi och organisk kemi, Biomedicinskt Centrum, Box 576 751 23 Uppsala Projekt: 18/04 Inledning Vad utmärker en antikropp? En antikropp är ett protein, som har den unika egenskapen att spontant fästa sig vid en viss substans, men i idealfallet inte till andra substanser. Antikropparna får man genom att injicera denna substans, kallad antigen, i ett försöksdjur. Eftersom antigenet ej tillhör djurets egen uppsättning av proteiner uppfattas det som främmande (obehagligt), varför djuret vill oskadliggöra det, vilket det gör genom att tillverka en antikropp (ett protein) med egenskapen att binda sig till det främmande ämnet och om möjligt på så sätt neutralisera det främmande ämnets negativa konsekvenser för djuret. Efter några veckor då halten av antikropparna är hög tappas djuret på blod, från vilket antikropparna isoleras för en rad olika applikationer, t. ex. (1) som vaccin mot olika sjukdomar, (2) för att spåra ett antigen (biomarkör) som ändrar sin koncentration vid en sjukdom, t. ex. en viss typ av cancer och sedan bestämma koncentrationen av detta markörprotein, (3) för att fastlägga koncentrationen av en viss cellkomponent, ett ofta återkommande problem inom många biovetenskaper, etc. Dessa och flera liknande tester är mycket vanliga och antalet försöksdjur, som användes är följaktligen mycket stort. Det faktum att testerna är mycket enkla bidrar naturligtvis till populariteten. Vid sjukhusanalyser tar man ett blodprov från patienten och centrifugerar bort blodkroppama. Till återstoden sätter man antikroppen till det protein, som produceras i relativt stor mängd vid den sjukdom man misstänker att patienten har. Ju högre koncentrationen av komplexet antigen/antikropp är, desto större är halten också av antigenet, dvs av markörproteinet för sjukdomen. Denna koncentrationsbestämning användes sedan för att fastställa diagnosen. Den ovan skisserade användningen av proteinantikroppar för selektiv bestämning av halten av en viss substans har uppenbara fördelar och är därför mycket populär. Nackdelarna är att (1) försöksdjur måste utnyttjas med de etiska problem detta medför, (2) metoden ur ekonomisk synpunkt är kostsam, (3) framställningen av en proteinantikropp tar flera veckor, vilket inte bara kan vara plågsamt för försöksdjuret, utan även försinkar många planerade försök, (4) dessa antikroppar är av proteinnatur och därför lätt förlorar sin aktivitet, (5) proteinantikroppar ej kan skapas mot nativa virus och celler t. ex. bakterier, sporer, etc. eftersom dessa bryts ned metaboliskt i försöksdjuret. Tillverkningen av artificiella antikroppar. En vattenlösning av s. k. monomerer blandas med en vattenlösning av antigenet. Monomererna får sedan reagera med varandra och bildar då ett nätverk i form av en gel (ge1é) i vilken antigenmolekylema, t. ex. proteiner, är inneslutna. Då antigenmolekylerna tvättats bort lämnar de hålrum, vilkas form överensstämmer med formen på denna antigenmolekyl, d.v.s. en formselektivitet har skapats. Inga andra molekyler passar exakt in i denna hålighet. Den täta kontakten mellan antigenet och hålighetens vägg gör att bindningar skapas mellan dem, d.v.s. vi får även en bindningsselektivitet. Ju fler typer av oberoende selektiviteter vi introducerar, desto högre blir den totala selektiviteten och desto mindre strukturella skillnader mellan två antigener kan vi detektera, vilket ju är ett av syftena med vårt forskningsprojekt (Syfte c, nedan). 1 Det bör observeras att syntesmetoden är universell i den bemärkelsen, att den kan envändas för både proteiner, virus och celler och säkerligen också för många andra typer av polymerer och partiklar. Man behöver alltså inte lägga ner arbete på modifiering av vår metod för varje nytt antigen. Det övergripande syftet med vårt projekt är, att (a) utveckla en method där alla de ovan beskrivna nackdelarna har eliminerats, (b) finna enkla metoder för att detektera antigenet, (c) ytterligare öka den redan nu höga selektiviteten, (d) visa den praktiska användningen av gelantikropparna, (e) tillverka gelantikropparna i form av nanopartiklar för att testa om dessa kan användas som vaccin. Uppnådda resultat. Syftet (a) har uppnåtts. Vi har framställt gelantikroppar mot humant och bovint hemoglobin, myoglobin från häst, transferrin med och utan järn, cellulas, vildtyp och mutant av Semliki Forest Virus, olika stammar av E. coli bakterier, olika typer av bakterier. Syfte (b). Vi har utarbetat metoder baserade på analys av eluatet från en kolonn uppbyggd av gelantikroppar, färgning av antigenet, mätning av fluorescensen av komplexet antigen/gelantikropp, masspektrometri, QCM (en sorts mikrovåg). Ytterligare metoder kommer dock att prövas. Syfte (c). Som nämnts ovan under Tillverkningen av artificialla antikroppar har vi en total selektivitet, basaerad på form- och bindningsselektivitet. Den totala selektiviteten har vi ökat genom att införa ytterligare en selektivitetsfaktor, nämligen laddningen av komplexet gelantikropp/antigen. Ett mått på denna laddning får man om man bestämmer hur snabbt komplexet vandrar i ett elektriskt fält. För detta ändamål använder vi den ursprungliga s.k. fria zonelektroforesapparaten (som jag konstruerade 1958). Denna teknik, baserad på tre selektivitetsprinciper, är troligen den enklaste och mest känsliga som finns för att upptäcka små skillnader i strukturen av proteiner, virus, bakterier, etc. Som exempel vill vi nämna att med denna teknik kan vi särskilja vildtyp och mutant av Semliki Forest Virus, trots att den strukturella skillnaden endast är tre aminosyror i ett av de tre proteinerna på ytan av viruspartikeln. En granskare av vår uppsats kallade idén revolutionerande. Syfte (d). Som exempel på den praktiska användningen av gelantikropparna kommer vi snart att studera: Kliniska applikationer för gelantikroppar. Det är svårt att hitta ett enklare och lika pålitligt analysredskap som antikropparna inte bara inom den ovan nämnda kliniska diagnostiken, utan även inom ett mycket stort antal andra områden, t. ex. för detektering av patogena virus, sporer (Anthrax) och bakterier i luft/vatten/födoämnen; för analys av blod på HIV, West Nile Fever och Hepatitis före en blodtransfusion, vilket är en vanlig försiktighetsåtgärd på flera sjukhus; kanske för eliminering av toxiner, virus (HIV) och cirkulerande cancerceller i kroppsvätskor, en teknik som möjligen kan ha samma effekt som ett vaccin (tekniken finns utarbetad för andra ändamål). Applikationsområdet är alltså enormt stort. Syfte (e) att tillverka vaccin har ännu ej påbörjats. Nedan presenteras i korthet en jämförelse av fördelarna med syntetiska gelantikroppar och med proteinantikroppar, producerade i försöksdjur: Fördelar med syntetiska antikroppar, jämfört med proteinantikroppar: 2 a) Inga försöksdjur krävs. b) Billigare att framställa. c) Selektiviteten är högre, eftersom endast en del av proteinantikroppens yta är i kontakt med antigenet, medan hela antigenets yta är i kontakt med den syntetiska gelantikroppens hålighet, vilket betyder, att såväl form- som bindningsselektiviteten är högre för de syntetiska antikropparna. Den tredje selektivitetsparametern, baserad på laddningen av komplexet antigen/antikropp, kan ej utnyttjas för proteinantikropparna, eftersom det i praktiken är mycket svårt att renframställa detta komplex. Motsvarande svårighet existerar ej för de syntetiska gelantikropparna, eftersom komplexet utgöres av gelpartikeln med bundna antigenmolekyler vilket genom en enkel sedimentation eller centrifugering lätt kan isoleras och sedan underkastas en elektroforetisk analys, såsom ovan beskrivits. Fördelar med proteinantikroppar framställda i försöksdjur: Metoder finns redan utarbetade för framställning av vaccin, baserade på proteinantikroppar. Det är emellertid troligt att artificiella gelantikroppar i form av nanopartiklar också kan användas som vaccin. Denna möjlighet bör snarast undersökas. Kan vår teknik ersätta de konventionella proteinantikropparna och på så sätt begränsa djurförsöken? I diskussionerna ovan har denna fråga intagit en central plats och de visar otvetydigt att så är fallet men endast om ytterligare ekonomiska resurserna kan tillgodoses. Publikationer 2005-2006 för forskningsområdet artificiella gelantikroppar. Rezeli, M., Kilár, F., Hjertén, S. Monolithic Beds of Artificial Gel Antibodies. J. Chromatogr. A 2006, 1109, 100-102. Takátsy, A., Kilár, F., Hjertén, S. Universal Method for Synthesis of Artificial Gel Antibodies by the Imprinting Approach, Combined with a Unique Electrophoresis Technique for Detection of Minute Structural Differences of Proteins, Viruses and Cells (Bacteria) Ia. Gel Antibodies against Proteins (Transferrins), accepted for publication in J. Sep. Sci., 2006. Takátsy, A., Végvári, Á., Kilár, F., Hjertén, S. Universal Method for Synthesis of Artificial Gel Antibodies by the Imprinting Approach Combined with a Unique Electrophoresis Technique for Detection of Minute Structural Differences of Proteins, Viruses and Cells (Bacteria) Ib. Gel Antibodies against Proteins (Hemoglobins), accepted for publication in Electrophoresis, 2006. Takátsy, A., Sedzik, J., Kilár, F., Hjertén, S. Universal Method for Synthesis of Artificial Gel Antibodies by the Imprinting Approach Combined with a Unique Electrophoresis Technique for Detection of Minute Structural Differences of Proteins, Viruses and Cells (Bacteria) II. Gel Antibodies against Viruses (Semliki Forest Virus), accepted for publication in J. Sep. Sci., 2006. Bacskay, I., Takátsy, A. Végvári, Á., Elfwing, A., Ballagi-Pordány, A., Kilár, F., Hjertén, S. Universal Method for Synthesis of Artificial Gel Antibodies by the Imprinting Approach Combined with a Unique Electrophoresis Technique for Detection of Minute Differences in the 3-D Structure of Proteins, Viruses and Cells (Bacteria) III. Gel Antibodies against Cells (Bacteria), accepted for publication in Electrophoresis, 2006. 3 Artificial Gel Antibodies against Proteins, Viruses and Bacteria Conventional antibodies are proteins which are raised in experimental animals by injection of a foreign substance which the animal does not recognize and, therefore, tries to neutralize it by synthesizing a protein, an antibody, which has the property to interact with the antigen and form a strong complex. However, it takes several weeks to produce the antibodies in sufficiently large quantities and during this time (and also later) the animal may suffer seriously, particularly when the antigen is toxic. In addition, the surroundings in which the animals are forced to live could in many cases be better. For these and other reasons, there is a general trend to find methods to produce antibodies, not based on experimental animals. In this connection it should be stressed that one of the most famous philosophers, Professor Peter Singer, has coined the frequently quoted thesis that all sentient creatures should be treated similarly. Of moral importance is the feeling of pain and fortune. This feeling may human beings, as well as animals, have. Accordingly, there is no difference between human beings and animals in this respect. Singer´s conclusion is that there are no convincing reasons to consider human beings, i.e., Homo sapiens, to be particularly valuable and unique. One of our projects is focussed on the synthesis of artificial gel (not protein) antibodies, i.e. experimental animals are not used. The method is so simple that it can be performed in any laboratory. The artificial antibodies consist of gel granules with diameters of 0.1-0.2 mm. In these granules there are cavities which have the same shape and size as the antigen: Only the antigen will fit into the cavities and stick to their walls. Accordingly, we can easily “fish out” this particular antigen from a mixture of this antigen and many other different substances. The selectivity is, thus, extremely high. For instance, we can within 5-20 minutes decide whether a sample contains human or bovine hemoglobin, a particular mutant of a virus or a particular strain of a bacterium. The gel antibodies can certainly also be used in biosensors to detect Anthrax (to prevent bio-terrorism) and Avian Flue (and in the form of a mouth mask for protection against this and other pathological viruses and bacteria), etc., etc. Whether the gel antibodies can be employed in the form of vaccine is an open question, as is their use to remove HIV from the circulation as a method to cure people from the disease. An advantage of the artificial gel antibodies, compared to the conventional protein antibodies, is that they are much more stable, which is of great practical importance when used in not very well equipped laboratories in the poor (African) countries by people with low scientific education. 4