Kväve Metabolism
advertisement

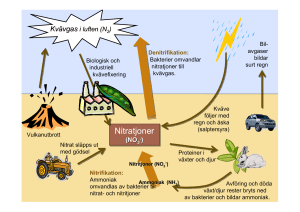
Kväve Metabolism Elin Johansson, Maria Grahn och Beatrice Lundin KE0026 Stefan Knight 2004-05-31 Inledning Tillförsel av kväve till naturen sker genom olika processer som tex urladdningar vid åskväder, gödsling och med hjälp av kvävefixerande organismer. I naturen är det bara vissa prokaryota organismer som har förmågan att fixera atmosfäriskt kväve som sedan kan användas vid syntes av andra molekyler. Högre stående organismer har inte denna förmåga utan är helt beroende av att dessa ”enkla” organismer förser dem med denna viktiga beståndsdel. Bakterier fixerar årligen ca 200 miljoner ton kväve per år i landekosystemen. Symbios mellan bakterier och växter Den största andelen av kvävefixering sker via sk kvävefixerande bakterier. Dessa verkar oftast i symbios med en växt, vanligen ärtväxter, och är lokaliserade till växtens rotsystem. Där befinner sig bakterierna inneslutna i ”rotknölar” där utbyte av näringsämnen kan ske mellan värdväxten och bakterien. Växten förser bakterien med skydd och kolhydrater medan bakterien tillhandahåller växten med kväve. Kväve behövs för uppbyggnad av nukleotider och aminosyror som i sin tur är viktiga i bla DNA. Fixeringen av atmosfäriskt kväve på detta sätt sker genom enzymet nitrogenas som finns i bakterierna. Nitrogenas omvandlar N2 till ammoniak, NH3, och ammoniumjoner, NH4+. N2 + 3 H2 ‡ 2 NH3 (1) Kvävgasmolekylen som innehåller en trippelbindning kräver stora mängder energi för att brytas. Denna energi fås i form av hydrolys av ATP. Den totala reaktionen kan tecknas: N2 + 10 H+ + 8 e- + 16 ATP ‡ 2 NH4+ + 16 ADP + 16 Pi + H2 (2) Fixeringen sker i bakterierna under “normala” förhållanden med avseende på temperatur och tryck. Energimängden, 16 ATP, som krävs är att jämföra med den industriella process där trippelbindningen bryts och N2 omvandlas till ammoniak. Där behövs energitillförsel i form av en temperatur på ca 500 ºC och ett tryck på ca 300 atm. Det är i form av ammoniak och ammoniumjoner som kväve sedan går vidare i sitt kretslopp. 2 Kvävets kretslopp Bild 1. Kvävets kretslopp (Campbell, 1999) Efter det att kväve har fixerats i bakterierna finns det flera alternativa reaktionsvägar, se bild 1. 1. Upptag direkt av värdväxten för omvandling till aminosyror. Eftersom ammoniak är skadligt för växten måste det omvandlas omedelbart. Detta sker genom att syntetisera aminosyran glutamat från NH4+ och a-ketoglutarat genom inverkan av enzymet glutamat dehydrogenas. NH4+ + a-ketoglutarat + NADPH + H+ ‡ glutamat + NADP+ + H2O (3) Glutamat omvandlas sedan vidare till aminosyran glutamin genom fortsatt reaktion med NH4+. Glutamat ger även upphov till ett flertal andra aminosyror. 2. Utsläpp av ammoniak till jorden. Ammoniak tillförs jorden på olika sätt, dels genom överskott från de kvävefixerande bakterierna, dels från nedbrytning av organiskt material samt från gödsling och nederbörd. I jorden finns olika bakterier som har förmågan att omvandla ammoniak till nitratjoner, NO3-, detta kallas nitrifikation. Bakterierna använder syret från nitrat istället för syrgas till sin cellandning. 3 Det är i form av nitratjoner som kväve kan lagras i marken. Alla växter har möjlighet att tillgodogöra sig kväve genom nitrat. 3. Kvävet går vidare i näringskjedjan genom växtätarna. Nedbrytningen i magtarmkanalen spjälkar upp växternas proteiner och aminosyror vilket frigör kvävet för uppbyggnad av nya aminosyror. Vissa aminosyror, sk essentiella, måste tillföras via födan då alla aminosyror inte kan syntetiseras pga avsaknad av vissa enzymer. Genom avföring och död återförs kvävet till markens kretslopp. 4. Deniktrifikation innebär att vissa bakterier i marken omvandlar nitrat direkt till kvävgas under anaeroba förhållanden. Eftersom detta sker i en syrefri miljö använder bakterierna nitratet i stället för syre vid ATP-syntes och detta genererar kvävgas som en restprodukt. Nitrogenaskomplexet och dess funktion Nitrogenaskomplexet består av ett flertal olika protein bla dinitrogenas reduktas och dinitrogenas. Dinitrogenas reduktas består av två identiska subenheter, en sk dimer. Dess redoxcenter består av Fe4-S4 komplex, som har två bindningsställen för ATP. Huvudfunktionen för dinitrogenas reduktas är att transportera elektroner. Komplexet oxideras och reduceras av en elektron. För att en elektron ska transporteras krävs 2 ATP. När ATP binder och hydrolyseras sker en konformationsförändring som för proteinet närmare dinitrogenas. Redox-potentialen sänks och på så sätt kan elektroner lättare överföras till reduktioncentret i dinitrogenas. Dinitrogenas är en a2b2 tetramer där a och b subenheterna är väldigt lika varandra och homologa. Ett annat namn för proteinet är Molybdenum-Järn protein (MoFe-protein). Proteinet består i sin tur av en FeMo cofaktor (se bild 2) och ett P-kluster där FeMo cofaktorn består av två FeMoS kluster medan P-klustret består av två stycken Fe4-S3 kluster. Dinitrogenas FeMo cofaktor _ P-kluster _ 2 Fe3MoS3 kluster 2 Fe4-S3 kluster Bild 2. FeMo-cofaktor med inbundet kväve. (Stryer, 2002) 4 När elektroner transporteras från dinitrogenas reduktas tas de emot av P-klustret för vidare överföring till FeMo cofaktorn. Varje FeMo cofaktor kan binda till sig en N2, detta görs pga att varje järnatom endast har bundit tre andra atomer och därför har möjlighet att binda en atom till, vilket blir kvävet. Pga kväve-järn interaktionerna i komplexet försvagas bindningen mellan kväveatomerna och därigenom sänks aktiverinsenergin för reduktion. Av de totalt 8 elektroner som krävs för fixeringen går 6 st till själva kvävereduceringen och 2 st går till bildandet av H2. Vätgas bildas som en energislösande biprodukt vid kvävefixering. Se reaktion 2. Kvävefixeringen sker hos bakterier i en anaerob miljö. En syrefattig miljö är nödvändig för en effektiv process eftersom enzymet nitrogenas inhiberas av syre. Hur kan en reduktionsprocess ske i en oxidativ miljö? Trots att nitrogenas inhiberas av syre kan reduktionsprocessen ske i en syrerik miljö. Bakterierna har löst detta problem med anpassningar av olika slag. 1. Vissa aeroba bakterier har möjlighet att delvis koppla om elektrontransporten från ATP syntesen för att kunna förbränna syre. Syret förbränns direkt när det kommer in i cellen och det avges värme. 2. Cyanobakterier omvandlar var nionde cell till en specialiserad kvävefixerande cell med tjockare väggar för att förhindra att syre tar sig in. Denna typ av cell kallas för heterocyst. 3. Bakterier som lever i symbios med växter kapslas in i rotknölar. Se bild 3. I hålrummet inuti knölen som bakterien befinner sig i finns en vätska som innehåller leghemoglobin. Det är ett syrebindande protein som produceras av växten. Leghemoglobinet transporterar bort det syre som kommer in i rotknölarna och skapar den syrefattiga miljö som krävs. Bild 3. Rotknölar (Lehninger,1993) Från ammoniak till aminosyra När kvävet har fixerats reduceras det till ammoniak och ammoniumjoner. Dessa tas sedan tillvara för bildningen av aminosyror. _-ketoglutarat, en intermediär från citronsyracykeln, bildar tillsammans med ammoniumjoner aminosyran glutamat. Se reaktion (3). Glutamat omvandlas sedan vidare till glutamin genom reaktionen: NH4+ + glutamat + ATP ‡ glutamin + ADP + Pi (4) Alla organismer bildar glutamat och glutamin men enbart de prokaryota har förmågan att bilda glutamat från glutamin vilket sker då NH4+ koncentrationen är låg. 5 Glutamat och glutamin är basen för alla andra aminosyror då de bidrar med aminogrupper. Kolskelettet byggs upp av intermediärer från citronsyracykeln, glykolysen eller från ”the pentose phosphat pathway”. Olika aminosyror är olika ”svåra” att syntetisera och det är framförallt de aromatiska som är mest komplexa. Det är dessa som oftast är essentiella och behöver tas in genom födan. Urea-cykeln Det finns olika sätt för kvävet i aminosyror att återvända till kretsloppet, dels genom nedbrytning av dött organiskt material, dels via avföring och urin. Fiskar har förmågan att avlägsna kväve i form av ammoniak. Fåglar och reptiler utsöndrar kväve i form av urinsyror medan människor och djur bildar urinämne, sk urea. Dessa olika anpassningar är en följd av tillgången på vatten. Urinämne skapas i urea-cykeln där aminosyror bryts ner för att återvända till naturen. Se bild 4. I mitokondrierna kondenseras ammoniumjoner tillsammans med koldioxid och bildar carbamoyl fosfat, det är i denna form kväve går in i urea cykeln. Carbamoyl fosfat reagerar med ornithine och bildar citrullin som transporteras till cytosolen. Aspartat bidrar med ytterligare ett kväve genom att reagera med citrullin och bilda arginosuccinate som sedan delas för att bilda arginin och fumarate. Fumarate går in i citronsyracykeln medan arginin hydrolyseras och bildar urea och regenerarar ornithine som går tillbaka in i urea cykeln. Urea transporteras sedan via blodet till njurarna för att utsöndras ur kroppen i form av urin. Bild 4. Urea-cykeln (Stryer, 2002) Sammanfattning Kväve är en av de viktigaste byggstenarna i uppbyggnaden av levande organismer. Eftersom det enbart är vissa bakterier som har förmågan att fixera atmosfäriskt kväve är vi väldigt beroende av dem. Kvävets kretslopp består av många olika vägar tack vare bakteriernas mångfald. Nitrogenas är ett oerhört komplext enzym där forskning om dess funktion och struktur fortfarande pågår. Vi har därför valt att inte gå in på för djupa detaljer angående enzymet. I bild 5 sammanfattas kvävets kretslopp och dess reaktionsvägar väl. 6 Bild 5. Kvävets kretslopp. (Campbell, 1999) Litteratur • • • • • • Stryer. L, Berg. J M, Tymoczko. J L, Biochemistry, 5 ed, W.H Freeman & Co, 2002 Lehninger. A L, Nelson. D L, Cox. M M , Principles of Biochemistry, 2 ed, Worth Publishers, 1993 Campbell. M K, Biochemistry, 3 ed, Harcourt Brace & Co, 1999 Sprent. J I, Sprent. P, Nitrogen Fixing Organisms, Chapman and Hall, 1990 Karlsson. J, Krigsman. T, Molander. B O, Wickman. P O, Biologi 1, 1 ed, Liber Utbildning AB, 1994 http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=1 2642670 7